
【题目】下图为碘晶体晶胞结构。有关说法中正确的是( )
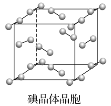
A. 碘晶体为无限延伸的空间结构,是原子晶体
B. 用切割法可知平均每个晶胞中有4个碘原子
C. 碘晶体中的碘原子间存在非极性键和范德华力
D. 碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
科目:高中化学 来源: 题型:
【题目】下列有关实验现象和解释或结论都正确的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 取硫酸催化淀粉水解的反应液,滴入少量新制 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
B |
| 有白色絮状沉淀生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 将充满 | 红棕色变深 | 反应 |
D | 向 | 得到红褐色透明液体 | 得到 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下碳酸、亚硫酸、次氯酸的电离平衡常数如下表:
H2CO3 | H2SO3 | HClO |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
K2=5.61×10-11 | K2=1.02×10-7 |
下列说法正确的是
A. 相同条件下,同浓度的 H2SO3溶液和 H2CO3溶液的酸性, 后者更强
B. Na2CO3溶液中通入少量SO2: 2CO3 2- + SO2+ H2O = 2HCO3 - + SO3 2-
C. NaClO 溶液中通入少量CO2:2ClO- + CO2 + H2O = 2HClO + CO3 2-
D. 向氯水中分别加入等浓度的 NaHCO3 和 NaHSO3溶液,均可提高氯水中 HClO 的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列有关判断中正确的是( )
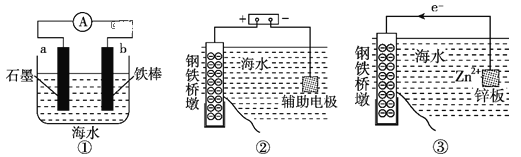
A.用装置①模拟研究时未见a上有气泡,说明铁没有被腐蚀
B.②中桥墩与外加电源正极连接能确保桥墩不被腐蚀
C.③中采用了牺牲阳极的阴极保护法保护桥墩
D.①②③中海水均是实现化学能与电能相互转化的电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取SO2并验证SO2某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:
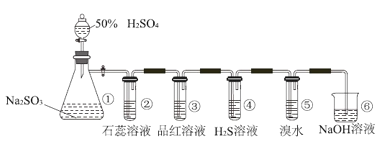
(1)①中发生反应的离子方程式为_____。
(2)③的实验现象是_____,证明SO2有_____性。
(3)④中SO2做_____剂。
(4)⑤中反应生成两种强酸,该反应的离子方程式是_____。
(5)⑥的作用是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数φ(X)随pH的变化如图所示。
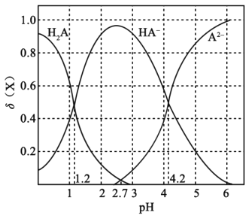
下列叙述错误的是( )
A.pH=1.2时,c(H2A)=c(HA-)
B.lg[K2(H2A)]=-4.2
C.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是化学电源的雏形。若保持如图所示原电池的电池反应不变,下列说法正确的是
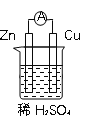
A. Zn可以换成Fe
B. Cu可以换成石墨
C. 稀H2SO4可以换成蔗糖溶液
D. 稀H2SO4可以换成CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主要过程如下图所示。

已知:几种物质中化学键的键能如下表所示。
化学键 | H2O中H—O键 | O2中O=O 键 | H2中H—H键 | H2O2中O—O键 | H2O2中O—H键 |
键能kJ/mol | 463 | 496 | 436 | 138 | 463 |
若反应过程中分解了2 mol水,则下列说法不正确的是
A. 总反应为2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B. 过程I吸收了926 kJ能量
C. 过程II放出了574 kJ能量
D. 过程Ⅲ属于放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时,Ksp(MnS)=4.65×10-14,Ksp(MnCO3)=2.24×10-11,298K下,MnS、MnCO3(R2-代表S2-或CO32-)在水中的溶解曲线如图所示:
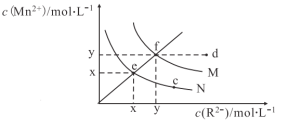
下列说法正确的是( )
A.图象中x约等于5.0×10-6
B.其它条件不变,加热N的悬浊液可使溶液组成由e点沿ef线向f点方向移动
C.常温下,加水稀释M溶液可使溶液组成由d点沿df线向f点方向移动
D.向含有MnS和MnCO3的饱和溶液中加少量MnCl2,c(CO32-)/c(S2-)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com