
【题目】某种工业废水中含有一定量的Cr2O72-和CrO42-,它们易被人体吸收积累而导致肝癌。污水处理厂常用还原沉淀法处理含铬废水,其流程如下:
![]()
(1)已知第①步存在平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
① Cr2O72-中Cr的化合价是 。
② 常温下,若平衡体系的pH=10,则溶液显 色。
(2)第②步发生反应的离子方程式为 ,还原1 mol Cr2O72-离子,需要 mol的FeSO4·7H2O;
(3)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L,溶液的pH应调至 。
【答案】
(1)①+6;②黄;
(2)6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;6;
(3)5;
【解析】
试题分析:(1)①Cr2O72-中O的化合价为-2价,由离子中元素化合价的代数和等于所带电荷数可得,Cr的化合价为+6,故答案为:+6;
②若平衡体系的pH=10,溶液显碱性,氢氧根离子与氢离子反应,则c(H+)减小,平衡2CrO42-(黄色)+2H+Cr2O72-(橙色)+H2O左移,溶液呈黄色,故答案为:黄;
(2)第②步中Cr2O72-与Fe2+反应生成Fe3+和Cr3+,其反应的离子方程式为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;根据电子得失守恒可知,还原1molCr2O72-离子得到Cr3+,得电子为2×(6-3)=6mol,需要FeSO47H2O的物质的量为6÷(3-2)=6mol,故答案为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;6;
(3)当c(Cr3+)=10-5mol/L时,溶液的c(OH-)=![]() =10-9mol/L,c(H+)═
=10-9mol/L,c(H+)═![]() =10-5mol/L,则pH=5,即要使c(Cr3+)降至10-5mol/L,溶液的pH应调至5,故答案为:5。
=10-5mol/L,则pH=5,即要使c(Cr3+)降至10-5mol/L,溶液的pH应调至5,故答案为:5。


科目:高中化学 来源: 题型:
【题目】下列有关垃圾处理的方法不正确的是 ( )
A.垃圾处理常用的方法是卫生填埋、焚烧、堆肥
B.将垃圾分类回收是垃圾处理的发展方向
C.填埋垃圾不需处理,只深埋即可
D.焚烧垃圾产生大量污染空气的物质,故不易采用此方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( ) ①参加反应的物质的性质是影响化学反应速率的主要因素②光是影响某些化学反应速率的外界条件之一③决定化学反应速率的主要因素是浓度 ④不管什么反应,增大浓度,或加热或加压,或使用催化剂,都可以加快反应速率.
A.①②
B.②③
C.③④
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列
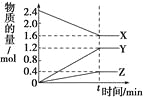
表述中正确的是
A. 反应的化学方程式为2X = 3Y + Z
B. t时,正、逆反应都不再继续进行,反应达到化学平衡
C. 若t=4,则0~t的X的化学反应速率为0.1 molL-1min-1
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是
A. 无水硫酸铜、蔗糖 B. 硅胶、硫酸亚铁
C. 食盐、硫酸亚铁 D. 生石灰、食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)若甲学生在实验过程中,记录滴定前滴定管内液面读数为1.10 mL,滴定后液面如图,则此时消耗标准溶液的体积为 。

(2)乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.11 |
2 | 25.00 | 1.56 | 31.30 |
3 | 25.00 | 0.22 | 26.31 |
选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为 (小数点后保留四位)。
(3)下列哪些操作会使测定结果偏高 (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲设计一个实验验证红热的炭与浓硫酸发生反应所生成的各种产物。某同学设计的实验流程依次为:气体产物、无水硫酸铜、品红溶液1、酸性高锰酸钾、品红溶液2、澄清石灰水。

(1)红热的炭与浓硫酸发生反应的实验装置如图,仪器a的名称为________,在使用前需要检漏,检漏的方法是_________。
(2)能证明红热的炭与浓硫酸反应产物中有CO2的实验现象为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com