
【题目】(1)有以下物质: ①NaHSO4晶体②SO3③液态硫酸 ④铁⑤BaSO4固体⑥饱和FeCl3溶液⑦酒精(C2H5OH)⑧熔融的K2SO4,其中能导电的是__________,属于电解质的是__________,属于非电解质的是__________
(2)下列各组化学用语中:①3He、4He ② 2H2 O、1H2O ③ 1H、3H ④14N和13C质子数相同的有_________,中子数相同的有________,互为同位素的有________
(3)化学反应FeS+H2SO4(浓)![]() Fe2(SO4)3+SO2↑ +S↓ +H2O(未配平)中:氧化产物是:__________, 还原产物是:__________
Fe2(SO4)3+SO2↑ +S↓ +H2O(未配平)中:氧化产物是:__________, 还原产物是:__________
(4)请写出醋酸(CH3COOH)与氢氧化钠溶液反应的离子方程式_______
(5)盐酸可以除铁锈,请写出发生反应的离子方程式:__________
(6)工业上常用H2O2在酸性条件下氧化污水中的Fe2+,请写出离子方程式:__________
【答案】④⑥⑧ ①③⑤⑧ ②⑦ ①②③ ④ ①③ Fe2(SO4)3;S SO2 CH3COOH+OH-=CH3COO-+H2O Fe2O3+6H+=2Fe3++3H2O 2Fe2++ H2O2+2H+=2Fe3++2H2O
【解析】
(1)电解质和非电解质的前提必须是化合物,单质和混合物既不是电解质也不是非电解质。常见的电解质有:酸、碱、盐、活泼金属氧化物,水;常见的非电解质有:蔗糖、酒精,淀粉等大多数的有机物,非金属氧化物,氨气等。
(2)质子数相同,中子数不同的原子互为同位素。
(3)化学反应FeS+H2SO4(浓)![]() Fe2(SO4)3+SO2↑ +S↓ +H2O中铁元素化合价+2变化为+3价,被氧化得到氧化产物Fe2(SO4)3,FeS中硫元素化合价-2价变化为0价,化合价升高失电子被氧化,得到氧化产物S,硫酸中硫元素化合价+6价变化为+4价,被还原得到还原产物SO2。
Fe2(SO4)3+SO2↑ +S↓ +H2O中铁元素化合价+2变化为+3价,被氧化得到氧化产物Fe2(SO4)3,FeS中硫元素化合价-2价变化为0价,化合价升高失电子被氧化,得到氧化产物S,硫酸中硫元素化合价+6价变化为+4价,被还原得到还原产物SO2。
(4)醋酸(CH3COOH)与氢氧化钠溶液反应生成醋酸钠和水,醋酸为弱电解质,反应的离子方程式为:CH3COOH+OH-=CH3COO-+H2O。
(5)盐酸可以除铁锈是氧化铁和盐酸反应生成氯化铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O。
(6)工业上常用H2O2在酸性条件下氧化污水中的Fe2+,生成铁离子和水,结合电荷守恒、电子守恒、原子守恒配平得到离子方程式为:2Fe2++ H2O2+2H+=2Fe3++2H2O。
(1)①NaHSO4晶体不能导电,熔融或水溶液中能导电,属于电解质;②SO3不能导电,本身不能电离,属于非电解质;③液态硫酸不能导电,溶于水导电,属于电解质;④铁里有自由电子能导电,是单质,既不是电解质也不是非电解质;⑤BaSO4固体不能导电,熔融状态导电,是电解质;⑥饱和FeCl3溶液能导电,是混合物,既不是电解质也不是非电解质;⑦酒精(C2H5OH)不能导电,属于非电解质;⑧熔融的K2SO4存在自由移动的离子能导电,属于电解质;故其中能导电的是④⑥⑧;属于电解质的是①③⑤⑧,属于非电解质的是②⑦,故答案为:④⑥⑧;①③⑤⑧;②⑦。
(2)质子数相同的是同种元素,故质子数相同的有①②③;中子数=质量数-质子数,中子数相同的有④;质子数相同,中子数不同的原子互为同位素,互为同位素的有①③,故答案为:①②③;④;①③。
(3)化学反应FeS+H2SO4(浓)![]() Fe2(SO4)3+SO2↑ +S↓ +H2O中铁元素化合价+2变化为+3价,被氧化得到氧化产物Fe2(SO4)3,FeS中硫元素化合价-2价变化为0价,化合价升高失电子被氧化,得到氧化产物S,硫酸中硫元素化合价+6价变化为+4价,被还原得到还原产物SO2,故答案为:Fe2(SO4)3,S;SO2。
Fe2(SO4)3+SO2↑ +S↓ +H2O中铁元素化合价+2变化为+3价,被氧化得到氧化产物Fe2(SO4)3,FeS中硫元素化合价-2价变化为0价,化合价升高失电子被氧化,得到氧化产物S,硫酸中硫元素化合价+6价变化为+4价,被还原得到还原产物SO2,故答案为:Fe2(SO4)3,S;SO2。
(4)醋酸(CH3COOH)与氢氧化钠溶液反应生成醋酸钠和水,醋酸为弱电解质,反应的离子方程式为:CH3COOH+OH-=CH3COO-+H2O,故答案为:CH3COOH+OH-=CH3COO-+H2O。
(5)盐酸可以除铁锈是氧化铁和盐酸反应生成氯化铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O。
(6)工业上常用H2O2在酸性条件下氧化污水中的Fe2+,生成铁离子和水,结合电荷守恒、电子守恒、原子守恒配平得到离子方程式为:2Fe2++ H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++ H2O2+2H+=2Fe3++2H2O。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】(1)由蒸发海水制得的粗盐中常含有Na2SO4、CaCl2和MgCl2等杂质,在食盐生产过程中需要将这些杂质除去。请回答:
Na2SO4、CaCl2和MgCl2在溶液中能形成Na+、Ca2+、Mg2+、SO42━、和Cl━五种离子。要除去其中的Mg2+,离子方程式为____________,检验其中的SO42━的方法________________;
(2)Na2CO3固体中混有少量NaHCO3,除去杂质的方法是_________,反应方程式为________________;
(3)除去CO2气体中少量HCl,所用试剂是__________,反应的化学方程式为______________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去)。
![]()
(1)A、B、C、W均为气体,若A是无色有刺激性气味的气体, 气体B遇到空气变成红棕色。
①写出气体C溶于水的化学方程式______________;
②检验气体A的操作方法是______________;
(2)若A是一种黄绿色的气体,W是一种常见的金属单质。
①实验室制取气体A的离子方程式________________;
②B与W转化为C的离子反应方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )

A. 该有机物的分子式为C7H7O3
B. 该有机物能发生取代、加成和氧化反应
C. 1mol该有机物最多能与2mol H2发生加成反应
D. 该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。四种元素形成的单质依次为m、n、p、q;这些元素组成的二元化合物r、t、u,其中u为形成酸雨的主要物质之一;25℃时,0.01mol/L的v溶液中pH=12。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径的大小:W>Z>Y>X
B. v能抑制水的电离而u能促进水的电离
C. 粘有q的试管可用酒精洗涤
D. Z分别与Y、W组成的化合物中化学健类型可能相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是短周期元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。
(1) HWO的结构式为____。
(2) ①X、Y、Z、W原子半径由大到小依次是____(填元素符号)。
②X、Z、W最高价氧化物水化物酸性由强到弱依次是_________。(填化学式)。
(3) W同族上一周期元素单质不能把W元素从其钠盐的水溶液中置换出来,用化学方程式解释____________________。
(4) ①家用“管道通”的有效成分是烧碱和Y的单质,使用时需加入一定量的水,此时发生反应的化学方程式为_________________________。
②含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式__________________________________。
(5) NW3是黄色油状液体,无漂白性,在热水中会发生水解。NW3的电子式为____。若取该液体滴入50℃左右的热水中,片刻后取该热水溶液滴到干燥的红色石蕊试纸上,试纸先变蓝后褪色。写出NW3在热水中发生水解的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种有机化合物甲、乙的球棍模型如图所示,下列说法错误的是
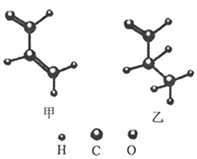
A. 甲、乙互为同系物,都能使酸性高锰酸钾溶液褪色
B. 甲分子中所有原子可能处于同一平面内
C. 用红外光谱能区分甲、乙两种物质
D. 一定条件下,甲与足量H2反应后,可得到1-丙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com