
【题目】一定温度下,在一容器内进行某一反应,M、N的物质的量随反应时间变化的曲线如下图所示,则下列叙述中,正确的是( )

A. 反应的化学方程式一定为2M![]() N
N
B. ![]() 时,逆反应速率一定大于正反应速率
时,逆反应速率一定大于正反应速率
C. ![]() 时,反应达到了化学平衡状态
时,反应达到了化学平衡状态
D. ![]() 时,正反应速率等于逆反应速率
时,正反应速率等于逆反应速率
科目:高中化学 来源: 题型:
【题目】关于有机物a(![]() )、b(
)、b(![]() )、c(
)、c(![]() )的说法正确的是
)的说法正确的是
A. a、b、c的分子式均为C8H8
B. a、b、c均能与溴水发生反应
C. a、b、c中只有a的所有原子会处于同一平面
D. a、b、c的一氯代物中,b有1种,a、c均有5种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
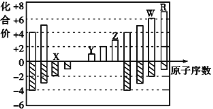
A. 气态氢化物的稳定性:R>W
B. X与Y可以形成原子个数比为1∶1和1∶2的两种离子化合物
C. 由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2-
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
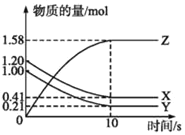
(1)写出该反应的化学方程式___________________
(2)下列叙述中不能说明上述反应达到平衡状态的是___________.
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(3)为使该反应的反应速率减小,可采取的措施是_____.
A 恒压时充入Ne B 适当升高温度
C 缩小容器的体积 D 选择高效催化剂.
II.一定温度下将3mol的A及3molB混合于2L的密闭
容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60﹪,C的平均反应速率是0.18mol/(L.min)。
xC(g)+2D(g),经过5分钟后反应达到平衡,测得A的转化率为60﹪,C的平均反应速率是0.18mol/(L.min)。
求:(1)平衡时B的浓度=______mol/L。
(2)D的平均反应速率υ(D)=______mol/( L.min)。
(3)x=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:

请回答下列问题:
(1)反应I的化学方程式为_____________________________________。1mol H2SO4(液)分解成气态物质需要吸收的能量是275.5kJ,硫的燃烧热为297 kJ·mol-1,则反应Ⅱ的热化学方程式为________________________________。
(2)单质硫也可以生成多硫化物实现能量间的转化。
①钠硫电池是一种新型高能电池,总反应为2Na+xS ![]() Na2Sx,该电池工作时的正极反应式为____________________,给该电池充电时,钠电极应与外电源的____________(填“正”或“负”)极相连接。
Na2Sx,该电池工作时的正极反应式为____________________,给该电池充电时,钠电极应与外电源的____________(填“正”或“负”)极相连接。
②多硫化合物H2S2O8中S的化合价为+6,分子中过氧键的数目为______________________。
③在碱性溶液中,多硫离子Sx2-被BrO![]() 氧化成SO
氧化成SO![]() ,
,![]() 被还原成Br-。该反应的离子方程式是________________________。
被还原成Br-。该反应的离子方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)及其化合物与生产、生活密切相关,广泛应用在杀虫剂以及药物中。回答下列问题:
(1)砷是第四周期VA族元素。下列关于第VA族元素及其化合物的说法不正确的是_______(填序号)。
a.沸点:PH3<NH3
b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(2)工业生产中常用“古氏试砷法”检验微量砷,其反应原理为:
①将含砷化合物转化为具有极强还原性的AsH3;
②AsH3与AgNO3溶液反应产生As2O3与另一种固体,该反应的离子方程式为_____________。
(3)砷及其化合物几乎都有毒,通常+3价砷化合物毒性强于+5价砷化合物。海产品中含有微量+5价砷化合物,食用海鲜后不能马上进食水果的原因是________________________________。
(4)砷酸(H3AsO4)可用于制造杀虫剂、药物。As2O3溶于稀硝酸中可得砷酸,此反应的化学方程式为________________________________。
(5)利用单质铁处理水体砷污染的原理为:单质铁在水体中被氧化腐蚀得到水合氧化铁[Fe(OH)3和FeOOH],吸附沉降砷的化合物。在其它条件一定时,调节水样的pH,得到除砷效率曲线如图所示。
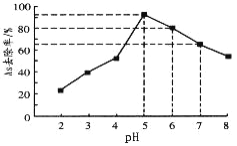
①请解释水样酸性较强时,除砷效率较低的原因是_____________________。
②国家饮用水标准规定水中砷的含量应低于0.05mg·L-1(1mg=1000μg)。某水样中含砷总浓度为100μg·L-1,若控制水样的pH=6,出水后的砷浓度_________________(填“能”或“否”)达到饮用水标准。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O![]() Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
D |
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法不正确的是
A. 100mL l mol·L-1KClO溶液中,阴离子的数目大于0.1NA
B. 14g乙烯和丙烯混合气体中含有C—H共价键的数目为2NA
C. 5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等
D. 含0.4molHNO3的浓硝酸与足量铜反应,转移的电子数等于0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是资源的宝库:合理利用海水资源是当今是世界研究的重点课题。结合所学知识回答下列问题:
(1)列举一项海水中的能源:__________ ,海水中储量最大的资源是________ ,获得该资源最古老的方法是____________。
(2)海水中还有大量NaCl,MgCl2等盐类物质,从海水中获得纯净NaCl的分离提纯方法有过滤、______。
(3)目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:
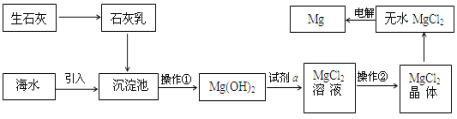
提示: MgCl2晶体的化学式为MgCl26H2O; MgO的熔点为2852℃,无水MgCl2的熔点为714℃。
①操作②的名称___________、冷却结晶、过滤。
②用氯化镁电解生产金属镁的化学方程式为:_____________________。
(4)粗盐提纯后的的卤水中含有大量的溴,从中提取溴的部分过程如下:

实验室模拟上述过程设计以下装置进行实验(所有橡胶制品已被保护,夹持装置已略去)

①A装置中通入a气体的目的是(用离子方程式表示) __________________________________________;
②A装置中先通入a气体后改通热空气。通入热空气的目的是______________________________________;
③B装置中b气体是SO2,目的是吸收富集Br2,此处离子方程式为___________________________________;
④向B装置中再次通入Cl2得到单质溴,对液体进行蒸馏,收集液溴。蒸馏应该选择下列仪器_____(填序号) 。
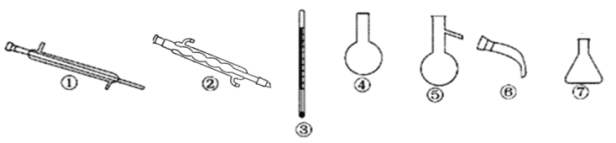 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com