
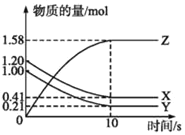
����Ŀ��I.һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ��
(1)д���÷�Ӧ�Ļ�ѧ����ʽ___________________
(2)���������в���˵��������Ӧ�ﵽƽ��״̬����___________��
A����X��Y�ķ�Ӧ����֮��Ϊ1��1
B���ڻ��������X�������ٷ������ֲ���
C����������ƽ��Ħ����������ʱ��ı仯���仯
D�����������ܶȲ���ʱ��ı仯���仯
E��X��Y��Z��Ũ��֮��Ϊ1��1��2
(3)Ϊʹ�÷�Ӧ�ķ�Ӧ���ʼ�С���ɲ�ȡ�Ĵ�ʩ��_____��
A ��ѹʱ����Ne���� ��B �ʵ������¶�
C ��С��������� D ѡ���Ч������
II.һ���¶��½�3mol��A��3molB�����2L���ܱ�
�����У��������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(g)������5������Ӧ�ﵽƽ�⣬���A��ת����Ϊ60����C��ƽ����Ӧ������0.18mol/(L.min)��
xC(g)+2D(g)������5������Ӧ�ﵽƽ�⣬���A��ת����Ϊ60����C��ƽ����Ӧ������0.18mol/(L.min)��
��(1)ƽ��ʱB��Ũ��=______mol/L��
(2)D��ƽ����Ӧ���ʦ�(D)=______mol/( L.min)��
(3)x=______��
���𰸡�X(g)+Y(g)![]() 2Z(g) ACDE A 1.2 0.12 3
2Z(g) ACDE A 1.2 0.12 3
��������
I.(1)���ݻ�ѧ��Ӧ�и����ʵ����ʵ����ı仯���뻯ѧ������֮�ȳ�������д��ѧ����ʽ��
(2)���ݿ��淴Ӧƽ��״̬ʱ��ʵ�ʺ���������Ϸ�Ӧ����ʽ�����ʵĻ�ѧ��������ϵ�ж�ƽ��״̬��
(3)����Ӱ�컯ѧ��Ӧ���ʵ����ط����жϣ�
II.����A��ʼʱ�����ʵ�����ת���ʼ���ת�������������ʶ���ʽ����V(A)��Ȼ��������ʱȵ��ڻ�ѧ�������ıȣ����V(C)��С������V(B)��V(D)��xֵ��
(1)��ͼ����Կ���X��Y�����ʵ�����С��Z�����ʵ������࣬��X��YΪ��Ӧ�ZΪ�������ѧ��Ӧ�и����ʵ����ʵ����仯���뻯ѧ������֮�ȳ����ȣ�����Y��X��Z=(1.20mol-0.41mol)��(.0mol-0.21mol)��1.58mol=1��1��2����������������ʶ����ڣ��ɼ��÷�ӦΪ���淴Ӧ����Ӧ�Ļ�ѧ����ʽΪX+Y![]() 2Z��
2Z��
(1) A.X��Y�Ƿ�Ӧ�����ʽ��ϵ����ͬ�����κ�����¶��߷�Ӧ���ʶ���ȣ���˲��ܸ���X��Y�ķ�Ӧ����֮��Ϊ1��1�ж�ƽ��״̬��A�������⣻
B.����Ӧ�ﵽƽ��״̬���κ�һ��ֵ��������䣬�����ʵ������������䣬���ڻ��������X�������ٷ������ֲ�������жϷ�Ӧ����ƽ��״̬��B���������⣻
C.���ڷ�Ӧǰ��������������䣬��������ʵ������䣬���Ի�������ƽ��Ħ���������Dz���ʱ��ı仯���仯���ʲ��ܾݴ��ж�ƽ��״̬��C�������⣻
D.���ڷ�Ӧǰ��������������䣬�����������䣬���Ի��������������ܶ����Dz���ʱ��ı仯���仯���ʲ��ܾݴ��ж�ƽ��״̬��D�������⣻
E.X��Y��Z��Ũ��֮��Ϊ1��1��2���ܴ���ƽ��״̬��Ҳ���ܲ���ƽ��״̬��E�������⣻
�ʺ���ѡ����ACDE��
(3) A.��ѹʱ����Ne���������ݻ��������ʵ�Ũ�ȼ�С����Ӧ���ʼ�С��A�������⣻���� ��B.�ʵ������¶ȣ����ʵ��������ӣ���Ӧ���ʼӿ죬B���������⣻
C.��С��������������ʵ�Ũ������ѧ��Ӧ���ʼӿ죬C���������⣻
D.ѡ���Ч��������ѧ��Ӧ���ʼӿ죬D���������⣻
�ʺ���ѡ����A��
II.������Ӧ3A(g)+B(g)![]() xC(g)+2D(g)�����ڷ�Ӧ��2L���ܱ������ڽ��У�n(A)= 3mol��A��ת������60%����Aת����Ϊ��n=3mol��60%=1.8mol��
xC(g)+2D(g)�����ڷ�Ӧ��2L���ܱ������ڽ��У�n(A)= 3mol��A��ת������60%����Aת����Ϊ��n=3mol��60%=1.8mol��
(1)���ݷ�Ӧ����ʽ��ϵ����֪��ÿ��3molA������Ӧ��ͬʱ����1molB����A��Ӧ��1.8mol������B��Ӧ��0.6mol����5minʱB���ʵ�Ũ��Ϊc(B)=(3mol-0.6mol)��2L=1.2mol/L��
(2) Aת����Ϊ��n=3mol��60%=1.8mol���������ݻ�Ϊ2L����Ӧʱ��Ϊ5min������V(A)=![]() =0.18mol/(L��min)������V(A)��V(D)=3:2������V(D)=
=0.18mol/(L��min)������V(A)��V(D)=3:2������V(D)=![]() V(A)= 0.12 mol/(L��min)��
V(A)= 0.12 mol/(L��min)��
(3)V(A):V(C)=3:x��V(A)=V(C)=0.18mol/(L��min)������x=3��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��������
A. ��ƽ����ϵ PCl5(g) ![]() PCl3(g) + Cl2(g) �м���һ������37Cl2��һ��ʱ���37Cl���������Ȼ��ס����Ȼ�������������������
PCl3(g) + Cl2(g) �м���һ������37Cl2��һ��ʱ���37Cl���������Ȼ��ס����Ȼ�������������������
B. CH3COOH��H18O��CH2CH3����������Ӧ�ǿ��淴Ӧ���ﵽƽ���18O���������Ҵ���������������������ܴ����������ˮ������
C. CH2Cl2û��ͬ���칹�����ʵ֤���˼����������̼ԭ��Ϊ���ĵ���������ṹ
D. ����������ȫȼ�պ�������ֻ��CO2��H2O���л���һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA�ǰ����ӵ�������ֵ������˵����ȷ����
A. H2O2�ֽ����1 mol O2ת�Ƶ�����Ϊ4NA
B. 0.1mol H2��0.1mol���������ܱ������г�ַ�Ӧ�������ڷ�������Ϊ0.2NA
C. 1mol NaHSO4����ʱ���������������ĿΪ2NA
D. S8���ӽṹ��ͼ��1mol�÷����к���S��S������Ϊ7NA

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�鼰�������Ƴ���Ӧ���۵���
ʵ�� | ���� | ���� | |
A | ������������Ʒ����ϡ���ᣬ�μ�KSCN��Һ | ��Һ��Ϊ��ɫ | ����������Ʒ���������� |
B | ���������Һ��ͨ��CO2 | ������ɫ���� | �ǽ����ԣ�C��Si |
C | ��ʢ��FeS������ձ��еμ����ᣬ����������ͨ����ˮ�� | ��ˮ��ɫ | ��ԭ�ԣ�S2-��Br-��Cl- |
D | ����ɫ��Һ�е����Ȼ�����Һ��ϡ���� | �а�ɫ�������� | ��ɫ��Һ��һ������SO42-��SO32- |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������е��ʱ���ر���ȷ����( )
A.H<0��S>0B.H<0��S<0C.H>0��S>0D.H>0��S<0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڡ������ᴿ�����ܽ⡢���ˡ�������ʵ�鲽���У�ʹ�ô�������������
A. �ձ� B. ������ƽ C. ������ D. ©��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ�����ڽ���ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯����������ͼ��ʾ�������������У���ȷ����( )

A. ��Ӧ�Ļ�ѧ����ʽһ��Ϊ2M![]() N
N
B. ![]() ʱ���淴Ӧ����һ����������Ӧ����
ʱ���淴Ӧ����һ����������Ӧ����
C. ![]() ʱ����Ӧ�ﵽ�˻�ѧƽ��״̬
ʱ����Ӧ�ﵽ�˻�ѧƽ��״̬
D. ![]() ʱ������Ӧ���ʵ����淴Ӧ����
ʱ������Ӧ���ʵ����淴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���Ǻϳ�����ͼ��ʾ��һϵ�е����飬�������顢�����顢������ȡ�����˵����ȷ����



������ ������ ������
A. ����֮�以Ϊͬϵ��
B. ������Ļ�ѧʽΪC18H24
C. �������������Ϊͬ���칹�壬��������![]() ��Ϊͬ���칹��
��Ϊͬ���칹��
D. ���ǵ�һ�ȴ����ֻ�����֣���������Ķ��ȴ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷�Ӧ6NO2��8NH3===7N2��12H2O���ɵ�ص�װ����ͼ��ʾ���˷�������ʵ����Ч�������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܡ�����˵����ȷ���ǣ���

A. ���������缫�������غ������Ҳ�缫
B. Ϊʹ��س����ŵ磬���ӽ���Ĥ��ѡ�������ӽ���Ĥ
C. �缫A����ӦʽΪ2NH3��6e��===N2��6H��
D. ����4.48 L NO2������ʱ��ת�Ƶ�����Ϊ0.8NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com