
【题目】下列做法中不符合“绿色化学”思想的是
A. 以水性涂料代替油性涂料
B. 以无磷洗涤剂代替含磷洗涤剂
C. 试验后的有毒有害物质应分类收集,统一处理
D. 在通风橱中制取氯气时不用NaOH溶液吸收尾气
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组为了模拟工业流程从浓缩的海水中提取液溴,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性。设计了如下操作步骤及主要实验装置(夹持装置略去):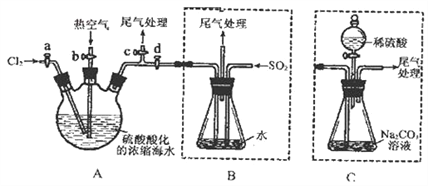
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2;
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:
(1)步骤②中鼓入热空气的作用为_____________________________;
(2)步骤③中发生的主要反应的离子方程式为______________________________。
(3)此实验中尾气可用______(填选项字母)吸收处理。
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCI溶液
(4)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了NaBrO3等,该反应的化学方程式为____________。
(5)与B装置相比,采用C装置的优点为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东北虎主要分布在我国长白山、小兴安岭等地,华南虎主要分布在我国长江流域以南地区,根据我们学过的知识判断,东北虎之所以适应了其生存环境,与华南虎相比,下列哪种物质含量所占比例明显高( )
A. 脂肪 B. 糖原 C. 蛋白质 D. 核酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对氨的实验室制法、氨气及铵盐的性质进行探究。
回答下列问题:
Ⅰ.氨气的制备
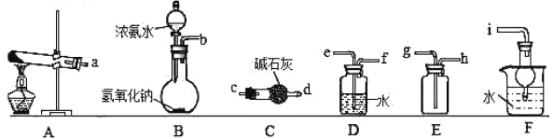
(1)若用A装置制备氨气,写出反应的化学方程式_______________。欲收集一瓶干燥的氨气,选择上图中的装置(可重复使用),其连接顺序为:a→___________(按气流方向,用小写字母表示)。
(2)用装置B,将浓氨水与氢氧化钠固体混合,也能制得氨气,请解释该法能制备氨气的原 因________________________。
Ⅱ.按下图装置进行氨气的性质实验(旋塞1和旋塞2实验前关闭),G、H是两个等体积的容器。
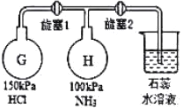
(3)先打开旋塞I,H瓶中现象是________________,原因是________________。一段时间后,关闭旋塞1,再打幵旋塞2,H瓶中现象是_________。
Ⅲ.设计实验,探究某一因素对一定物质的量浓度NH4Cl水解程度的影响。
限选试剂与仪器:NH4Cl固体、蒸馏水、烧杯、胶头滴管、玻璃棒、药匙、电子天平、pH计、温度计、恒温水浴槽(可控制温度)
(4)上述所列仪器中缺少一样必要的玻璃仪器,其名称是_______________。
(5)根据上述所给的试剂和仪器,推测实验目的:探究_______对NH4Cl水解程度的影响。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得常温下0.1 mol/L某一元酸(HA)溶液的pH不等于1,0.1 mol/L某一元碱(BOH)溶液里:![]() =10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
=10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
A.c(B+)>c(A-)>c(OH-)>c(H+)
B.c(A-)>c(B+)>c(H+)>c(OH-)
C.c(H+)>c(A-)>c(OH-)>c(B+)
D.c(B+)>c(A-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. pH=a的氨水溶液,稀释10倍后,其pH=b,则b<a-1
B. pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液中c(Na+):③<②<①
C. 某温度Ksp(Ag2S)=6×10-50, Ksp(AgCl)=2×10-6, 则 2AgCl(s)+S2-(aq)![]() Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×1037
Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×1037
D. 一定浓度的 NaHS 溶液中:c(Na+)+c(OH-)==c(H+)+c(HS-)+2c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. CS2为V形的极性分子 B. ClO3﹣的空间构型为平面三角形
C. SiF4和SO32﹣的中心原子均为sp2杂化 D. SF6中有6对相同的成键电子对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“关爱生命,注意安全”。惨痛的天津爆炸触目惊心,火灾之后依然火势绵延不绝的原因之一是易燃物中含有电石。工业上常用电石(主要成分为CaC2,杂质为CaS等)与水反应生产乙炔气。
(1)工业上合成CaC2主要采用氧热法。
已知:CaO(s)+3C(s)=CaC2(s)+CO(g) △H=+464.1kJ·mol-1
C(s)+l/2O2(g)=CO(g) △H=-110.5kJ.mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO,为维持热平衡,每生产l molCaC2,转移电子的物质的量为_______。
(2)已知2000℃时,合成碳化钙的过程中还可能涉及到如下反应
CaO(s)+C(s) ![]() Ca(g)+CO(g) K1 △H1=a KJ·mol-1
Ca(g)+CO(g) K1 △H1=a KJ·mol-1
Ca(g)+2C(s) ![]() CaC2(s) K2 △H2=b KJ·mol-1
CaC2(s) K2 △H2=b KJ·mol-1
2CaO(s)+CaC2(s) ![]() 3Ca(g)+2CO(g) K3 △H3=c KJ·mol-1
3Ca(g)+2CO(g) K3 △H3=c KJ·mol-1
则K1=_______ (用含K2、K3的代数式表示);c=_____(用含a、b的代数式表示)。
(3)利用电石产生乙炔气的过程中产生的H2S气体制取H2,既廉价又环保。
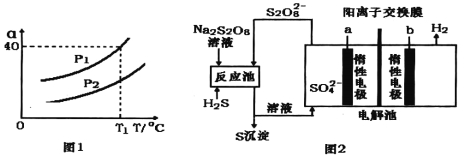
①利用硫化氢的热不稳定性制取氢气。在体积为2L的恒容密闭容器中,H2S起始物质的量为2mol,达到平衡后H2S的转化率![]() 随温度和压强变化如图l所示。据图计算T1℃时压强P1时,硫为气态,则平衡体系中H2的体积分数_____。由图知压强P1__P2(填“大于”“小于”或“等于”),理由是______。
随温度和压强变化如图l所示。据图计算T1℃时压强P1时,硫为气态,则平衡体系中H2的体积分数_____。由图知压强P1__P2(填“大于”“小于”或“等于”),理由是______。
②电化学法制取氢气的原理如图2,请写出反应池中发生反应的离子方程式_____,惰性电极a上发生的电极反应式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com