
【题目】室温下,将1.000 mol/L盐酸滴入20.00 mL 1.000 mo1/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )
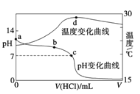
A. a点由水电离出的c(H+) = 1.0 × 10-14 mo1/L
B. b点:c(NH4+) > c(Cl-) > c(OH-) > c(H+)
C. c点:盐酸与氨水恰好完全反应
D. d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
【答案】B
【解析】
根据酸碱中和反应过程中pH和温度的变化,分析解释水的电离、恰好中和、离子浓度间的关系。
A项:a点未加盐酸,1.000mol/L氨水的7<pH<14,则c(H+)> 10-14 mo1/L,氨水中只有水电离生成氢离子,即c(H+)水=c(H+)> 10-14 mo1/L,A项错误;
B项:b点加入一定量盐酸后溶液仍为碱性,c(OH-) > c(H+),据电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-),则c(NH4+)>c(Cl-),故有c(NH4+) > c(Cl-) > c(OH-) > c(H+),B项正确;
C项:盐酸与氨水恰好完全反应时,生成的氯化铵水解溶液呈酸性,而c点溶液呈中性,必有少量氨水剩余,C项错误;
D项:d点时混合液温度最高,此时恰好反应,之后,过量的盐酸使溶液温度略下降,D项错误。
本题选B。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为常见的有机物,它们之间有如下转化关系。已知:①A是一种植物生长调节剂,有催熟作用;②醛基在氧气中易被氧化成羧基。回答下列问题: 
(1)A和B中官能团名称分别是___和___。
(2)在F的众多同系物中:最简单的同系物其空间构型为___;含5个碳原子的同系物其同分异构体有___种,其中一氯代物种类最少的同系物的结构简式为___。
(3)反应⑥和⑦均可得到G,要制备得到较纯净的G,应该选用反应_____。
(4)反应①﹣⑦属取代反应的有___;反应④中,浓硫酸的作用是___。反应②的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国自主研发的“蓝鲸一号”在中国南海神狐海域完成可燃冰连续试采,并得到中共中央国务院公开致电祝贺。“可燃冰”是天然气水合物,外形像冰,在常温常压下迅速分解释放出甲烷,被称为未来新能源。
(1)“可燃冰”作为能源的优点是_______________________________(回答一条即可)。
(2)甲烷自热重整是一种先进的制氢方法,包含甲烷氧化和蒸汽重整两个过程。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应如下:
反应过程 | 化学方程式 | 焓变△H(kJ.mol-l) | 活化能E.(kJ.mol-1) |
甲烷氧化 | CH4(g)+ | -802.6 | 125.6 |
CH4(g)+O2(g) | -322.0 | 172.5 | |
蒸气重整 | CH4(g)+H2O(g) | +206.2 | 240.1 |
CH4(g)+2H2O(g) | +158. 6 | 243.9 |
回答下列问题:
①在初始阶段,甲烷蒸汽重整的反应速率______(填“大于”“小于”或“等于”)甲烷氧化的反应速率。
②反应CH4(g)+H2O(g)![]() CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。
CO(g)+3H2(g)的平衡转化率与温度、压强关系[其中n(CH4):n(H2O)=1:1]如图所示。

该反应在图中A点的平衡常数Kp=________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),图中压强(p1、p2、p3、p4)由大到小的顺序为___________。
③从能量角度分析,甲烷自热重整方法的先进之处在于___________。
(3)甲烷超干重整CO2技术可得到富含CO的气体,其能源和环境上的双重意义重大,甲烷超干重整CO2的催化转化原理如图所示。

①过程II中第二步反应的化学方程式为_________。
②过程II的催化剂是______,只有过程I投料比![]() _______,催化剂组成才会保持不变。
_______,催化剂组成才会保持不变。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年是“国际化学元素周期表年”。 1869 年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法中错误的是
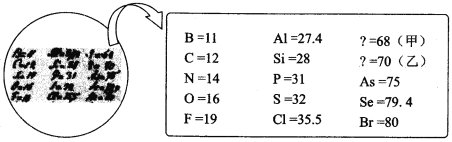
A. 甲位于现行元素周期表第四周期第ⅢA 族B. 原子半径比较:甲>乙> Si
C. 乙的简单气态氢化物的稳定性强于CH4D. 推测乙的单质可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氨气是重要的化工原料,主要用作化肥、冷冻剂等。现向一固定容积的反应器中通入2molN2和6molH2在催化剂作用下加热至平衡状态,测得此时容器内压强比反应前减小了![]() ,列式计算H2的平衡转化率___。
,列式计算H2的平衡转化率___。
(2)燃料的燃烧将化学能转化成热能,提供了人类生存和发展所需要的能量和动力。现将标况下8.96L乙烷和乙烯的混合气体和足量氧气充分混合并点燃,燃烧产物经过浓硫酸充分吸收后增重16.2g,则混合气体中乙烷和乙烯的物质的量之比为多少___?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应①2H2O(l)![]() 2H2(g)+O2(g)+Q1和反应②2H2O(l)
2H2(g)+O2(g)+Q1和反应②2H2O(l)![]() 2H2(g)+O2(g)+Q2,都是分解得到H2和O2,下列判断错误的是( )
2H2(g)+O2(g)+Q2,都是分解得到H2和O2,下列判断错误的是( )
A. 反应①中太阳能转化为化学能B. 反应②中电能转化为化学能
C. Q1>0、Q2<0D. Q1=Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲利用如图装置制取能较长时间存在的Fe(OH)2,其中实验所用溶液现配现用且蒸馏水先加热煮沸。下列分析正确的是

A. X可以是稀硫酸或稀硝酸或稀盐酸
B. 实验开始时应先关闭止水夹a、打开b,再向烧瓶中加入X
C. 反应一段时间后可在烧瓶中观察到白色沉淀
D. 反应结束后若关闭b及分液漏斗活塞,则Fe(OH)2可较长时间存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物的构型判断错误的是
A. 甲烷是正四面体结构,烷烃的碳原子呈直线形
B. 乙烯是平面结构,四个氢原子和二个碳原子共面
C. 苯分子中碳原子采用sp2杂化,得到平面正六边形结构
D. 氨气分子的空间构型为三角锥形,氮原子杂化方式为SP3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com