
����Ŀ����ͭ����Ҫ�ɷ�ΪCu2S,���̿���Ҫ�ɷ�ΪMnO2,���Ƕ���������SiO2��Fe2O3�����ʡ���ҵ���ۺ����������ֿ����Ʊ������̺ͼ�ʽ̼��ͭ����Ҫ����������ͼ:

��֪:��MnO2�ܽ����������е�������Ϊ������;
��[Cu(NH3)4]SO4�����ȶ�,����ˮ�л�ֽ�����NH3;
�۲��ֽ��������������������������pH��Χ���±���ʾ(��ʼ������pH����������Ũ��Ϊ1.0 mol��L-1����):
��ʼ������pH | ������ȫ��pH | |
Fe3+ | 1.1 | 3.2 |
Mn2+ | 8.3 | 9.8 |
Cu2+ | 4.4 | 6.4 |
��1�����ʱ,Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ��________________(��дһ��)��
��2�����ڽ���ҺpH�ķ�ΧΪ________,��Ŀ����____________________��
��3���������п�ѭ��ʹ�õ�������________(д��ѧʽ)��
��4���ڸù��յġ���������������,�����ȵ��¶Ƚϵͻ����,�������__________�Ľ����
��ˮ�������õIJ��ֹ�������ͼ��ʾ��

��1����ˮ����ȡ��NaCl��������������KClO3���壨KClO3�ܽ�����¶ȱ仯����ͨ��______��________��_________�IJ���������
��2������Mg(OH)2�õij�����һ������ʯ�һ���ʯ�ң�����Mg(OH)2�����л����Ca(OH)2����ͨ������ϴ��ȥ��Ca(OH)2����������Ƿ�ϴ���IJ�������_______________��
���𰸡� �����ʯ(�������¶Ȼ��ʵ��������Ũ�Ȼ����,��дһ�ּ���) 3.2��pH<4.4 ʹFe3+ת��Ϊ����������������ȥ NH3�� ��ʽ̼��ͭ�������� �ܽ� �����ᾧ ���ȹ��� ȡ����ϴҺ�������μ�Na2CO3��Һ���������ְ�ɫ������˵��ϴ��
��������I.��ͭ����Ҫ�ɷ�ΪCu2S�����̿���Ҫ�ɷ�MnO2����������Fe2O3��SiO2�����ʣ�����ϡ�����ȡ�����˵õ�SiO2������S����Һ�к���Fe3+��Mn2+��Cu2+���ð�ˮ������ҺpH���������µ����ʣ�ͬʱ����ʹ������ת��Ϊ���������������˳�ȥ����Һ�м���̼����狀Ͱ�ˮ�Ļ���ʹ������ת��Ϊ̼���̣�̼�����������ᷴӦ���������ᾧ�õ������̾��壬���ȹ��˵õ�����Һ���ϳ��İ�������ѭ��ʹ�ã�ͬʱ�ٹ��˵õ���ʽ̼��ͭ��
II.(1). KClO3�ܽ�����¶ȱ仯���NaCl �ܽ�����¶ȱ仯С�����ᴿNaCl(����������KClO3)ʱ����ͨ���ܽ��������ᾧ�����ȹ��˵IJ���������(2).ȡ����ϴҺ�������μ�Na2CO3��Һ���������ְ�ɫ������ϴ����
I .(1). ���ʱ��ͨ�������ʯ�������¶Ȼ���н�����ʵ��������Ũ�ȣ���������߽�ȡ�ʣ��ʴ�Ϊ�������ʯ(�������¶Ȼ��ʵ��������Ũ�Ȼ��������дһ�ּ���)��
(2). ������ҺpH��Ŀ����ʹFe3+ת��Ϊ����������������ȥ��Cu2+��Mn2+���ܳ�����Ҫ��ȥ��Һ�е�Fe3+���ӣ���ҺpH=3.2ʱFe3+������ȫ��������ҺpH=4.4ʱͭ���ӿ�ʼ��������pH��Χ��3.2��pH<4.4���ʴ�Ϊ��3.2��pH<4.4��ʹFe3+ת��Ϊ����������������ȥ��
(3). ������������֪������ѭ��ʹ�õ�������NH3���ʴ�Ϊ��NH3��
(4). �¶ȹ��ߣ���ʽ̼��ͭ�ᷢ���ֽ⣬�¶ȹ��ͣ����н϶��[Cu(NH3)4]SO4���ڣ�������ɼ�ʽ̼��ͭ�������٣��ʴ�Ϊ����ʽ̼��ͭ�������٣�
II.(1). ��KClO3���ܽ�����¶ȱ仯���NaCl �ܽ�����¶ȱ仯С����ˮ����ȡ��NaCl��������������KClO3����ʱ����ͨ���������ܽ��������ᾧ�����ȹ��˵ķ������о������ʴ�Ϊ���ܽ⣻�����ᾧ�����ȹ��ˣ�
(2). ����Mg(OH)2�õij�����һ������ʯ�һ���ʯ�ң�����Mg(OH)2�����л����Ca(OH)2����ͨ������ϴ��ȥ��Ca(OH)2����������Ƿ�ϴ���IJ�����������ȡ����ϴҺ�������μ�Na2CO3��Һ���������ְ�ɫ������˵���Ѿ�ϴ�����ʴ�Ϊ��ȡ����ϴҺ�������μ�Na2CO3��Һ���������ְ�ɫ������˵��ϴ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֪t ��ʱAgCl��KspΪ2��10-10������t ��ʱ,Ag2CrO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����(����)

A. t ��ʱ��Ag2CrO4��KspΪ1��10-9
B. �ڱ���Ag2CrO4��Һ�м���K2CrO4��ʹ��Һ��Y�㵽X��
C. t ��ʱ����ӦAg2CrO4(s)+2Cl-(aq) ![]() 2AgCl(s)+CrO42-(aq)��ƽ�ⳣ��K=2.5��107
2AgCl(s)+CrO42-(aq)��ƽ�ⳣ��K=2.5��107
D. t ��ʱ����0.01 mol��L-1 AgNO3��Һ�ζ�20 mL 0.01 mol��L-1 KCl��0.01 mol��L-1��K2CrO4�Ļ����Һ��CrO42-�ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ����ȡ���������ռ��������
ѡ�� | ���� | �� | �� | �� |
|
A | NH3 | Ũ��ˮ | ��ʯ�� | Ũ���� | |
B | SO2 | Ũ���� | Na2SO3 | Ũ���� | |
C | NO2 | Ũ���� | ͭм | H2O | |
D | Cl2 | Ũ���� | MnO2 | H2O |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���߿��е�װ�ÿ���������Ũ������ľ̿�۵ļ��������·�Ӧ������������������д���пհף�

��1�����װװ���Т١��ڡ�������������������˳���Ϊ�ڡ��١��ۣ�����Լ����������____________�����ܼ����������____________��
��2�����������������˳���Ϊ�١��ۡ��ڣ�����Լ����������____________�����ܼ����������____________��
��3�����������������˳���Ϊ�ڡ��ۡ��٣�����Լ����������____________�����ܼ����������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ijͬѧ����ˮ�ʼ��վ����480mL0.5mol��L-1NaOH��Һ�Ա�ʹ�á�
��1���������������ͼ��ʾ�����ͼ����Ӧ����ͼ�е�______֮�䡣
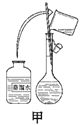
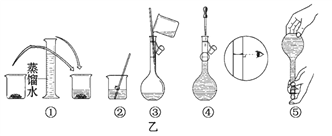
A.�����ۡ������� B.�����ڡ������� C.������
��2����ͬѧӦ��ȡNaOH����________g��������Ϊ23.1 g���ձ�����������ƽ�ϳ�ȡ����NaOH����ʱ����������ͼ��ѡ������ȷ��ʾ����λ�õ�ѡ��________(����ĸ)��
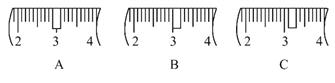
������������A��B��C���ֳ��û�ѧ��������ش������й����⣺
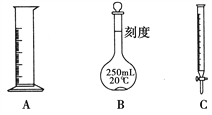
��1�����ֻ�ѧ�����б�����0���̶ȵ�Ϊ________(������)��
��2�����ֻ�ѧ������ʹ��ʱ������Ҫ�����Ƿ�©Һ��Ϊ________(����ĸ����)��
��3�������ֻ�ѧ�����е�һ�ֶ�Һ��������м�������ȷ�Ķ���Ϊn mL�����Ӷ���Ϊx mL�����Ӷ���Ϊy mL����y>n>x��������������________(������)��
������ѧ����С�����������ͼ��ʾ��һ�����巢�����ռ���β������װ�ã���̽����װ�õĶ���ԡ�
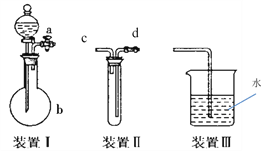
��1��ʵ��ǰҪ����װ�����������ԣ�д����������____________��
��2������װ������ֱ���ռ�CO2��������Ϊ_____________��
��3����������װ�ÿ����ʵ������ȡNH3������װ���� ����NH3ʱ�ᷢ������������ˮ���ټ���һ��Һ��ɷ�ֹ�����ķ�������Һ��Ϊ________���ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦFe��s��+CO2��g��![]() FeO��s��+CO��g����ƽ�ⳣ��ΪK1����ӦFe��s��+H2O��g��
FeO��s��+CO��g����ƽ�ⳣ��ΪK1����ӦFe��s��+H2O��g��![]() FeO��s��+H2��g����ƽ�ⳣ��ΪK2���ڲ�ͬ�¶�ʱK1��K2��ֵ���±���
FeO��s��+H2��g����ƽ�ⳣ��ΪK2���ڲ�ͬ�¶�ʱK1��K2��ֵ���±���
�¶ȣ������¶ȣ� | K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
��1�������¶�Ϊ973Kʱ����ӦCO2��g��+H2��g��![]() CO��g��+H2O��g�� K=__________��
CO��g��+H2O��g�� K=__________��
��2��Ŀǰ��ҵ����һ�ַ�������CO2�������״���CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)�� �����Ϊ1 L�ĺ����ܱ������У�����1 mol CO2��3 mol H2���з�Ӧ��
CH3OH(g)��H2O(g)�� �����Ϊ1 L�ĺ����ܱ������У�����1 mol CO2��3 mol H2���з�Ӧ��
�ٸ÷�Ӧ�ܹ��Է����е�ԭ����___________________________��
�����д�ʩ����ʹc(CH3OH)�������________��
a�������¶� b������He(g)��ʹ��ϵѹǿ����
c����H2O(g)����ϵ�з������ d���ٳ���1 mol CO2��3 mol H2
�����¶�T1ʱ������Ӧ�ﵽƽ��ʱ�����n(H2)��2.4 mol�������������䣬���¶�T2ʱ������Ӧ�ﵽƽ��ʱ�����n(CO2)��0.82 mol����T2________T1(������������������������)��
��3��ijʵ�齫һ������CO2��H2����һ��������ܱ������У������ֲ�ͬ�����·�����Ӧ��CO2(g) ��3H2(g) ![]() CH3OH(g)��H2O(g) ��H����49.0 kJ��mol��1�����CH3OH�����ʵ�����ʱ��仯����ͼ��ʾ���ش����⣺
CH3OH(g)��H2O(g) ��H����49.0 kJ��mol��1�����CH3OH�����ʵ�����ʱ��仯����ͼ��ʾ���ش����⣺

������I������Ӧ��ƽ�ⳣ����С��ϵΪK��________K��(������������������������)��
��һ���¶��£����ݻ���ͬ�ҹ̶��������ܱ������У������·�ʽͶ�뷴Ӧ�һ��ʱ���ﵽƽ�⡣
���� | �� | �� |
��Ӧ�� Ͷ���� | 1 mol CO2��3 mol H2 | a mol CO2��b mol H2�� c mol CH3OH(g)��c mol H2O(g) |
������ƽ��������ѹǿΪ��ʼʱ��0.8����Ҫʹƽ������������ͬ��ֵ�Ũ����ȣ�����ʼʱά�ַ�Ӧ������У���c��ȡֵ��ΧΪ________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������̿�MnCO3���ۺ�FeCO3��SiO2��Cu2(OH)2CO3�����ʣ�Ϊԭ����ȡ�������̣�������ʾ��ͼ���£�

��֪�������������������pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
�ش��������⣺
��1�������ܽ�MnCO3�Ļ�ѧ������______________������1����Ҫ�ɷ�Ϊ________________��
��2������Һ1�м���˫��ˮʱ����Ӧ�����ӷ���ʽ��___________________��
��3����Һ2�м����Թ��������ܵ����MnS���Գ�ȥCu2+����Ӧ�����ӷ���ʽ��__________________����CuS��MnS���������Һ�У�c(Cu2+)/c(Mn2+)=_____________ ��Ksp(CuS)=1.2��10-36��Ksp(MnS)=2.5��10-13����
��4�������������£�NaClO3��Һ��MnCl2����ΪMnO2���仹ԭ����ΪCl2���÷�Ӧ�����ӷ���ʽΪ ___________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ�ClO2������ɫ������ˮ�����壩�Ǹ�Ч���Ͷ��������������������}��
(1)��ҵ�Ͽ���KC1O3��Na2SO3��H2SO4�������Ƶ�ClO2�÷�Ӧ�������뻹ԭ�����ʵ���֮��Ϊ_______________��
(2)ʵ������NH4Cl�����ᡢNaClO2(�������ƣ�Ϊԭ�ϣ�ͨ�����¹����Ʊ�ClO2��
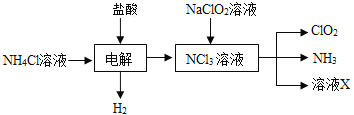
ͼ1 ͼ2
�ٵ��ʱ������Ӧ�Ļ�ѧ����ʽΪ_______________________________________________ ��
����ҺX�д������ڵ���������________________________________________________ ��
�۳�ȥClO2�е�NH3��ѡ�õ��Լ��� ___________________(����)��
a��ˮ b����ʯ�� c��Ũ���� d������ʳ��ˮ
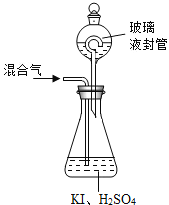
(3)����ͼ2װ�ÿ��Բⶨ�������ClO2�ĺ�����
������ƿ�м��������ĵ⻯�أ���50 mLˮ�ܽ���ټ��� 3 mL ϡ���
���ڲ���Һ��װ���м���ˮ.ʹҺ��û������Һ��ܵĹܿڣ�
��һ�����Ļ������ͨ����ƿ�����գ�
����������Һ��װ���е�ˮ������ƿ�У�
������0.1000 mol��L-1��������Ʊ���Һ�ζ���ƿ�е���Һ��I2+2S2O32����2I��+S4O62��)��ָʾ����ʾ�յ�ʱ����ȥ20.00 mL�����������Һ���ڴ˹����У�
����ƿ��ClO2��⻯�ط�Ӧ�����ӷ���ʽΪ_______________________________��
�ڲ���Һ��װ�õ�������________________________________________________��
��V�м����ָʾ��ͨ��Ϊ___________���ζ����յ��������_________________________��
�ܲ�û������ClO2������Ϊ____________________________ g.��
(4)O2������������ˮ�Ậ��һ������������Ρ���Ҫ��ȥ������������Σ��������������˵���________(����)��
a������ b���⻯�� c������ d����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ10.1gij±����������NaOH��Һ��ϣ���ַ�Ӧ��������AgNO3-HNO3�����Һ,����18.8gdz��ɫ���������±����������
A. CH3Br B. CH3CH2Br C. CH2BrCH2Br D. CH3CHBrCH2Br
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com