
【题目】铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
A.降低温度
B.加入适量的水
C.加入少量CuSO4溶液
D.加入浓度较大的盐酸
科目:高中化学 来源: 题型:
【题目】已知某温度下,反应2SO2+O22SO3 , 的平衡常数K=19,在该温度下的体积固定的密闭容器中充入C(SO2)=1molL﹣1 , C(O2)=1 molL﹣1 , 当反应在该温度下SO2 , 为80%时,该反应(填“是”或“否”)达到化学平衡状态,若未达到,向(填“正反应”或“逆反应”)方向进行.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关2个电化学装置的叙述正确的是( ) 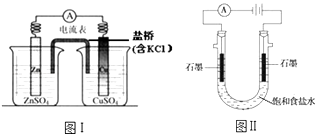
A.图Ⅰ,电流形成的完整过程是:负极Zn﹣2e﹣═Zn2+ , 电子经导线流向正极,正极Cu2++2e﹣═Cu
B.图Ⅰ,在不改变总反应的前提下,可用Na2SO4替换ZnSO4 , 用石墨替换Cu棒
C.图Ⅱ,通电后H+和Na+先从阳极区移动到阴极,然后阴极才发生反应2H++2e﹣═H2↑
D.图Ⅱ,通电后,由于OH﹣向阳极迁移,导致阳极附近pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为:![]() KClO3+
KClO3+![]() HCl(浓)―→
HCl(浓)―→![]() KCl+
KCl+![]() ClO2↑+
ClO2↑+![]() Cl2↑+
Cl2↑+![]() H2O
H2O
(1)请配平该化学方程式(未知系数填入框内)_____。
(2)浓盐酸在反应中显示出来的性质是________(填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)5 ℃ 下将产物氯气0.1 mol溶于水配成1 L溶液,已知该溶液中氢氧根离子浓度最小,请将溶液中的其他成分按照其物质的量浓度从大到小顺序排列____________________(填分子或离子化学式,少写及顺序错误不得分)。
(4)若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应:
①SO2+H2O=H2SO3 ②C+H2O=H2+CO
③2Al+6H+=2Al3++3H2↑ ④2Mg+CO2![]() 2MgO+C
2MgO+C
⑤2Na2O2+2H2O=4NaOH+O2↑ ⑥Ca2C2+2H20=Ca(OH)2+C2H2↑
(1)上述反应中不属于氧化还原反应的有_________(填各反应的序号,下同);反应物中H2O被还原的是_______;还原产物为单质的是_______。
(2)上述各反应所涉及到的物质中,属于弱电解质的是______(填化学式)。
(3)用单线桥表示反应④中电子转移的方向和数目___________________。
(4)高铁酸钾(K2FeO4)溶液呈紫红色,向其中加入过量亚硝酸钠,溶液紫红色逐渐褪去,出现红褐色沉淀,溶液的pH逐渐增大。请写出该反应的离子方程式__________________。
(5)下列两组混合物,括号内为杂质,填写除去杂质所需电解质溶液(限定只能用含有钠元素的试剂,假设用量可控),并写出反应的离子方程式。
①Fe2O3(SiO2) 试剂________,________________________________________。
②Na2CO3(NaAlO2) 试剂________,________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 澄清石灰水与过量碳酸氢钠溶液反应:HCO3-+ Ca2+ + OH-![]() CaCO3↓+H2O
CaCO3↓+H2O
B. 工业上氯气和石灰乳反应制漂白粉:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
C. 向硫酸氢钠溶液中滴加氢氧化钡溶液至SO42-沉淀完全:Ba2++2OH-+2H++SO42-![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 硫酸氢钠溶液与小苏打溶液的反应:H++HCO3-![]() H2O+CO2↑
H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,铁是使用最广泛的金属之一,已知在高温下,Fe与水蒸气可发生反应.应用如图装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”. 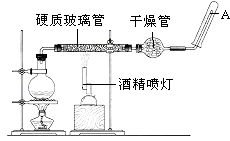
请回答下列的问题.
(1)铁在周期表中的位置是 .
(2)请写出该反应的化学方程式: .
(3)曾利用铝和铁的氧化物反应原理来焊接钢轨,该反应的化学方程式为 .
(4)现有铁和铂组成的合金共a mol,其中Pt的物质的量分数为x,研成粉末状后全部投入含b mol HNO3的稀溶液中,使其充分反应,且HNO3的还原产物只有NO.试回答下列问题: ①随HNO3用量的增加,溶液中的金属离子和残留固体的成分依次有四种情况,请用粒子符号填写下表空白:
① | ② | ③ | ④ | |
溶液中的金属离子 | Fe2+ | |||
残留固体成分 | Fe、Pt | Pt | Pt |
②当x=0.5,且溶液中Fe3+与Fe2+和物质的量相等,在标准状况下共产生112mL NO.则a= , b= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于C12的说法正确的是
A. C12的密度比空气小,可以用向下排空气法收集 B. C12能使湿润的红色布条褪色
C. Cu在C12中燃烧,生成物为CuCl D. 实验室可用加热分解KC1O3的方法制取C12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com