
【题目】1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯反应温度为115~125℃,反应装置如下图。下列对该实验的描述错误的是( )
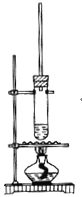
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
【答案】C
【解析】
A.实验室制取乙酸丁酯,反应需要的反应温度为115~125℃,而水浴加热适合温度低于100℃的反应,故该反应不能用水浴加热,A正确;
B.乙酸和丁醇易挥发,当有易挥发的液体反应物时,为了避免反应物损耗和充分利用原料,可通过在发生装置安装长玻璃管或冷凝回流管等实现,B正确;
C.酯化反应为可逆反应,反应物不能完全转化为生成物,因此制取的乙酸丁酯中含有挥发的未反应的乙酸及丁醇,提纯乙酸丁酯需使用碳酸钠溶液,来吸收未反应的乙酸及溶解丁醇,同时又可降低乙酸丁酯的溶解度便于分离出乙酸丁酯,如果用氢氧化钠,会使乙酸丁酯水解,C错误;
D.酯化反应为可逆反应,在其他条件不变时,增加反应物乙酸的量,可使平衡向生成酯的方向移动,从而提高1-丁醇的转化率,D正确;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】钴、铜及其化合物在工业上有重要用途,回答下列问题:
(1) 请补充完基态Co的简化电子排布式:[Ar]______, Co2+有________个未成对电子。
(2)Na3[Co(NO2)6]常用作检验K+的试剂, 配位体![]() 的中心原子的杂化形式为______, 空间构型为______。大π键可用符号
的中心原子的杂化形式为______, 空间构型为______。大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为![]() ,则
,则![]() 中大π键应表示为________。
中大π键应表示为________。
(3)配合物[Cu(En)2]SO4的名称是硫酸二乙二胺合铜(Ⅱ), 是铜的一种重要化合物。其中 En 是乙二胺(H2NCH2CH2NH2)的简写。
①该配合物[Cu(En)2]SO4中N、 O、 Cu的第一电离能由小到大的顺序是__________。
②乙二胺和三甲胺[N(CH3)3]均属于胺, 且相对分子质量相近, 但乙二胺比三甲胺的沸点高得多, 原因是___________
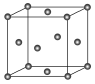
(4) 金属Cu晶体中的原子堆积方式如图所示, 其配位数为________,铜原子的半径为a nm, 阿伏加德罗常数的值为NA, Cu的密度为________ g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质](15分)
锌是人体必需的微量元素之一,起着极其重要的作用,回答下列问题:
(1)请写出Zn2+的核外电子排布式_____________________。
(2)ZnCl2熔点为275 ℃,而CaCl2的熔点为782 ℃,请分析熔点不同的原因:_________。
(3)Zn2+能与多种微粒形成配合物,如Zn2+与CNO可形成[Zn(CNO)4]2,[Zn(CNO)4]2中配位原子为__________,[Zn(CNO)4]2的组成中非金属元素的电负性大小顺序为____________;Zn2+与CN可形成[Zn(CN)4]2,[Zn(CN)4]2中σ键、π键和配位键的个数比为________;配合物Zn(NH3)4CO3中阴离子的空间构型为____________,N原子的杂化方式为____________。
(4)Zn与S所形成化合物的晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图:
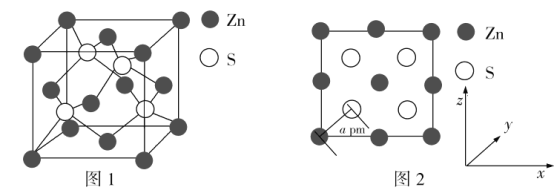
①晶胞中S原子的配位数为_________。
②晶胞中最近的两个S原子之间的距离为_______pm。
③设阿伏加德罗常数的值为NA,则该晶胞的密度是__________g·cm3(列出计算表达式)。
[化学——选修5:有机化学基础](15分)
哌替啶盐酸盐G有镇痛作用,其合成路线如下。回答下列问题:
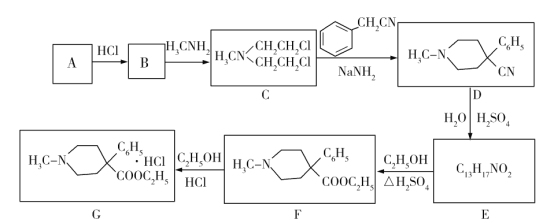
(1)写出A的结构简式:________;B中含有碳碳双键,则B的名称为_____________。
(2)G中含氧官能团名称为____________;B→C的反应类型为_________________。
(3)E的结构简式为_____________。
(4)写出C→D的化学方程式:_______________________________________。
(5)M与E互为同分异构体,符合下列条件的M有______种。
①属于芳香α-氨基酸;
②含有两个六元环。
其中一种同分异构体,—NH2被H原子取代后,除苯基上H原子外,其他核磁共振氢谱的峰面积比为4∶4∶1∶1∶1,该同分异构体的结构简式为______________。
(6)请结合以上合成路线,写出以H3CNHCH2Cl和CH2=CHCl及上述流程中出现的物质为原料合成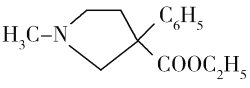 的路线______________________。
的路线______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是一种重要的化工原料,可由乙烷为原料制取,回答下列问题。
(1)传统的热裂解法和现代的氧化裂解法的热化学方程式如下:
①C2H6(g)=C2H4(g)+H2(g) ΔH1=+136kJ·mol-1
②C2H6(g)+![]() O2(g)=C2H4(g)+H2O(g) ΔH2=-110kJ·mol-1
O2(g)=C2H4(g)+H2O(g) ΔH2=-110kJ·mol-1
已知反应相关的部分化学键键能数据如下:
化学键 | H-H(g) | H-O(g) | O=O |
键能(kJ·mol-1) | 436 | x | 496 |
由此计算x=___,通过比较ΔH1和ΔH2,说明和热裂解法相比,氧化裂解法的优点是___(任写一点)。
(2)乙烷的氧化裂解反应产物中除了C2H4外,还存在CH4、CO、CO2等副产物(副反应均为放热反应),图甲为温度对乙烷氧化裂解反应性能的影响。乙烷的转化率随温度的升高而升高的原因是___,反应的最佳温度为___(填序号)。
A.700℃ B.750℃ C.850℃ D.900℃

[乙烯选择性=![]() ;乙烯收率=乙烷转化率×乙烯选择性]
;乙烯收率=乙烷转化率×乙烯选择性]
(3)烃类氧化反应中,氧气含量低会导致反应产生积炭堵塞反应管。图乙为![]() 的值对乙烷氧化裂解反应性能的影响。判断乙烷氧化裂解过程中
的值对乙烷氧化裂解反应性能的影响。判断乙烷氧化裂解过程中![]() 的最佳值是___,判断的理由是___。
的最佳值是___,判断的理由是___。
(4)工业上,保持体系总压恒定为100kPa的条件下进行该反应,通常在乙烷和氧气的混合气体中掺混惰性气体(惰性气体的体积分数为70%),掺混惰性气体的目的是___。反应达平衡时,各组分的体积分数如下表:
组分 | C2H6 | O2 | C2H4 | H2O | 其他物质 |
体积分数/% | 2.4 | 1.0 | 12 | 15 | 69.6 |
计算该温度下的平衡常数:Kp=___(用平衡分压代替平衡浓度,平衡分压=总压×体积分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学对提高人类生活质量和促进社会发展具有重要作用。下列说法正确的是( )
A.某些金属元素的焰色反应、海水提溴、煤的气化、石油的裂化都是化学变化的过程
B.氮氧化物的大量排放,会导致光化学烟雾、酸雨和温室效应等环境问题
C.油脂的主要成分是高级脂肪酸甘油酯,长时间放置的油脂会因水解而变质
D.白葡萄酒含维生素C等多种维生素,通常添加微量![]() 的目的是防止营养成分被氧化
的目的是防止营养成分被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃是由C、H元素组成的有机物、不同有机物的结构不同。试回答下列问题:
(1)分子式为C6H12的某烯烃的所有的碳原子都在同一个平面上,则该烯烃的结构式___,系统命名为___。
(2)组成符合CnH2n-2的某种烃,分子结构中没有支链或侧链,它完全燃烧时所消耗的氧气的体积是相同状态下该烃蒸气体积的8.5倍。
(a)若该烃为链状烯烃,并且与等物质的量的Br2加成只能得到某单一产物,则该烃的结构简式为___。
(b)若该烃只能与含等物质的量的Br2四氯化碳溶液发生反应,则其结构简式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到相应实验目的的是
选项 | 实验操作 | 实验目的 |
A | 室温下,用pH试纸分别测定浓度均为0.1mol/L HClO溶液和CH3COOH溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向10mL浓度均为0.1mol/L的BaCl2和CaCl2混合溶液中加入10mL 0.1mol/L Na2SO4溶液,出现白色沉淀 | 证明Ksp(BaSO4)<Ksp(CaSO4) |
C | 向含有酚酞试液的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
D | 室温下,等体积、pH=2的HA和HB两种酸分别与足量Zn反应,HB放出的H2多 | 证明HB是强酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1 L 0.1 mol/L的AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断不正确的是
A.电解质AgNO3溶液的浓度仍为0.l mol/LB.阳极上产生112 mL O2(标况)
C.转移1.204×1022个电子D.反应中有0.02 mol的Ag被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com