
| �ŵ� |
| ��� |
| ����� | ���볣����mol?L-1�� |
| H3PO4 | Ka1=7.1��10-3��Ka2=6.2��10-8��Ka3=4.5��10-13 |
| HF | Ka=6.4��10-4 |
| CH3COOH | Ka=1.7��10-5 |
| NH3?H2O | Kb=1.7��10-5 |
| c(H+)?c(F-) |
| c(HF) |
| �ŵ� |
| ��� |
| c(H+)?c(F-) |
| c(HF) |
| 2 | Ka?c(HF) |


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��I2�ڷ�Ӧ�����ǻ�ԭ����ڷ�Ӧ�������������� |
| B��NaHSO4��������Ӧ�о����������� |
| C��������Ӧ�����ɵ�����I2ʱת�Ƶĵ�������� |
| D��NaI��NaIO3��һ���������ܷ�Ӧ����I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ȼ |
| ����˵�� | ����֤����ѧ����ʽ�� |
| ��1���ֽⷴӦһ���е������� | |
| ��2���е��ʺͻ��������ɵķ�Ӧ�����û���Ӧ | |
| ��3���û���Ӧһ���н������ʲμ� | |
| ��4��ԭ�����ڻ�ѧ��Ӧǰ��һ���������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K��HF��=7.2��10-4 |
| B��K��HNO2��=4.9��10-10 |
| C������������Ӧ���ɵó����� |
| D��Ka��HCN����Ka��HNO2 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
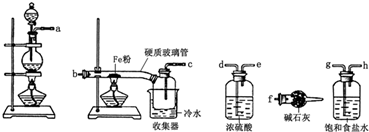
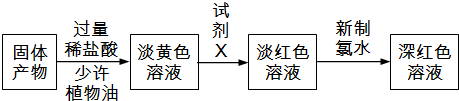
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������Cu��H2 |
| B������������11.2L��O2 |
| C������������Һ��PHֵ���ϼ�С |
| D���������е���ת����Ŀ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��FeO |
| B��Fe3O4 |
| C��Fe2O3 |
| D��FeO2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com