
【题目】在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为![]() ,溶质的质量分数为ω,溶质的物质的量浓度为C mol/L。下列叙述中正确的有( )
,溶质的质量分数为ω,溶质的物质的量浓度为C mol/L。下列叙述中正确的有( )
①![]() ②
②![]() ③上述溶液中加入V mL水后,所得溶液的质量分数大于0.5ω ④上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
③上述溶液中加入V mL水后,所得溶液的质量分数大于0.5ω ④上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
A. ②③ B. ②④ C. ③④ D. ①③
【答案】B
【解析】①氨气溶于水,主要以NH3H2O存在,但仍然以NH3作为溶质,ω=![]() ×100%=
×100%=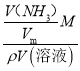 =
=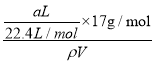 ×100%=
×100%=![]() ×100%,选项①错误;②、C=
×100%,选项①错误;②、C=![]() =
=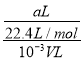 =
=![]() mol/L,选项②正确;③水的密度比氨水的密度大,所以上述溶液中再加入VmL水后,混合后溶液的质量大于2倍的原氨水的质量,溶质氨气的质量不变,所以所得溶液的质量分数小于0.5ω,选项③错误;④上述溶液中再加入1.5VmL同浓度稀盐酸,溶液为氯化铵与氯化氢的混合溶液,浓度之比为2:1,溶液呈酸性,c(H+)>c(OH-),铵根离子水解,水解程度微弱,所以c(Cl-)>c(NH4+),充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),选项④正确;答案选B。
mol/L,选项②正确;③水的密度比氨水的密度大,所以上述溶液中再加入VmL水后,混合后溶液的质量大于2倍的原氨水的质量,溶质氨气的质量不变,所以所得溶液的质量分数小于0.5ω,选项③错误;④上述溶液中再加入1.5VmL同浓度稀盐酸,溶液为氯化铵与氯化氢的混合溶液,浓度之比为2:1,溶液呈酸性,c(H+)>c(OH-),铵根离子水解,水解程度微弱,所以c(Cl-)>c(NH4+),充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),选项④正确;答案选B。


科目:高中化学 来源: 题型:
【题目】某同学利用“多米诺骨牌”效应,设计了如图气体制取与性质验证的组合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.请看图回答问题: 
(1)A中反应的化学方程式;B中白磷不燃烧,原因是
(2)D中看到的现象是 .
(3)用化学方程式表示E中颜色变化的原因;用F装置收集气体的依据是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,已知:①NaOH溶液、②NH4Cl溶液、③NaCl溶液、④Na2CO3溶液,相同物质的量浓度的上述溶液按pH减小排序正确的是( )
A. ④③②① B. ①④③② C. ①②④③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,若关闭活塞,则品红溶液无变化,石蕊试液变红,澄清石灰水变浑浊;若打开活塞,则品红溶液褪色,石蕊试液变红,澄清石灰水变浑浊。据此判断气体和广口瓶中盛放的物质分别是( )

A. CO2和Na2CO3溶液 B. Cl2和NaHCO3溶液
C. SO2和浓H2SO4 D. SO2和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨水中存在电离平衡:NH3H2O![]() NH4++OH-,下列情况能引起电离平衡向右移动的是( )
NH4++OH-,下列情况能引起电离平衡向右移动的是( )
①加NH4Cl 固体②加NaOH溶液③加盐酸④加CH3COOH溶液⑤加水⑥加压
A. ①②⑤ B. ②③④ C. ③④⑤ D. ④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质与应用对应关系正确的是 ( )
A. 晶体硅熔点高、硬度大,可用于制作半导体材料
B. 氢氧化铝具有弱碱性,可用于制胃酸中和剂
C. 漂白粉在空气中不稳定,可用于漂白纸张
D. 氧化铁能与酸反应,可用于制作红色涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属元素锡(Sn)和碳元素位于同一主族,主要化合价为+2和+4。某同学通过下列方法测定金属锡样品的纯度:(假定杂质不参加反应)
(1)将试样溶于盐酸中,反应的化学方程式为:______________________。
(2)加入过量的FeCl3溶液,反应的化学方程式为:______________________。
(3)用已知浓度的K2Cr2O7酸性溶液滴定生成的Fe2+.反应的离子方程式为:______________
(4)现有金属锡样品1.142g,经上述各步反应后,共用去0.100mol/L的K2Cr2O7溶液16.00ml. 则试样中锡的质量分数_____________________。
(5)步骤(4)中如果取用16.00ml的K2Cr2O7溶液则应用____________(填仪器名称)。该同学在配制0.100mol/L 的K2Cr2O7溶液的试验中,若其他步骤都正确,但定容时俯视刻度线则所得溶液的浓度____________(填偏高,偏低,或无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是:
A. 在空气中燃烧 B. 通入足量溴水中
C. 通入酸性高锰酸钾溶液中 D. 通入水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com