
【题目】下列关于物质性质变化的比较中,正确的是( )
A.酸性强弱HIO4<HBrO4<HClO4
B.原子半径大小S>Na>O
C.碱性强弱KOH<NaOH<LiOH
D.金属性强弱Na<Mg<Al
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加,m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol/Lr溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
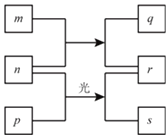
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一种阴、阳离子双隔膜三室电解槽处理废水中的NH![]() ,模拟装置如图所示。下列说法正确的是( )
,模拟装置如图所示。下列说法正确的是( )
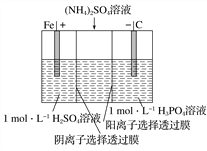
A. 阳极室溶液由无色变成棕黄色 B. 阴极的电极反应式为4OH--4e-===2H2O+O2↑
C. 电解一段时间后,阴极室溶液中的pH升高 D. 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol·L-1、体积均为V0的MOH与ROH溶液,分别加水稀释至体积V,pH随lg(V/ V0)的变化如图所示,下列叙述错误的是( )
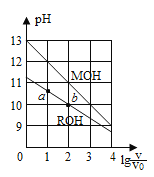
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当lg(V/ V0))=2时,若两溶液同时升高温度,则c(M+)/c(R+)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.含有共价键的化合物一定是共价化合物
B.Na2O2中既含有离子键又含有非极性共价键
C.KOH中只含有共价键
D.KI和HI中化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图,根据图示判断下列说法正确的是( )
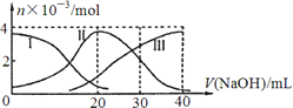
A.H2A在水中的电离方程式是:H2A=H++HA-;HA-![]() H++A2-
H++A2-
B.当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D.当V(NaOH)=30mL时,则有:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
①31g白磷含有的P-P键数为N A
②1molCH3+(碳正离子)中含有电子数为10NA
③1mol铜与足量硫蒸气反应,转移电子数为2NA
④1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2N A 个电子
⑤用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过电子数为N A
⑥0.84gNaHCO3晶体中阳离子和阴离子总数为0.03N A
⑦3.9gNa2O2吸收足量的CO2时转移的电子数是0.05 N A
⑧标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1N A
⑨28g C16O与28g C18O中含有的质子数均为14×6.02×1023
⑩标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
A.②④⑦⑧ B.③④⑥⑦⑧ C.④⑦ D.④⑥⑨⑩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com