
【题目】已知:四甲基氢氧化铵[(CH3)4NOH ]是强碱,甲胺 (CH3NH2H2O)为弱碱。常温下,在体积均为20 mL、浓度均为0.1 mol/L的四甲基氢氧化铵溶液和甲胺溶液中,分别滴加浓度为0.1 mol/L的盐酸,溶液的导电率与盐酸体积的关系如图所示。下列说法正确的是

A. pH的相对大小: c>d
B. 在b、c、e三点中,水的电离程度最大的点是e
C. b 点溶液:c(H+)+c(CH3NH3+) = c(OH-)
D. c 点溶液:c(Cl-)>c(CH3NH3+) >c(H+) >c(OH-)
【答案】D
【解析】
A.当滴加20mL盐酸时,恰好完全反应,一个是强酸强碱盐溶液,溶液呈中性;一个是强酸弱碱盐溶液,溶液水解呈酸性,再比较pH大小;
B.酸碱会抑制水的电离,能水解的盐则会促进水的电离,据此分析;
C.该选项中的等式阴阳离子分别再等号两边,所以可以写出电荷守恒分析是否正确;
D.当滴加20mL盐酸时,溶质为强酸弱碱盐CH3NH3Cl,水解使溶液显酸性,且水解程度是很弱的,据此分析离子大小。
A.当滴加20mL盐酸时,恰好完全反应,四甲基氢氧化铵[(CH3)4NOH ]是强碱,此时溶液中溶质为强酸强碱盐,溶液呈中性;甲胺 (CH3NH2H2O)为弱碱,此时溶液中溶质为强酸弱碱盐,溶液呈酸性,pH相对大小:c<d,故A错误;
B.体积为20mL、浓度为0.1mol·L-1的甲胺溶液,滴加浓度为0.1mol·L-1的盐酸,当滴加20mL盐酸时,恰好完全反应,此时溶液中溶质为强酸弱碱盐,促进水电离,此时水电离程度最大,即b、c、e三点中c点水的电离程度最大,故B错误;
C.根据电荷守恒,b 点溶液:c(H+)+c(CH3NH3+) = c(OH-)+ c(Cl-),故C错误;
D.当滴加20mL盐酸时,恰好完全反应,此时溶液中溶质为强酸弱碱盐CH3NH3Cl,少量CH3NH3+水解使溶液显酸性,所以溶液中的离子浓度大小:c(Cl-)>c(CH3NH3+) >c(H+) >c(OH-),故D正确;
答案:D。


 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备Co2O3的工艺流程简图如下:
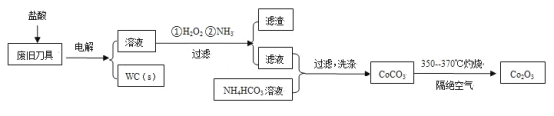
已知:在上述流程中,各种金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Co2+ |
开始沉淀的pH | 1.9 | 7.0 | 6.5 |
沉淀完全的pH | 3.2 | 9.0 | 9.4 |
回答下列问题:
(1)以废旧刀具作阳极,不锈钢作阴极,盐酸为电解质溶液。电解时阳极的电极反应有:Co-2e-=Co2+和______。
(2)通入氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择的pH的范围是_______。
(3)生成CoCO3的离子方程式是________。
(4)实验测得NH4HCO3溶液显碱性。制备CoCO3时,不能将滤液加入NH4HCO3溶液中,原因是_______。
(5)已知:Ksp(CoCO3)=1.4×10-13,Ksp(CoC2O4)=6.3×10-8。若仅从沉淀转化角度考虑,在0.01mol/L Na2C2O4溶液中加入CoCO3固体能否转化为CoC2O4沉淀?通过计算说明:_________。
(6)洗涤CoCO3不充分对最终产品纯度并无影响,但在焙烧时会造成环境污染,主要原因是____。
(7)CoCO3生成Co2O3的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从植物花汁中提取的一种有机物,可简化表示为HIn,在水溶液中因存在下列电离平衡,故可用做酸、碱指示剂:HIn(aq) (红色溶液)![]() H+(aq)+In-(aq) (黄色溶液),在上述溶液中加入下列物质,最终能使指示剂显黄色的是
H+(aq)+In-(aq) (黄色溶液),在上述溶液中加入下列物质,最终能使指示剂显黄色的是
A. HCl B. Na2O2 C. Na2CO3溶液 D. NaHSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某合作学习小组的同学验证文献上用乙烯气脱除氮氧化物。回答下列问题:
(1)甲组同学设计实验制取纯净的乙烯气体和NO。
①设计的制备C2H4装置如图所示:

资料:C2H5OH![]() CH2=CH2↑+H2O(主)
CH2=CH2↑+H2O(主)
C2H5OH+2H2SO4(浓)![]() 2C+2SO2↑+5H2O(副)
2C+2SO2↑+5H2O(副)
C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O(副)
CO2↑+2SO2↑+2H2O(副)
写出乙烯的电子式___________
装置B中盛放的试剂为___________(填小写字母)。
a KMnO4溶液 b Br2/CCl4溶液 c 浓NaOH溶液 d 浓硫酸
②设计图装置制备NO气体

装置D烧瓶中的实验现象为:___________;
装置E盛放的试剂是___________。
(2)乙组利用甲组制得的C2H4和NO并选用下列装置进行催化反应,并检验乙烯的氧化物CO和CO2(部分装置可重复使用,已知C2H4可被热的CuO氧化为碳的氧化物,酸性高锰酸钾可氧化NO和C2H4,不氧化CO)。

①各装置的连接顺序为:
![]() →K→G→___________→H→G→___________→M。(按顺序填一个或多个字母)
→K→G→___________→H→G→___________→M。(按顺序填一个或多个字母)
②K后接的G的作用是___________。
③酸性高锰酸钾溶液的作用是___________。
④证明乙烯的氧化产物中有CO的现象是___________;
若NO还原为N2,乙烯氧化为等物质的量的CO和CO2,则反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的表述正确的是
A. 当ΔH为“-”时,表示该反应为吸热反应
B. 已知C(s)+![]() O2(g)====CO(g)的反应热为110.5 kJ/ mol,说明碳的燃烧热为110.5 kJ / mol
O2(g)====CO(g)的反应热为110.5 kJ/ mol,说明碳的燃烧热为110.5 kJ / mol
C. 反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D. 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,放出的热量:CH3COOH<HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-
B. 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl-
C. pH=12的溶液:K+、Na+、CH3COO-、Br-
D. 25℃时,由水电离产生的c(H+)为 1![]() 10-9的溶液中:Mg2+、Cu2+、SO32-、NO3-
10-9的溶液中:Mg2+、Cu2+、SO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。可以判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。可以判断该分解反应已经达到化学平衡的是
A. 密闭容器中二氧化碳的体积分数不变 B. 密闭容器中气体的总物质的量改变
C. 密闭容器中混合气体的密度不变 D. 2v正(NH3)=v逆(CO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸吡酮洛芬(H)是一种消炎镇痛药,其合成路线如下:

已知R-CN![]() R-COOH
R-COOH
回答下列问题:
(1)A的化学名称是____。
(2)由B生成C的化学方程式为________。
(3)D的结构简式为_______。
(4)F中官能团的名称为_____。
(5)G生成H(试剂X的分子式为C6H8N2)的反应类型是____。
(6)E的分子式为____。X与E互为同分异构体,X的分子中含两个苯环,X水解后产物之一既能发生银镜反应又能与FeCl3溶液发生显色反应,X的核磁共振氢谱显示有6种不同化学环境的氢,峰面积之比为1:2:2:2:2:3。写出符合条件的X的结构简式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L1nol/L某一元酸HR溶液中滴加一元碱BOH溶液,混合溶液的![]() 与pH变化的关系如图所示.下列叙述正确的是
与pH变化的关系如图所示.下列叙述正确的是
A. M线表示![]() 随pH的变化B. BR溶液呈碱性
随pH的变化B. BR溶液呈碱性
C. 若温度升高,两条线均向上平移D. 常温下,0.1mol·L-1NaR溶液的pH=10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com