
【题目】A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空:
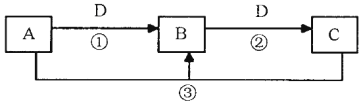
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则反应②的离子方程式为 ;实验室保存C的水溶液应加入 (填试剂名称)。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为 。
(3)若C是一种能形成硫酸型酸雨的污染性气体,D是一种能支持燃烧和呼吸的气体,则反应③中氧化产物和还原产物的质量比为 。
(4)若D是一种常见的温室气体,A、B、C的的焰色反应都呈黄色,则反应③的离子方程式为 。
【答案】(10分)(1)Fe+2Fe3+=3Fe2+(2分)铁粉和稀盐酸(2分)
(2)4NH3+5O2![]() 4NO+6H2O(2分)(3)1:2(2分)
4NO+6H2O(2分)(3)1:2(2分)
(4)HCO3-+OH-=CO32-+H2O(2分)
【解析】
试题解析: (1)根据题意:D为铁,A为氯气;氯化铁溶液和铁反应:Fe+2Fe3+=3Fe2+ 氯化亚铁溶液易被氧化,加入铁粉;抑制水解;加入稀盐酸;(2)根据题意:A为氨气,氨气和氧气反应生成一氧化氮和水;4NH3+ 5O2 =4NO +6H2O;(3)根据题意:C是二氧化硫,D是氧气,H2S+2O2==SO2+2H2O;氧化产物和还原产物的质量比为1:2; (4)A、B、C的的焰色反应都呈黄色,含有钠元素,D是一种常见的温室气体为二氧化碳;碳酸氢钠和氢氧化钠溶液反应:HCO3- + OH- =CO32- + H2O;
考点: 物质之间的转化关系;


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】2014年是门捷列夫诞辰180周年,下列事实不能用元素周期律解释的有( )
A.碱性:KOH>NaOH
B.溶解度:SO2>CO2
C.酸性:HClO4>H2SO4
D.气态氢化物的稳定性:H2O>NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义。
(1)下列措施中,有利于降低大气中的CO2、SO2、NO2浓度的有___________(填字母)。
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)为开发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料。写出由CO和H2生产甲醇的化学方程式________________________,
用该反应合成1 mol液态甲醇吸收热量131.9 kJ。又知2H2(g)+CO(g)+3/2O2(g)==CO2(g)+2H2O(g) ΔH=-594.1 kJ/mol。请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A. XX化妆品从纯天然植物中提取,不含任何化学物质
B. 红宝石、玛瑙、水晶、钻石等制作装饰品的材枓,其物质的主要成份都是硅酸盐
C. 氢氧燃料电池、硅太阳能电池中都利用了原电池原理
D. 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材科
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR。则在此反应中Y和M的质量之比为
A.16:9 B.23:9 C.32:9 D. 46:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类、脂肪和蛋白质的说法不正确的是( )
A. 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体
B. 葡萄糖可以发生氧化反应和银镜反应,说明葡萄糖具有还原性
C. 通过盐析从溶液中析出的蛋白质仍能溶解于水
D. 脂肪能发生皂化反应,生成甘油和高级脂肪酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一密闭容器中充入1mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发
生反应: H2(g)+I2(g)===2HI(g) ΔH<0。保持容器内气体压强不变,向其中加入1mol N2,反应 速率____________(填“变大”、“变小”或“不变”),平衡_____________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(2)在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)![]() zC(g),平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30 mol/L,则B的转化率___________,C的体积分数___________(填“变大”、“变小”或“不变”)。
zC(g),平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达到平衡时,测得A的浓度降低为0.30 mol/L,则B的转化率___________,C的体积分数___________(填“变大”、“变小”或“不变”)。
(3)已知反应2CO(g)+O2(g)===2CO2(g) ΔH= —566 kJ/mol,则CO的燃烧热为_____________。
(4)已知反应A(g)![]() B(g) + C(g),维持体系总压p恒定,在温度T时,物质的量为n 的气体A发生上述反应,达平衡时,A的转化率为
B(g) + C(g),维持体系总压p恒定,在温度T时,物质的量为n 的气体A发生上述反应,达平衡时,A的转化率为![]() ,则在该温度下反应的平衡常数表达式是Kp=____________。(用平衡分压代替平衡浓度计算,分压=总压
,则在该温度下反应的平衡常数表达式是Kp=____________。(用平衡分压代替平衡浓度计算,分压=总压![]() 物质的量分数,表达式化成最简形式)
物质的量分数,表达式化成最简形式)
(5)反应mA(g)+nB(g)![]() pC(g)达到平衡后,当减压后混合体系中C的百分含量增大。则加压后,C的浓度____________,(填“变大”、“变小”或“不变”);若C是有色物质,A、B是无色物质,减小压强,反应混合物的颜色_____________(填“变深”、“变浅”或“不变”)。
pC(g)达到平衡后,当减压后混合体系中C的百分含量增大。则加压后,C的浓度____________,(填“变大”、“变小”或“不变”);若C是有色物质,A、B是无色物质,减小压强,反应混合物的颜色_____________(填“变深”、“变浅”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com