
【题目】常温下,在下列各组指定溶液中一定不能大量共存的离子组的个数是( )
①强酸性溶液中:Mg2+、K+、![]() 、
、![]()
②强碱性溶液中:Na+、Ba2+、![]() 、
、![]()
③在无色溶液中:H+、K+、![]() 、F-
、F-
④0.1mol/LBa(NO3)2溶液:Mg2+、K+、![]() 、Cl-
、Cl-
⑤无色透明溶液中:![]() 、K+、Cl-、
、K+、Cl-、![]()
⑥无色透明的碱性溶液中:Na+、Ba2+、Cl-、![]()
A.一个B.两个C.三个D.四个
【答案】C
【解析】
①强酸性溶液中氢离子浓度大于氢氧根离子浓度:Mg2+、K+、SO42-、NO3-四种离子之间不反应,和氢离子之间也不反应,可以大量共存,故①不符合题意;
②强碱性溶液中氢氧根离子浓度大于氢离子浓度:Na+、Ba2+、HCO3-、NO3-中,HCO3-与OH-反应生成CO32-,不能大量共存,故②符合题意;
③在无色溶液中:H+、K+、SO42-、F-中,F-与H+生成氢氟酸,不能大量共存,故③符合题意;
④0.1mol/LBa(NO3)2溶液:Mg2+、K+、SO42-、Cl-中,Ba2+与SO42 –会生成硫酸钡沉淀,在溶液中不能大量共存,故④符合题意;
⑤无色透明溶液中:SO42-、K+、Cl-、NO3-离子间不发生反应,可以大量共存,故⑤不符合题意;
⑥无色透明的碱性溶液中:Na+、Ba2+、NO3-、Cl-离子间不发生化学反应,可以大量共存,故⑥不符合题意;
②③④符合题意,C可选;
答案选C。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
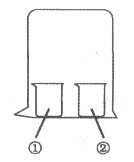
①中的物质 | ②中的物质 | 预测①的现象 | |
A | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | MgCl2溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是_____。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2—N2+HCl
①该反应中被氧化的元素是___(填元素名称),氧化剂是__(填化学式)。
②配平该方程式:____NH3+ ____Cl2—____N2+____HCl
③工业生产中常用喷洒氨水的方法来检查是否有Cl2泄漏,若Cl2有泄漏,可以观察到的现象是______,产生该现象的反应方程式为___。
(3)“地康法”制氯气的反应原理图示如下:
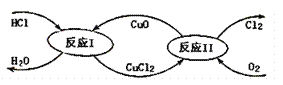
①反应I的化学方程式为____。
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】18.4g由铁、铜组成的混合粉末加入100mL5.0molL﹣1FeCl3溶液中,充分反应后,剩余固体质量为3.2g。下列说法正确的是( )
A.原固体混合物中:n(Cu):n(Fe)=2:1
B.反应后溶液中的溶质有FeCl2、FeCl3、CuCl2
C.反应后溶液中:n(Fe2+)+n(Cu2+)=0.8mol
D.剩余固体是铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料、防腐等工业,它不溶于H2SO4、HNO3和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],随着环境酸度的改变n随之改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

(1)写出溶解过程中产生无色气体的化学式:_______。
(2)还原过程中发生的主要反应的离子方程式:______。
(3)析出的CuCl晶体水洗后要立即用无水乙醇洗涤,在真空干燥机内于70℃ 干燥2h,冷却密封包装。70℃, 真空干燥、密封包装的原因是:______。
(4)滤液中主要成分是(NH4)2SO4,工业上用(NH4)2SO4与Al2(SO4)3制取铵明矾,铵明矾在食品,制革等方面有重要用途,写出铵明矾的化学式________。
(5)随着pH值减小[Cu2(OH)4-nCln]中Cu%_______。(填字母)
A.增大 B.不变 C.不能确定 D.减小
(6)如图是各反应物在最佳配比条件下,反应温度对CuCl产率影响。由图可知,溶液温度控制在60℃时,CuCl产率能达到94%,当温度高于65 时,CuCl产率会下降,从生成物的角度分析,其原因可能是______。
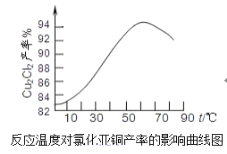
(7)以碳棒为电极电解CuCl2溶液也可得到CuCl,写出电解时阴极上发生的电极反应式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VL浓度为0.5mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是( )
A.通入标准状况下的HCl气体11.2VL
B.将溶液加热浓缩到0.5VL
C.加入10mol.L-1的盐酸0.1VL,再稀释至1.5VL
D.加入VL1.5mol.L-1的盐酸混合均匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。某化学研究小组利用氮气、氧化铝和活性炭在高温下制取氮化铝。 请回答下列问题:
(1)请写出制取氮化铝的化学方程式________。
制得的AlN样品仅含有Al2O3杂质,已知:AlN+NaOH+H2O=NaAlO2+NH3↑为测定AlN含量,设计如下三种实验方案。(测定过程均忽略NH3在强碱溶液中的溶解)
(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
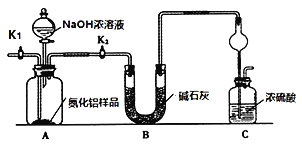
实验步骤:组装好实验装置,检查装置气密性并加入实验药品,关闭K1,打开K2 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。
(2)图中C装置中球形干燥管的作用是________。
(3)通入氮气的目的是_______。
(4)图中装置会导致测定结果_______(填“偏高”“偏低”或“无影响”)。
(方案2)用如图装置测定mg样品中AlN的纯度(部分夹持装置已略去)。
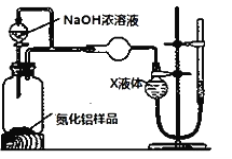
(5)为测定生成气体的体积,量气装置中的X液体可以是___(填字母)
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
(6)若mg样品完全反应,测得生成气体的体积为VmL(已转换为标准状况),则AlN的质量分数是______。若其他操作均正确,但反应结束后读数时,右侧量气管中液面高于左侧球型管中液面,则最后测得AlN的质量分数会_____(填“偏高”“偏低”或“无影响”)。
(方案3)按以下步骤测定样品中A1N的纯度:(过滤时使用无灰滤纸过滤)
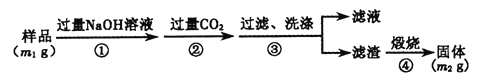
(7)步骤②生成沉淀的离子方程式为_______。
(8)样品中A1N的质量分数为_______(用含m1、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应H2(g)+I2(g)![]() 2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
A.H2(g)的消耗速率与HI(g)的生成速率之比为2:1
B.反应进行的净速率是正、逆反应速率之差
C.正、逆反应速率的比值是恒定的
D.压强不变时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习小组研究钠的燃烧反应产物,取金属钠(表面已被氧化),吸干煤油,置于坩埚内,上方倒扣盛满O2集气瓶,加热一段时间,充分反应后观察到产物为白色固体和淡黄色固体的混合物,测得反应前后各物质的质量如下表:
质量/g | ||
反应前 | 坩埚 | 100 |
盛有金属钠的坩埚 | 105.4 | |
反应后 | 盛有固体产物的坩埚 | 107.4 |
请回答下列问题:
(1)根据实验现象,推测固体产物成分为___________________(填化学式)
(2)将产物全部溶于水,观察到有气泡生成,写出该反应的化学方程式为________。
(3)测得上述溶液中n(Na+)=0.2mol,通过计算证实加热过程中存在表面的Na2O转化为Na2O2。___________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com