
【题目】已知![]() 时下列物质的溶度积
时下列物质的溶度积![]() 单位略
单位略![]() 。
。
| AgCl |
|
| |
|
|
|
|
|
下列说法正确的是![]()
A.等体积、浓度均为![]() 的
的![]() 和
和![]() 溶液混合能产生沉淀
溶液混合能产生沉淀
B.向含有浓度均为![]() 的
的![]() 和
和![]() 的溶液中慢慢滴入
的溶液中慢慢滴入![]() 溶液时,
溶液时,![]() 先沉淀
先沉淀
C.在![]() 悬浊液中加入盐酸时发生反应的离子方程式为
悬浊液中加入盐酸时发生反应的离子方程式为![]()
D.![]() 时,上述四种饱和溶液的物质的量浓度:
时,上述四种饱和溶液的物质的量浓度: ![]()
【答案】C
【解析】
A.浓度熵QC=c(CH3COO-)×c(Ag+)=0.01×0.01=1×10-4,Ksp=2.3 ×10-3,QC< Ksp ,所以溶液混合不能产生沉淀,故A错误;
B. AgCl饱和所需Ag+浓度=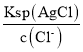 =
=![]() =1.77×10-8,所以Ag+浓度=
=1.77×10-8,所以Ag+浓度= =
=![]() =1.1×10-5,则1.77×10-8<1.1×10-5,所以氯离子先沉淀,故B错误;
=1.1×10-5,则1.77×10-8<1.1×10-5,所以氯离子先沉淀,故B错误;
C.![]() ,向
,向![]() 悬浊液中加入盐酸时
悬浊液中加入盐酸时![]() 转化为AgCl,离子方程式为
转化为AgCl,离子方程式为![]() ,故C正确;
,故C正确;
D.因为CH3COOAg饱和溶液中Ag+的浓度为![]() mol/L=4.8 ×10-2mol/L,因为AgCl 饱和溶液中Ag+的浓度为
mol/L=4.8 ×10-2mol/L,因为AgCl 饱和溶液中Ag+的浓度为![]() mol/L=1.33×10-5 mol/L ,c(AgCl)= 1.33×10-5 mol/L,假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4) =x2×0.5x=1.12×10-12,即x=
mol/L=1.33×10-5 mol/L ,c(AgCl)= 1.33×10-5 mol/L,假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4) =x2×0.5x=1.12×10-12,即x=![]() =1.3×10-4mol/L,c( Ag2CrO4) =0.65×10-4mol/L。假设Ag2S饱和溶液中Ag+的浓度为x,则S2-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2S) = x2×0.5x =6.7×10-15 ,即x=2.38×10-5 mol/L,c(Ag2S) =1.19×10-5mol/L ,则顺序为:c(CH3COOAg)>c( Ag2CrO4)>c(AgCl) >c(Ag2S),故D错误;
=1.3×10-4mol/L,c( Ag2CrO4) =0.65×10-4mol/L。假设Ag2S饱和溶液中Ag+的浓度为x,则S2-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2S) = x2×0.5x =6.7×10-15 ,即x=2.38×10-5 mol/L,c(Ag2S) =1.19×10-5mol/L ,则顺序为:c(CH3COOAg)>c( Ag2CrO4)>c(AgCl) >c(Ag2S),故D错误;
故选:C。


科目:高中化学 来源: 题型:
【题目】肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(ClO3-在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(Cr2O72-被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________。
②实验中加热煮沸的目的是___________。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中正确的是
A. 相同浓度的三种溶液:①(NH4)2CO3溶液、②NH4HCO3溶液、③NH4NO3溶液中 c(NH4+):③>①>②
B. 相同pH的溶液:①NaClO溶液、②NaHCO3溶液、③CH3COONa溶液中 c(Na+):③>②>①
C. 同浓度、同体积的溶液:①CH3COONa溶液、②NH4Cl溶液、③NaNO3溶液中 pH:②>③>①
D. 相同浓度的溶液:①氨水、②NaOH溶液、③Ba(OH)2溶液 c(H+):②>①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计一个电池(如下图所示),探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

(1)通入氢气的电极为________ (填正极或负极),该电极反应式为_______。
(2)石墨电极为________ (填阳极或阴极),乙中总反应离子方程式为________。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_________(填“增大”“减小”或“不变”)。
(4)若甲中消耗0.01molO2,丙中精铜增重_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO3溶液常温时显酸性,溶液中存在以下平衡:
HSO3-+H2O![]() H2SO3+OH- ①
H2SO3+OH- ①
HSO3-![]() H++SO32- ②
H++SO32- ②
向0.1mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大
B.加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+c(SO32-)
C.加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-)
D.加入少量NaOH溶液,![]() 、
、![]() 的值均增大
的值均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活密切相关.下列说法不正确的是![]()
A.采用加热方法消毒的目的是使蛋白质变性而杀灭细菌
B.石油分馏可得到石油气、汽油、煤油、柴油等
C.“海水淡化”可以解决“淡水供应危机”,加入明矾可以使海水淡化
D.已知![]() 所以工业上用
所以工业上用![]() 制取
制取![]() 时,用MnS除去溶液中含有的
时,用MnS除去溶液中含有的![]() 离子
离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准浓度氢氧化钠的溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定的浓度偏大的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③酸式滴定用蒸馏水洗净后,未用盐酸润洗
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
⑤滴定后观察碱式滴定管读数时,俯视刻度线
A.①④B.①③C.②③D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质与其用途完全符合的有多少条( )
![]() 光导纤维
光导纤维 ![]() 制玻璃
制玻璃 ![]() 红色油漆或涂料
红色油漆或涂料 ![]() 耐火材料
耐火材料 ![]() 消毒剂
消毒剂 ![]() 制纯碱
制纯碱![]() 食品漂白剂
食品漂白剂![]() 焊接钢轨
焊接钢轨![]() 制冷剂.
制冷剂.![]() 人工降雨
人工降雨
A.6B.7C.5D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A.甲酸钠溶液和盐酸反应:HCOO-+H+=HCOOH
B.硫化钠的第一步水解:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C.醋酸钡溶液和硫酸反应:Ba2++SO42—=BaSO4↓
D.氢氧化钙溶液和碳酸氢镁反应:Ca2++OH-+HCO3-=CaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com