
ΓΨΧβΡΩΓΩœθΥαοß «“Μ÷÷≥Θ”ΟΒΡΜ·Ζ Θ§ΤδΙΛ“Β…ζ≤ζΝς≥Χ»γΆΦΘ§«κΜΊ¥πœ¬Ν–Έ ΧβΓΘ

Θ®1Θ©–¥≥ωΖ¥”Π»ίΤςB÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ___ΓΘ
Θ®2Θ©Έϋ ’ΥΰC÷–Ά®»κΩ’ΤχΒΡΡΩΒΡ «___Θ®”ΟΜ·―ßΖΫ≥Χ ΫΫβ ΆΘ©ΘΜCΓΔDΝΫΗωΖ¥”Π»ίΤς÷–ΖΔ…ζΒΡΖ¥”ΠΘ§ τ”Ύ―θΜ·ΜΙ‘≠Ζ¥”ΠΒΡ «___ (ΧνΖ¥”Π»ίΤς¥ζΚ≈)ΓΘ
Θ®3Θ©≈®œθΥα“ΜΑψ±Θ¥φ‘ΎΉΊ…Ϊ ‘ΦΝΤΩάοΘ§≤ΔΖ≈÷Ο‘Ύ“θΝΙ¥ΠΘ§”ΟΜ·―ßΖΫ≥Χ ΫΫβ Ά‘≠“ρΘΚ___ΓΘ
Θ®4Θ©ΧΦ”κ≈®œθΥαΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «___ΓΘ
Θ®5Θ©Φλ―ι≤ζΈοœθΥαοß÷–Κ§”–NH4+ΒΡΖΫΖ® «___ΓΘ
Θ®6Θ©ΫΪ Δ”–12mLNO2ΚΆO2ΒΡΜλΚœΤχΧεΒΡΝΩΆ≤ΒΙΝΔ”ΎΥ°≤έ÷–Θ§≥δΖ÷Ζ¥”ΠΚσΘ§ΜΙ Θ”ύ2mLΈό…ΪΤχΧεΘ§ Θ”ύΒΡΤχΧεΩ…Ρή «___ΓΔ___Θ§‘ρ‘≠ΜλΚœΤχΧε÷–O2ΒΡΧεΜΐΩ…ΡήΈΣ___mLΜρ___mLΓΘ
ΓΨ¥πΑΗΓΩ![]() 4NO+3O2+2H2O=4HNO3 C
4NO+3O2+2H2O=4HNO3 C ![]()
![]() »Γ―υΤΖ…Ό–μ”Ύ ‘ΙήΘ§Φ”’τΝσΥ°»ήΫβΘ§Άυ ‘Ιή÷–Φ”»κ ΝΩ≈®ΒΡ«β―θΜ·ΡΤ»ή“ΚΘ§Φ”»» ‘ΙήΘ§”ΟΡςΉ”Φ–ΉΓ“Μ Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ÷Ο”Ύ ‘ΙήΩΎΘ§»τ ‘÷Ϋ±δάΕΘ®ΜρΫΪ“Μ’Κ”–≈®―ΈΥαΒΡ≤ΘΝßΑτΩΩΫϋ ‘ΙήΩΎΘ§»τ≤ζ…ζΑΉ―ΧΘ©Θ§ΥΒΟς―υΤΖ÷–Κ§”–οßΗυ NO O2 4mL 1.2mL
»Γ―υΤΖ…Ό–μ”Ύ ‘ΙήΘ§Φ”’τΝσΥ°»ήΫβΘ§Άυ ‘Ιή÷–Φ”»κ ΝΩ≈®ΒΡ«β―θΜ·ΡΤ»ή“ΚΘ§Φ”»» ‘ΙήΘ§”ΟΡςΉ”Φ–ΉΓ“Μ Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ÷Ο”Ύ ‘ΙήΩΎΘ§»τ ‘÷Ϋ±δάΕΘ®ΜρΫΪ“Μ’Κ”–≈®―ΈΥαΒΡ≤ΘΝßΑτΩΩΫϋ ‘ΙήΩΎΘ§»τ≤ζ…ζΑΉ―ΧΘ©Θ§ΥΒΟς―υΤΖ÷–Κ§”–οßΗυ NO O2 4mL 1.2mL
ΓΨΫβΈωΓΩ
Θ®1Θ©B÷–Α±ΤχΉΣΜ·ΈΣNOΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ![]() ΘΜ
ΘΜ
Θ®2Θ©‘Ύ’ϊΗω…ζ≤ζΝς≥Χ÷–Θ§Έϋ ’ΥΰC÷–Ά®»κΩ’ΤχΒΡΡΩΒΡ «ΫΪ“Μ―θΜ·ΒΣ―θΜ·≥…Εΰ―θΜ·ΒΣΘ§»ΜΚσ”κΥ°Ζ¥”Π…ζ≥…HNO3Θ§ΤδΖ¥”ΠΖΫ≥Χ ΫΈΣΘΚ4NO+3O2+2H2O=4HNO3ΘΜC÷–NOΉΣΜ·ΈΣNO2 «―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§ΕχœθΥαΈϋ ’Α±Τχ…ζ≥…œθΥαΑ± «Ζ«―θΜ·ΜΙ‘≠Ζ¥”ΠΘΜ
Θ®3Θ©≈®œθΥαΦϊΙβΜρ ή»»“ΉΖ÷ΫβΘ§Υυ“‘”ΠΖ≈÷Ο‘Ύ“θΝΙ¥ΠΘ§Ζ÷ΫβΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ![]() ΘΜ
ΘΜ
Θ®4Θ©C”κ≈®œθΥα‘ΎΦ”»»ΧθΦΰœ¬ΖΔ…ζ…ζ≥…NO2ΓΔCO2ΓΔH2OΘ§ΤδΖ¥”ΠΖΫ≥Χ ΫΈΣΘΚ![]() ΘΜ
ΘΜ
Θ®5Θ©οßΗυάκΉ”≥ΘΦϊΦλ―ιΖΫΖ®ΈΣΘΚΫΪοßΗυάκΉ”ΉΣΜ·ΈΣΑ±ΤχΘ§»ΜΚσάϊ”Ο Σ»σΚλ…Ϊ ·»ο ‘÷ΫΦλ―ιΑ±ΤχΘ§Μράϊ”ΟΑ±Τχ”κHClΖ¥”Π…ζ≥…¬»Μ·οßΨßΧεΘ§ΤδΦλ―ιΖΫΖ®ΈΣΘΚ»Γ―υΤΖ…Ό–μ”Ύ ‘ΙήΘ§Φ”’τΝσΥ°»ήΫβΘ§Άυ ‘Ιή÷–Φ”»κ ΝΩ≈®ΒΡ«β―θΜ·ΡΤ»ή“ΚΘ§Φ”»» ‘ΙήΘ§”ΟΡςΉ”Φ–ΉΓ“Μ Σ»σΒΡΚλ…Ϊ ·»ο ‘÷Ϋ÷Ο”Ύ ‘ΙήΩΎΘ§»τ ‘÷Ϋ±δάΕΘ®ΜρΫΪ“Μ’Κ”–≈®―ΈΥαΒΡ≤ΘΝßΑτΩΩΫϋ ‘ΙήΩΎΘ§»τ≤ζ…ζΑΉ―ΧΘ©Θ§ΥΒΟς―υΤΖ÷–Κ§”–οßΗυΘΜ
Θ®6Θ©Ω…ΡήΖΔ…ζΒΡΖ¥”ΠΈΣΘΚ4NO2+O2+2H2O=4HNO3Θ§3NO2+H2O=2HNO3+NOΘ§ ‘Ιή÷–O2ΚΆNO2ΤχΧεΑ¥ΧεΜΐ±»1ΘΚ4ΜλΚœ»Ϊ≤Ω»ήΫβΘ§“ΚΧε≥δ¬ζ ‘ΙήΘ§ΦΌΕ®»Ϊ≤ΩΈΣΕΰ―θΜ·ΒΣΘ§ Θ”ύΤχΧεΧεΜΐΈΣ![]() ΓΝ12mL=4mLΘ§ ΒΦ «ΫαΙϊ Θ”ύ2mLΤχΧεΘ§–Γ”Ύ4mLΘ§‘ρΥΒΟς Θ”ύΤχΧεΈΣNOΜρ―θΤχΘ§
ΓΝ12mL=4mLΘ§ ΒΦ «ΫαΙϊ Θ”ύ2mLΤχΧεΘ§–Γ”Ύ4mLΘ§‘ρΥΒΟς Θ”ύΤχΧεΈΣNOΜρ―θΤχΘ§
»τΈΣ―θΤχΘ§‘ρ≤ΈΦ”Ζ¥”ΠΒΡΤχΧεΈΣ12mL-2mL=10mLΘ§ΗυΨί4NO2+O2+2H2O=4HNO3Θ§Ω…÷Σ≤ΈΦ”¥ΥΖ¥”ΠΒΡNO2ΒΡΧεΜΐΈΣ10mLΓΝ![]() =8mLΘ§≤ΈΦ”Ζ¥”ΠΒΡO2ΒΡΧεΜΐΈΣ10mL-8mL=2mLΘ§‘≠ΜλΚœΤχΧε÷–O2ΒΡΧεΜΐΈΣ2mL+2mL=4mLΘΜ
=8mLΘ§≤ΈΦ”Ζ¥”ΠΒΡO2ΒΡΧεΜΐΈΣ10mL-8mL=2mLΘ§‘≠ΜλΚœΤχΧε÷–O2ΒΡΧεΜΐΈΣ2mL+2mL=4mLΘΜ
»τ Θ”ύΤχΧεΈΣNOΤχΧεΘ§ΗυΨί3NO2+H2O=2HNO3+NOΘ§Ω…÷ΣΙΐΝΩΒΡNO2ΈΣ3ΓΝ2mL=6mLΘ§Ζ¥”Π4NO2+O2+2H2O=4HNO3œϊΚΡΒΡΤχΧεΉήΧεΜΐΈΣ12mL-6mL=6mLΘ§‘ρΖ¥”ΠœϊΚΡΒΡ―θΤχΈΣ6mLΓΝ![]() =1.2mLΓΘ
=1.2mLΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœϊ≥ΐΚ§ΒΣΜ·ΚœΈοΕ‘¥σΤχΚΆΥ°ΧεΒΡΈέ»Ψ «ΜΖΨ≥±ΘΜΛΒΡ÷Ί“Σ―–ΨΩΩΈΧβΓΘ
(1)“―÷ΣΘΚN2(g)ΘΪO2(g)=2NO(g)ΓΓΓΓΓΓΓΓ ΠΛHΘΫa kJΓΛmolΘ≠1
2NO(g)ΘΪO2(g)=2NO2(g)ΓΓ ΠΛHΘΫb kJΓΛmolΘ≠1
4NH3(g)ΘΪ5O2(g)=4NO(g)ΘΪ6H2O(l)ΓΓ ΠΛHΘΫc kJΓΛmolΘ≠1
‘ρ≥ΘΈ¬≥Θ―Ιœ¬Θ§NH3”κNO2Ζ¥”Π…ζ≥…ΈόΈέ»ΨΈο÷ ΒΡ»»Μ·―ßΖΫ≥Χ Ϋ_____________ΓΘ
(2)Υ°Χε÷–ΙΐΝΩΑ±ΒΣ(“‘NH3±μ Ψ)ΜαΒΦ÷¬Υ°ΧεΗΜ”Σ―χΜ·ΓΘ
ΔΌ”Ο¥Έ¬»ΥαΡΤ≥ΐ»ΞΑ±ΒΣΒΡ‘≠άμ»γΆΦΥυ ΨΘΚ

–¥≥ωΗΟΆΦ ΨΒΡΉήΖ¥”ΠΜ·―ßΖΫ≥Χ ΫΘΚ__________________ΓΘΗΟΖ¥”Π–ηΩΊ÷ΤΈ¬Ε»Θ§Έ¬Ε»ΙΐΗΏ ±Α±ΒΣ»Ξ≥ΐ¬ ΫΒΒΆΒΡ÷ς“Σ‘≠“ρ «______________ΓΘ
ΔΎ»Γ“ΜΕ®ΝΩΒΡΚ§Α±ΒΣΖœΥ°Θ§ΗΡ±δΦ”»κ¥Έ¬»ΥαΡΤΒΡ”ΟΝΩΘ§Ζ¥”Π“ΜΕΈ ±ΦδΚσΘ§»ή“Κ÷–Α±ΒΣ»Ξ≥ΐ¬ ΓΔΉήΒΣ(»ή“Κ÷–Υυ”–Ω…»ή–‘ΒΡΚ§ΒΣΜ·ΚœΈο÷–ΒΣ‘ΣΥΊΒΡΉήΝΩ)»Ξ≥ΐ¬ “‘ΦΑ Θ”ύ¥Έ¬»ΥαΡΤΒΡΚ§ΝΩΥφm(NaClO)ΓΟm(NH3)ΒΡ±δΜ·«ιΩω»γΆΦΥυ ΨΘΚ

Β±m(NaClO)ΓΟm(NH3)>7.6 ±Θ§Υ°Χε÷–ΉήΒΣ»Ξ≥ΐ¬ Ζ¥Εχœ¬ΫΒΘ§Ω…ΡήΒΡ‘≠“ρ «___ΓΘ
(3)ΒγΦΪ…ζΈοΡΛΒγΫβΆ―œθ «ΒγΜ·―ßΚΆΈΔ…ζΈοΙΛ“’ΒΡΉιΚœΓΘΡ≥ΈΔ…ζΈοΡΛΡήάϊ”ΟΒγΫβ≤ζ…ζΒΡΜν–‘‘≠Ή”ΫΪNO3-ΜΙ‘≠ΈΣN2Θ§ΙΛΉς‘≠άμ»γΆΦΥυ ΨΘΚ

ΔΌ–¥≥ωΗΟΜν–‘‘≠Ή””κNO3-Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ________________ΓΘ
ΔΎ»τ―τΦΪ…ζ≥…±ξΉΦΉ¥Ωωœ¬2.24 LΤχΧεΘ§άμ¬έ…œΩ…≥ΐ»ΞNO3-ΒΡΈο÷ ΒΡΝΩΈΣ____molΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–÷ΗΕ®Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «
A. ”Ο ·ΡΪΒγΦΪΒγΫβMgCl2»ή“Κ:Mg2++2C1-+2H2O![]() Mg(OH)2Γΐ+Cl2Γϋ+H2Γϋ
Mg(OH)2Γΐ+Cl2Γϋ+H2Γϋ
B. œρΟςΖ·»ή“Κ÷–ΒΈΦ”ΧΦΥαΡΤ»ή“Κ:2Al3++3CO32-==Al2(CO3)3Γΐ
C. œρCa(HCO3)2»ή“Κ÷–ΒΈΦ”…ΌΉνNaOH»ή“Κ:Ca2++2HCO3-+2OH-==CaCO3Γΐ+CO32-+2H2O
D. œρFe(NO3)3»ή“Κ÷–Φ”»κΙΐΝΩΒΡHI»ή“Κ:2NO3-+8H++6I-==3I2+2NOΓϋ+4H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ±ξΉΦΉ¥Ωωœ¬Θ§œ¬Ν– Β―ι”Ο»γΆΦΥυ ΨΉΑ÷Ο≤ΜΡήΆξ≥…ΒΡ « Θ® Θ©
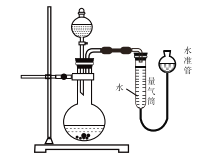
A. ≤βΕ®“ΜΕ®÷ ΝΩΒΡ![]() ΚΆ
ΚΆ![]() ΜλΚœΈο÷–
ΜλΚœΈο÷–![]() ΒΡΚ§ΝΩ
ΒΡΚ§ΝΩ
B. »ΖΕ®Ζ÷Ή” ΫΈΣ![]() ΒΡ”–ΜζΈοΖ÷Ή”÷–Κ§ΜνΤΟ«β‘≠Ή”ΒΡΗω ΐ
ΒΡ”–ΜζΈοΖ÷Ή”÷–Κ§ΜνΤΟ«β‘≠Ή”ΒΡΗω ΐ
C. ≤βΕ®“ΜΕ®÷ ΝΩΒΡ![]() ΨßΧε÷–ΫαΨßΥ° ΐΡΩ
ΨßΧε÷–ΫαΨßΥ° ΐΡΩ
D. ±»ΫœFe3+ΚΆCu2+Ε‘“ΜΕ®÷ ΝΩΒΡΥΪ―θΥ°Ζ÷ΫβΖ¥”ΠΒΡ¥ΏΜ·–߬
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σ4NH3+5O2![]() 4NO+6H2OΘ§»τΖ¥”ΠΥΌ¬ Ζ÷±π”Οv(NH3)ΓΔv(O2)ΓΔv(NO)ΓΔv(H2O)±μ ΨΘ§’ΐ»ΖΒΡΙΊœΒ «Θ® Θ©
4NO+6H2OΘ§»τΖ¥”ΠΥΌ¬ Ζ÷±π”Οv(NH3)ΓΔv(O2)ΓΔv(NO)ΓΔv(H2O)±μ ΨΘ§’ΐ»ΖΒΡΙΊœΒ «Θ® Θ©
A.4v(NH3)=5v(O2)B.5v(O2)=6v(H2O)
C.4v(NH3)=6v(H2O)D.4v(O2)= 5v(NO)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γœ¬ΆΦΥυ ΨΘ§ΆΦΔώ «Κψ―ΙΟή±’»ίΤςΘ§ΆΦΔρ «Κψ»ίΟή±’»ίΤςΓΘΒ±ΤδΥϋΧθΦΰœύΆ§ ±Θ§‘ΎΔώΓΔΔρ÷–Ζ÷±πΦ”»κ2mol![]() ΚΆ2mol
ΚΆ2mol![]() Θ§ΩΣ Φ ±»ίΤςΒΡΧεΜΐΨυΈΣVLΘ§ΖΔ…ζ»γœ¬Ζ¥”Π≤Δ¥οΒΫΤΫΚβΉ¥Χ§
Θ§ΩΣ Φ ±»ίΤςΒΡΧεΜΐΨυΈΣVLΘ§ΖΔ…ζ»γœ¬Ζ¥”Π≤Δ¥οΒΫΤΫΚβΉ¥Χ§![]() Χα ΨΘΚΈο÷ XΘ§YΒΡΉ¥Χ§ΨυΈ¥÷ΣΘ§Έο÷ ZΒΡΉ¥Χ§ΈΣΤχΧ§)Θ§2X(?)+Y(?)
Χα ΨΘΚΈο÷ XΘ§YΒΡΉ¥Χ§ΨυΈ¥÷ΣΘ§Έο÷ ZΒΡΉ¥Χ§ΈΣΤχΧ§)Θ§2X(?)+Y(?)![]() aZ(g)¥Υ ±Δώ÷–XΘ§YΘ§ZΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ1:3:2ΓΘœ¬Ν–≈–Εœ’ΐ»ΖΒΡ «
aZ(g)¥Υ ±Δώ÷–XΘ§YΘ§ZΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ1:3:2ΓΘœ¬Ν–≈–Εœ’ΐ»ΖΒΡ «![]()
![]()
Δώ Δρ
Δρ Δσ
Δσ
A.Έο÷ ZΒΡΜ·―ßΦΤΝΩ ΐ a= 2
B.»τXΓΔYΨυΈΣΤχΧ§Θ§‘ρ‘ΎΤΫΚβ ±XΒΡΉΣΜ·¬ ΘΚΔώ<Δρ
C.»τΔρ÷–ΤχΧεΒΡΟήΕ»»γΆΦΔσΥυ ΨΘ§‘ρXΓΔY÷–÷Μ”–“Μ÷÷ΈΣΤχΧ§
D.»τXΈΣΙΧΧ§ΓΔYΈΣΤχΧ§Θ§‘ρΔώΓΔΔρ÷–¥”ΩΣ ΦΒΫΤΫΚβΥυ–ηΒΡ ±ΦδΘΚΔώ>Δρ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©‘Ύ25ΓφΓΔ1.01ΓΝ105Pa ±Θ§16gΝρΖέ‘ΎΉψΝΩΒΡ―θΤχ÷–≥δΖ÷»Φ…’…ζ≥…Εΰ―θΜ·ΝρΤχΧεΘ§Ζ≈≥ω148.5kJΒΡ»»ΝΩΘ§‘ρSΒΡ»Φ…’»»ΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣΘΚ_____________________ΓΘ
Θ®2Θ©1L 1mol/LœΓ―ΈΥαΗζ1L 1mol/L NaOH»ή“ΚΤπ÷–ΚΆΖ¥”ΠΖ≈≥ω57.3kJ»»ΝΩΘ§Τδ÷–ΚΆ»»ΒΡ»»Μ·―ßΖΫ≥ΧΈΣΘΚ________________ΓΘ
Θ®3Θ©“―÷Σ»γΆΦΥυ ΨΒΡΩ…ΡφΖ¥”ΠΘΚ

ΔΌA(g)+B(g)![]() 2C(g) +D(g)ΘΜΠΛH = Q kJ/mol‘ρQ_______0Θ®ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±Θ©
2C(g) +D(g)ΘΜΠΛH = Q kJ/mol‘ρQ_______0Θ®ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±Θ©
ΔΎΖ¥”ΠΧεœΒ÷–Φ”»κ¥ΏΜ·ΦΝΘ§Ζ¥”ΠΥΌ¬ ‘ω¥σΘ§‘ρE1ΒΡ±δΜ· «ΘΚ E1_______Θ§ΠΛHΒΡ±δΜ· «ΘΚΠΛH________Θ®ΧνΓΑ‘ω¥σΓ±ΓΑΦθ–ΓΓ±ΓΑ≤Μ±δΓ±Θ©ΓΘ
Θ®4Θ©ΖΔ…δΈά–«”Ο![]() Ής»ΦΝœΘ§
Ής»ΦΝœΘ§![]() Ής―θΜ·ΦΝΘ§ΝΫ’ΏΖ¥”Π…ζ≥…N2ΚΆΥ°’τΤχΘ§“―÷ΣΘΚN2(g) ΘΪ2O2Θ®gΘ©ΘΫ 2NO2(g)ΓςH1 ΘΫΘΪ67.7kJ/mol;N2H4Θ®gΘ©ΘΪO2Θ®gΘ©ΘΫ N2Θ®gΘ©ΘΪ2H2OΘ®gΘ© ΓςH2ΘΫΘ≠534kJ/mol,‘ρ1molΤχΧεκ¬ΚΆNO2Άξ»ΪΖ¥”Π ±ΒΡΖ¥”Π»»ΓςH=____________kJ/molΓΘ
Ής―θΜ·ΦΝΘ§ΝΫ’ΏΖ¥”Π…ζ≥…N2ΚΆΥ°’τΤχΘ§“―÷ΣΘΚN2(g) ΘΪ2O2Θ®gΘ©ΘΫ 2NO2(g)ΓςH1 ΘΫΘΪ67.7kJ/mol;N2H4Θ®gΘ©ΘΪO2Θ®gΘ©ΘΫ N2Θ®gΘ©ΘΪ2H2OΘ®gΘ© ΓςH2ΘΫΘ≠534kJ/mol,‘ρ1molΤχΧεκ¬ΚΆNO2Άξ»ΪΖ¥”Π ±ΒΡΖ¥”Π»»ΓςH=____________kJ/molΓΘ
Θ®5Θ©Ζ¥”ΠA+3B=2C+2D‘ΎΥΡ÷÷≤ΜΆ§«ιΩωœ¬ΒΡΖ¥”ΠΥΌ¬ Ζ÷±πΈΣΘΚ
ΔΌΘ°vΘ®AΘ©=0.15mol/Θ®LsΘ© ΔΎΘ°vΘ®BΘ©=0.6mol/Θ®LsΘ©ΔέΘ°vΘ®CΘ©=0.4mol/Θ®LsΘ© ΔήΘ°vΘ®DΘ©=0.45mol/Θ®LsΘ©‘ρΗΟΖ¥”ΠΫχ––ΉνΩλΒΡΈΣ________Θ®Χν–ρΚ≈Θ©
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣΘΚKClO3ΘΪ6HCl(≈®)=KClΘΪ3Cl2ΓϋΘΪ3H2OΘ§»γΆΦΥυ ΨΘ§ΫΪ…ΌΝΩ ‘ΦΝΖ÷±πΖ≈»κ≈ύ―χΟσ÷–ΒΡœύ”ΠΈΜ÷ΟΘ§ Β―ι ±ΫΪ≈®―ΈΥαΒΈ‘ΎKClO3ΨßΧε…œΘ§≤Δ”Ο±μΟφΟσΗ«ΚΟΓΘœ¬±μ÷–”… Β―ιœ÷œσΒΟ≥ωΒΡΫα¬έΆξ»Ϊ’ΐ»ΖΒΡ «(ΓΓΓΓ)
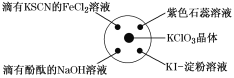
―Γœν | Β―ιœ÷œσ | Ϋα¬έ |
A | ΒΈ”–KSCNΒΡFeCl2»ή“Κ±δΚλ | Cl2ΨΏ”–ΜΙ‘≠–‘ |
B | ΒΈ”–Ζ”ΧΣΒΡNaOH»ή“ΚΆ …Ϊ | Cl2ΨΏ”–Υα–‘ |
C | Ήœ…Ϊ ·»ο»ή“Κœ»±δΚλΚσΆ …Ϊ | Cl2ΨΏ”–Τ·ΑΉ–‘ |
D | KIΒμΖέ»ή“Κ±δ≥…άΕ…Ϊ | Cl2ΨΏ”–―θΜ·–‘ |
A.AB.BC.CD.D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕ‘Ω…ΡφΖ¥”Π4NH3(g)ΘΪ5O2(g)![]() 4NO(g) ΘΪ6H2O (g)Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©
4NO(g) ΘΪ6H2O (g)Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©
A.Ζ¥”Π¥οΒΫΤΫΚβ ±Θ§»τΝΫ÷÷Ζ¥”ΠΈοΒΡΉΣΜ·¬ œύΒ»Θ§‘ρΤπ ΦΆΕ»κΒΡn(NH3)ΘΚn(O2)=4:5
B.Ζ¥”Π¥οΒΫΤΫΚβΚσΘ§Ε‘ΧεœΒ“Μ÷±Ϋχ––Φ”―ΙΘ§ΤΫΚβΉή «Ρφœρ“ΤΕ·
C.Ζ¥”Π¥οΒΫΤΫΚβ ±Θ§»τœρ―Ι«ΩΙΧΕ®ΒΡΟή±’»ίΤς÷–≥δ»κœΓ”–ΤχΧεΘ§ΤΫΚβ≤Μ“ΤΕ·
D.Β±v’ΐ(NH3)ΘΚv’ΐ(NO) =1:1 ±Θ§ΥΒΟςΗΟΜ·―ßΖ¥”Π“―Ψ≠¥οΒΫΤΫΚβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com