


| 5+1-2×3 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| 78 |
| NA |
| 312 |
| NA |
| 3 |
| ||||
| 3 |
| ||
| 3 |
| ||


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
| A、用氯水、KSCN溶液检验FeCl3中是否有FeCl2溶液 |
| B、用酸性KMnO4溶液检验FeCl3中是否有FeCl2 |
| C、用NaOH溶液检验MgCl2中是否有FeCl2 |
| D、用硝酸检验某黄色固体是纯铜还是黄铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D为原子序数依次增大的前四周期元素,元素A原子最外层电子数比内层多3个,元素B基态原子核外有2个未成对电子,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族.
A、B、C、D为原子序数依次增大的前四周期元素,元素A原子最外层电子数比内层多3个,元素B基态原子核外有2个未成对电子,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族.查看答案和解析>>
科目:高中化学 来源: 题型:
| 部分电离的物质 | H2O | NH3?H2O(一水合氨) | HClO(次氯酸) |
| 电离产生的离子 | H+和OH- | NH4+和OH- | H+和ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
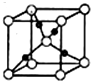 向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得铜锰氧化物CuMn2O4.在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O.
向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得铜锰氧化物CuMn2O4.在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
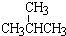 和
和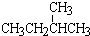 ;②正戊烷和
;②正戊烷和 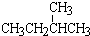 ;③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3)
;③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3)查看答案和解析>>
科目:高中化学 来源: 题型:
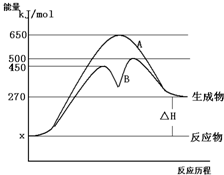 反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示.
反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 | B、0.08 |
| C、0.04 | D、0.02 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com