
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2-中的若干种离子,离子浓度均为0.1mol·L-1,某同学进行了如下实验,下列说法正确的是

A. 无法确定原试液中是否含有Al3+、Cl-
B. 原溶液中存在NH4+、Fe2+、Cl-、SO42-
C. 无法确定沉淀C的成分
D. 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
【答案】B
【解析】
加入过量稀硫酸无明显变化,说明无碳酸根离子、Ba2+、AlO2﹣;加入硝酸钡后有气体产生,说明有亚铁离子存在且被氧化,沉淀为硫酸钡;加入NaOH溶液后有气体,说明原溶液中有铵根离子,气体为氨气,沉淀B为红褐色氢氧化铁沉淀;通入少量CO2产生沉淀,先后与OH﹣、Ba2+反应,沉淀C为碳酸钡,不能说明存在Al3+。因为离子浓度均为0.1molL﹣1,从电荷的角度出发,只能含有NH4+、Fe2+、Cl﹣、SO42﹣才能保证电荷守恒,K+必然不能存在。
A. 通过上述分析,原试液中确定含有Cl-,无法确定含有Al3+,故A错误;
B. 通过上述分析可知原溶液中存在NH4+、Fe2+、Cl-、SO42-,故B正确;
C. 通过上述分析可知沉淀C的成分为碳酸钡,故C错误;
D. 通过上述分析可知滤液X中不存在大量的Ba2+,故D错误;
综上所述,本题正确答案为B。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4L己烷中含有分子数目为NA
B. 1mol/LNaOH溶液中含有Na+数目为NA
C. 7.8gNa2O2中含有的共价键数目为0.1NA
D. 将0.5molN2O4充入密闭容器中充分反应转化成NO2的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z 的原子序数逐渐增大,四种元素形成的化合物甲的结构如图所示。且 W 与 X、Y、Z 均可形成电子数相等的分子,W2Z常温常压下为液体。下列说法正确的是
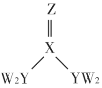
A.YW3 分子中的键角为120°
B.W2Z 的稳定性大于YW3
C.1mol甲分子中存在2mol Y-W键
D.Y 元素的氧化物对应的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯磺酸(HSO3Cl)在糖精、磺胺药的生产中有重要的应用。常温常压下氯磺酸为无色油状液体,沸点约为152℃,吸湿性和腐蚀性极强,在空气中发烟。学习小组在实验室用SO3和HCl来制备HSO3Cl并测定产品纯度。设计如下实验(夹持装置略去)。请回答下列问题:
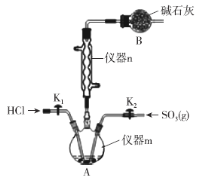
(1)仪器m的名称为___。
(2)已知:HSO3Cl中硫元素为+6价,O原子和Cl原子的最外层均满足8电子稳定结构,则HSO3Cl中的化学键为___ (填“离子键”、“极性键”或“非极性键”)。
(3)SO3可由五氧化二磷与浓硫酸共热制备,发生反应的化学方程式为___。
(4)装置B的作用为___。由仪器n可知制备HSO3Cl的反应为___ (填“放热反应”或“吸热反应”)。
(5)HSO3Cl纯度的测定(仪器m中得到的HSO3Cl中常溶有少量的SO3):
i.取25.0g产品溶于水中,加入过量的Ba(NO3)2溶液充分反应后,过滤。
ii.向滤液中加入过量的AgNO3溶液,过滤、洗涤、干燥、称量,测量所得沉淀AgCl的质量为28.7g。
①HSO3Cl遇水发生反应的化学方程式为___。
②产品HSO3Cl的纯度为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
实验室用干燥、纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器A冷却水的进水口为________(填“a”或“b”)。
(2)仪器B中盛放的药品是________,其目的是________________________。
(3)实验时,装置丁中发生反应的离子方程式为______________________________,当生成6.72L的氯气(标况下),转移电子的物质的量为________。
(4)装置丙中盛放的试剂是________,若缺少装置乙,对实验造成的影响是_______________。
(5)少量硫酰氯也可用液态氯磺酸(ClSO3H)低温催化分解获得,该反应的化学方程式为:2ClSO3H=H2SO4 +SO2Cl2,从分解产物中分离出硫酰氯的操作是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )

A. 两条曲线间任意点均有c(H+)·c(OH-)=Kw
B. M区域内任意点均有c(H+)<c(OH-)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10 mL 0.21 molL﹣1的盐酸和10 mL 0.1 molL﹣1Ba(OH)2溶液混合,再用水稀释至5 L,取出10 mL滴入甲基橙试剂,则溶液显示的颜色是( )
A. 蓝色B. 红色C. 黄色D. 橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.乳酸乙酯(2-羟基丙酸乙酯)常用于调制果香型、乳香型食用和酒用香精。为了在实验室制取乳酸乙酯,某研究性学习小组同学首先查阅资料,获得下列信息:
①部分物质的沸点:
物质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
②乳酸乙酯易溶于苯、乙醇;水、乙醇、苯的混合物在64.85℃时,能按一定的比例以共沸物的形式一起蒸发。
该研究性学习小组同学拟采用如图所示(未画全)的主要装置制取乳酸乙酯,其主要实验步骤如下:
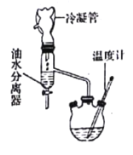
第一步:在反应容器中加入0.1 mol无水乳酸、45.0 mL(密度:0.789g/cm3)无水乙醇、一定量的苯和沸石……;装上油水分离器和冷凝管,缓慢加热回流2 h至反应完全。
第二步:将反应容器中液体倒入盛有适量5%Na2CO3溶液的烧杯中,搅拌并分出有机相后,再用水洗。
第三步:将无水CaCl2加入到水洗后的产品中充分静置,过滤、蒸馏,得产品7.08 g。
(1)第一步操作中,还缺少的试剂是______________________;加入苯的目的是_________________;实验过程中,若油水分离器中水层不再增厚,则表明___________________________________。
(2)第二步中证明“水洗”已经完成的实验方案是_______________________________ 。
(3)本实验制备乳酸乙酯的产率为_________________________。
Ⅱ.磷化铝、磷化锌、磷化钙与水反应产生高毒的PH3气体(熔点为-132℃,还原性强,易自燃),可用于粮食熏蒸杀虫。卫生安全标准规定:当粮食中磷化物(以PH3计)的含量低于0.05m·kg-1时算合格。可用以下方法测定粮食中残留的磷化物含量:
(操作流程)安装吸收装置![]() PH3的产生与吸收
PH3的产生与吸收![]() 转移KMnO4吸收溶液
转移KMnO4吸收溶液![]() 亚硫酸钠标准溶液滴定。
亚硫酸钠标准溶液滴定。
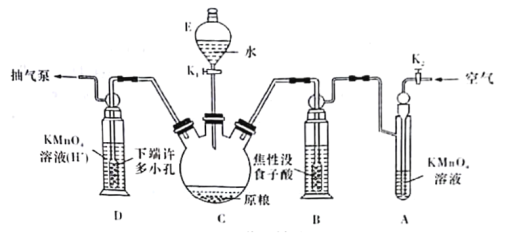
(实验装置)C中盛100 g原粮,D中盛有20.00mL 1.12×10-4 mol·L-1KMnO4溶液(H2SO4酸化)。请回答下列问题:
(4)仪器C的名称是______________;检查整套装置气密性的方法是___________________________________________________________________________。
(5)A中盛装KMnO4,溶液的作用是除去空气中的还原性气体;B中盛装焦性没食子酸的碱性溶液.其作用是______________________________。D中PH3被氧化成磷酸,所发生反应的离子方程式为____________________________________________。
(6)把D中吸收液转移至容量瓶中,加水稀释至250mL,取25.00mL于锥形瓶中,用5.0×10-5 mol·L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗标准Na2SO3溶液11.00 mL,则该原粮中磷化物(以PH3计)的含量为_________________________mg·kg-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质X在一定条件下可转化为物质Y或物质Z:
![]()
![]()
两个反应的能量变化如图所示,下列说法正确的是
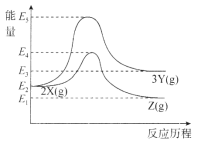
A.两个反应均为放热反应
B.X、Y、Z的关系是互为同素异形体或同分异构体
C.X转化为Y的活化能高于X转化为Z的活化能
D.其它条件一定,加压有利于提高X转化为Z的速率和平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com