
【题目】下列关于铝的叙述中,不正确的是( )
A.铝是地壳里含量最多的金属元素
B.铝容易失去电子,表现还原性
C.在空气中用酒精灯点不着
D.在常温下,铝不能与氧气反应
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】对四种无色溶液进行离子检验,实验结果如下,其中明显错误的是
A. K+、Na+、Cl-、NO3- B. Na+、NO3-、OH-、CO32-
C. Na+、OH-、Cl-、NO3- D. MnO4-、K+、S2-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把含有氧化铁的铁片投入到足量的稀盐酸中,直到铁片完全溶解,经分析该溶液中无Fe3+ , 且生成的Fe2+与反应生成的H2的物质的量之比为3:1,则原混合物中Fe2O3与Fe的物质的量之比为( )
A.1:1
B.2:5
C.4:1
D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料。已知0.5molN2H4(g)完全燃烧生成氨气和气态水时,放出267kJ热量.则下列热化学方程中正确的是
A.![]() N2H4(g)+
N2H4(g)+![]() O2(g)=
O2(g)=![]() N2(g)+H2O(g) △H=+267kJ/mol
N2(g)+H2O(g) △H=+267kJ/mol
B.N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=-534kJ/mol
C.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=+534kJ/mol
D.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修物质结构与性质】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在 对自旋相反的电子,基态氮原子的价层电子排布图为_________________________。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为 ,其中氧原子的杂化方式为 。
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= 。CO与N2结构相似,CO分子内σ键与π键个数之比为 。
(4)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是 。
(5)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释H2SeO4比H2SeO3酸性强的原因: ;
(6)已知Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
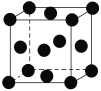
(7)用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,Cu的原子半径为________cm(阿伏加德罗常数为NA,只要求列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中可逆反应2NO2(g)![]() 2NO(g)+O2(g),达到平衡状态的标志是
2NO(g)+O2(g),达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n mol NO2
②单位时间内生成n molO2的同时生成2n mol NO
③混合气体的颜色不再改变的状态
④用NO2、NO、O2表示的反应速率的比为2:2:1的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
⑧2V正(NO2)=2V逆(O2)
A.①③⑥⑦ B.②⑤⑥⑦ C.①③④⑤⑧ D.①②③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现进行实验,测定草酸晶体(H2C2O4·xH2O)中的x值;
(1)称取Wg草酸晶体,配成100.00mL溶液
(2)取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定至KMnO4不再褪色为止,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
①本实验中,必需要用的仪器有(从下列仪器中选择,填序号)__________________,还缺少的仪器有(填名称):_______________________。
A、托盘天平(带砝码、镊子)
B、滴定管
C、100mL的量筒
D、100mL的容量瓶
E、烧杯
F、漏斗
G、锥形瓶
H、玻璃棒
I、药匙
J、烧瓶
②标准液KMnO4溶液应装在__________式滴定管中。
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x的值会__________(填偏大、偏小、无影响)。
④在滴定过程中若用去amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_________mol·L-1,由此,x=__________。
⑤若滴定终点读数时仰视刻度,则计算的x值会__________(填偏大、偏小、无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生。则下列结论正确的是( )
A.滤液中一定有Fe(NO3)3
B.滤渣只含Ag和Cu,一定无Zn
C.滤渣中一定有Ag、Cu和Fe,一定无Zn
D.滤渣中一定有Ag、Cu、Fe和Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”实施的是
A.推广使用燃煤脱硫技术,减少SO2污染
B.实施绿化工程,防治扬尘污染
C.加快清洁能源的开发利用
D.加大石油、煤炭的开发速度,提倡使用化石燃料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com