
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下
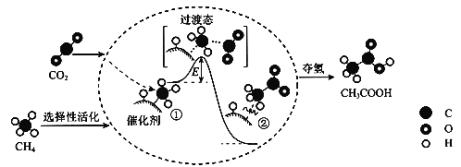
下列说法正确的是
A. 生成CH3COOH总反应的原子利用率小于100%
B. CH4+CO2→CH3COOH过程中,CH4分子中所有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效改变该反应的反应热
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某烧碱样品(含有氯化钠的杂质)的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________称量。配制溶液选用________(填编号字母)
A.小烧杯中 B.洁净纸片上
C.500 mL容量瓶 D.500 mL试剂瓶
(2)为了避免测定过程中样品部分与空气中二氧化碳反应导致结果偏差,滴定时,用0.2000 mol/L的盐酸标准液来滴定待测溶液,可选用________(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
(3)滴定过程中,眼睛应注视_____________,若用酚酞做指示剂,滴定终点的标志是____________,滴定结果是________(偏大,偏小,不变),理由______________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________mol/L,烧碱样品的纯度是____________。
滴定次数 | 待测溶液体积 (mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如右。下列说法不正确的是

A. 该过程将太阳能转化成为化学能
B. 该过程中,只涉及极性键的断裂与生成
C. 氧化剂与还原剂的物质的量之比为1∶3
D. 原料气N2可通过分离液态空气获得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种实验某气体化学性质的实验装置,图中B为开关。如先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条褪色。则D瓶中盛有的溶液是( )

A. 浓硫酸B. 饱和氯化钠溶液C. 浓氢氧化钠溶液D. 氢氧化钙悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按下面框图进行反应。又知D溶液为黄色,E溶液为无色,请回答:
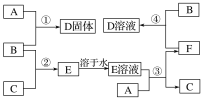
(1)A是__________,B是__________,C是_______________(填写化学式)。
(2)反应①的化学方程式为_______________________________。
(3)反应③的化学方程式为________________________________________。
(4)反应④的化学方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述正确的是
A.H2还原CuO的反应只属于还原反应
B.置换反应都是氧化还原反应,所以,3CO+Fe2O3![]() 2Fe+3CO2既是置换反应又是氧化还原反应
2Fe+3CO2既是置换反应又是氧化还原反应
C.3O2![]() 2O3是氧化还原反应
2O3是氧化还原反应
D.复分解反应一定不是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应2Al+6HCl=2AlCl3+3H2中:
(1)该反应被氧化的元素是______,被还原的元素是_______(填元素符号)。
(2)该反应中氧化剂是________,还原剂是________(填元素符号)。
(3)若反应中转移电子3mol,则在反应中消耗Al________mol。
(4)用双线桥法表示下列反应的电子转移情况:________。
Zn + 2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学设计了如图所示的实验装置。该装置既可用于制取气体,又可用于验证物质的性质。

(1)打开K1,关闭K2,可制取某些气体。
甲同学认为装置I可用于制取H2、NH3、O2,但装置Ⅱ只能收集H2、NH3,不能收集O2,其理由是_______。
乙同学认为在不改动装置Ⅱ仪器的前提下,进行适当改进,也可收集O2,你认为改进方法是:_____。
(2)打开K2,关闭K1,能比较一些物质的性质。
丙同学设计实验比较氧化性:KMnO4>Cl2>Br2。由A向B中加浓盐酸后一段时间,观察到C中的现象是_____;仪器D在该装置中的作用是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下方法来合成甲醇:
(1)用CO2生产甲醇。
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l) △H=﹣akJmol﹣1;
2H2(g)+O2(g)═2H2O(l) △H=﹣b kJmol﹣1;
则表示CH3OH(g)燃烧的热化学方程式为:____________________。
(2)用CO生产甲醇。
已知:CO(g)+2H2(g) ![]() CH3OH(g),下图是该反应在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g),下图是该反应在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1_______K2 (填 “>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是______________。
A.升高温度 B. 将CH3OH(g)从体系中分离
C.使用合适的催化剂 D. 充入He,使体系总压强增大
(3)甲醇(CH3OH)可以用作燃料电池,该电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气。负极发生的电极反应式是________________________,正极发生的电极反应式是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com