
【题目】某兴趣小组同学设计了如图所示的实验装置。该装置既可用于制取气体,又可用于验证物质的性质。

(1)打开K1,关闭K2,可制取某些气体。
甲同学认为装置I可用于制取H2、NH3、O2,但装置Ⅱ只能收集H2、NH3,不能收集O2,其理由是_______。
乙同学认为在不改动装置Ⅱ仪器的前提下,进行适当改进,也可收集O2,你认为改进方法是:_____。
(2)打开K2,关闭K1,能比较一些物质的性质。
丙同学设计实验比较氧化性:KMnO4>Cl2>Br2。由A向B中加浓盐酸后一段时间,观察到C中的现象是_____;仪器D在该装置中的作用是_______。
【答案】氧气的密度比空气大 将装置Ⅱ加满水 溶液呈橙色 防止发生倒吸现象
【解析】
(1)氧气密度比空气大,用排空气法收集,需用向上排空气法收集,Ⅱ装置中进气管短,出气管长,为向下排空气法;用排水法可以收集O2等气体;
(2)装置Ⅰ、Ⅲ验证物质的性质(K2打开,K1关闭).根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,如要设计实验证明氧化性KClO3>Cl2>Br2,则I中发生KClO3和浓盐酸的氧化还原反应,Ⅲ中发生氯气与NaBr的氧化还原反应,有缓冲作用的装置能防止倒吸。
(1)K2关闭,K1打开,甲同学:Ⅱ装置中进气管短,出气管长,为向下排空气法,O2的密度大于空气的密度,则氧气应采用向上排空气法收集,乙同学:O2 不能与水发生反应,而且难溶于水,所以能采用排水法收集;所以改进方法是将装置Ⅱ中装满水;
(2)根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,如要设计实验证明氧化性KClO3>Cl2>Br2,装置Ⅰ、Ⅲ验证物质的性质(K2打开,K1关闭),则I中发生KClO3和浓盐酸的氧化还原反应,Ⅲ中发生氯气与NaBr的氧化还原反应,由氧化性为氧化剂>氧化产物,则A中为浓盐酸,B中为KClO3固体,C中为NaBr溶液,观察到C中的现象为溶液呈橙色,仪器D为干燥管,有缓冲作用,所以能防止倒吸。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能的转换形态),人们将适应“低碳经济”和“低碳生活”。下列说法不正确的是
A. 研究菠菜蛋白质“发电”不属于“太阳能文明”
B. 发展太阳能经济有助于减缓温室效应
C. 太阳能电池可将太阳能转化为电能
D. 石油和天然气都属于碳素燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下
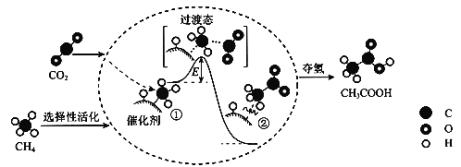
下列说法正确的是
A. 生成CH3COOH总反应的原子利用率小于100%
B. CH4+CO2→CH3COOH过程中,CH4分子中所有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效改变该反应的反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C都是金属,把A浸入C的硝酸盐溶液中,A的表面有C析出,A与B和酸溶液组成原电池时,B为电池的负极。A、B、C三种金属的活动性顺序为( )
A.A>B>CB.A>C>BC.B>A>CD.B>C>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列两种方法制取氯气:①用含HCl 146g的浓盐酸与足量的MnO2反应;②用87g MnO2与足量的浓盐酸反应,则所得Cl2质量
A. ①比②多B. ②比①多C. 一样多D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法中正确的是( )
A. 标准状况下,22.4L CO与11.2L O2混合后,气体的体积约为22.4L
B. 标准状况下,22.4 L CCl4所含的分子数为NA
C. 300 mL 0.2 mol/L蔗糖溶液中所含分子数为0.06NA
D. 14 g由乙烯(C2H4)和丙烯(C3H6)组成的混合物中含有原子的数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据物质的量相关计算填空:
(1)在标准状况下,1.6 g 某氧化物RO3体积为0.448L,则R的相对原子量为________。
(2)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是________。(其中阿伏加德罗常数用NA表示)
(3)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数为________。
(4)VmLAl2(SO4)3溶液中含Al3+ ag,取V/5 mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是______________ 。
(5)10 mL 0.1 mol·L-1 BaCl2溶液恰好能分别使相同体积的硫酸铁、硫酸铜两种溶液中的SO42-完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26次会议新修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),并于2019年5月20日正式生效。下列说法正确的是
A. 56g聚乙烯分子中含碳碳双键的数目为2 NA
B. 2 mol NH3和3molO2在催化剂和加热条件下充分反应生成NO的分子数为2 NA
C. 铅蓄电池放电时负极净增质量比正极净增质量多16g时转移电子数为NA
D. 1L0.5mlol·L-1Al2Fe(SO4)4溶液中阳离子数目小于1.5 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com