
【题目】阅读下列材料后,回答相应问题。
铁在人体中以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的铁盐,如硫酸亚铁(FeSO4)。
(1)人体中经常进行转化Fe2+![]() Fe3+,A反应中Fe2+作__剂,B反应中Fe3+作__剂,服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。这说明维生素C具有__性。
Fe3+,A反应中Fe2+作__剂,B反应中Fe3+作__剂,服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。这说明维生素C具有__性。
(2)新配制的FeCl2溶液应加入__以防止FeCl2转化为FeCl3,要除去FeCl3溶液中少量的FeCl2杂质,可向其中通入适量的__。
(3)为除去废水中的Fe2+,常先将废水中的Fe2+氧化为__(用离子符号表示),再__使Fe3+转化为红褐色的__(用化学式表示)沉淀析出。
(4)在制作印刷电路板的过程中常利用铜与氯化铁溶液的反应。反应的离子方程式为__。
(5)为消除废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,这一处理过程可用两个离子方程式表示为__,__;处理过程中需定期添加的原料是__。
(6)某同学为检验某未知溶液中是否为FeCl2溶液,采取如下实验方案加以验证:取少许未知试液于试管中![]()
![]() 溶液呈红色(证明含有FeCl2),你认为此方案__(填“合理”或“不合理”),若不合理,如何改进:__。
溶液呈红色(证明含有FeCl2),你认为此方案__(填“合理”或“不合理”),若不合理,如何改进:__。
【答案】还原 氧化 还原 铁粉 Cl2 Fe3+ 调节溶液的pH Fe(OH)3 Cu+2Fe3+=Cu2++2Fe2+ 2Fe2++Cl2=2Fe3++2Cl- Fe+2Fe3+=3Fe2+ 铁粉 不合理 取少量溶液,先加KSCN溶液,溶液不变红色,再加入氯水,溶液变成红色,则证明原溶液有Fe2+
【解析】
(1)在A中铁元素的化合价由+2价升高到+3价,铁元素的化合价升高,则A中Fe2+做还原剂,在B中铁元素的化合价由+3价降低为+2价,铁元素的化合价降低,则B中Fe3+做氧化剂,由信息维生素C可使食物中的三价铁离子还原成二价铁离子,该反应中铁元素的化合价降低,则维生素C中某元素的化合价升高,即维生素C为还原剂,体现还原性,故答案为:还原;氧化;还原;
(2)溶液中的Fe2+易被空气中的氧气氧化为Fe3+,则加入少量铁粉防止Fe2+被氧化为Fe3+,Fe2+被氯气氧化生成Fe3+,要除去FeCl3溶液中少量的FeCl2杂质,可向其中通入适量的氯气,故答案为:铁粉;Cl2;
(3)通常向废水中加入过氧化氢,使溶液中的Fe2+变为Fe3+,且不引入其他杂质离子,调节pH,Fe3+与溶液中的OH-反应生成氢氧化铁沉淀,故答案为: Fe3+;调节溶液的pH;Fe(OH)3
(4)铜与氯化铁溶液的反应,其化学反应方程式为:Cu+2FeCl3=CuCl2+2FeCl2,其反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,故答案为:Cu+2Fe3+=Cu2++2Fe2+;
(5)先是氯气与FeCl2溶液反应生成FeCl3,除去Cl2,然后FeCl3与铁粉反应,其对应的离子反应方程式分别为:2Fe2++Cl2=2Fe3++2Cl- ,Fe+2Fe3+=3Fe2+,并且在处理过程中定期添加的原料是铁粉,故答案为:2Fe2++Cl2=2Fe3++2Cl- ,Fe+2Fe3+=3Fe2+;铁粉;
(6)方案不合理,向溶液中通入氯气后发生反应:2FeCl2+Cl2=2FeCl3,再加KSCN溶液,溶液呈红色不能说明原溶液中是否含有Fe2+,因为原溶液中存在Fe3+,也会出现同样的现象,所以应该是先加KSCN溶液,无现象,再加氯水,溶液变成血红色,证明原溶液有Fe2+;故答案为:不合理;取少量溶液,先加KSCN溶液,溶液不变红色,再加入氯水,溶液变成红色,则证明原溶液有Fe2+。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的装置如图所示:
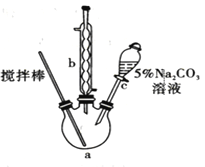
制取的反应原理:CH2 =CHCOOH + HOCH3![]() CH2=CHCOOCH3 + H2O。
CH2=CHCOOCH3 + H2O。
可能用到的信息如下表:
沸点 | 溶解性 | 性质 | |
丙烯酸 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 65℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
丙烯酸甲酯 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
(一)制取丙烯酸甲酯
①取0.14mol丙烯酸、0.2mol的甲醇、少量的浓硫酸放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,加热。
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性。
③分液,取上层油状液体,再加无水Na2SO4后,蒸馏,收集馏分。
(二)检验丙烯酸甲酯的产率,设计如下实验:
①将收集的油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5mol·L-1的KOH溶液10.00 mL,加热使之完全水解。
②用酚酞作指示剂,向冷却后的溶液中滴加0.5 mol·L-1的盐酸,滴定到终点时共消耗盐酸20.00 mL。
回答下列问题:
(1)仪器b的名称是_________________。
(2) 浓硫酸的作用_________________。
(3) 搅拌棒的作用:___________ ; 5% Na2CO3溶液的作用:______________。
(4) 加无水Na2SO4的作用:_____________ ;蒸馏收集___________温度的馏分。
(5) 滴定终点的判断:_________________________________________________。
(6)计算本次酯化反应中丙烯酸的转化率为____________(计算结果保留到小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。
(1)现有下列六种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O2,按照不同的分类标准,它们中有一种物质与其他五种有明显的不同,请找出这种物质,并写出分类的依据(至少要写出两种分类方法)。
①________________________________________________________________________;
②________________________________________________________________________。
(2)从反应中有无离子参加,可以将化学反应分为离子反应和非离子反应。Na2O2与水反应的离子方程式是________。从反应中________,可以将化学反应分为氧化还原反应和非氧化还原反应,从上述物质中分别找出两种能相互反应的物质,各写一个非氧化还原反应的方程式和氧化还原反应的方程式:________________________________________________________________________。
(3)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,请用简单的图示方法表示二者之间的关系___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酰氯(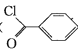 )是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
)是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
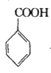 +COCl2
+COCl2![]()
![]() +CO2+HCl
+CO2+HCl
已知物质性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
苯甲酸 | 122.1 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
碳酰氯(COCl2) | -188 | 8.2 | 较易溶于苯、甲苯等。遇水迅速水解,生成氯化氢,与氨很快反应,主要生成尿素[CO(NH2)2]和氯化铵等无毒物质 |
苯甲酰氯 | -1 | 197 | 溶于乙醚、氯仿和苯。遇水或乙醇逐渐分解,生成苯甲酸或苯甲酸乙酯和氯化氢 |
三氯甲烷(CHCl3) | -63.5 | 63.1 | 不溶于水,溶于醇、苯。极易挥发,稳定性差,450℃以上发生热分解 |
I.制备碳酰氯
反应原理:2 CHCl3+O2![]() 2HCl+COCl2
2HCl+COCl2
甲. 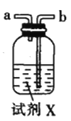 乙.
乙. 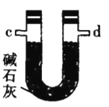 丙.
丙. 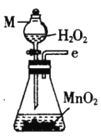 丁.
丁.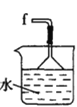 戊
戊 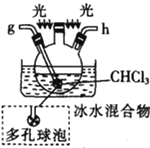
(1)仪器M的名称是____________
(2)按气流由左至右的顺序为___________→c→d→_________→_________→_________→_________→_________.
(3)试剂X是_______________(填名称)。
(4)装置乙中碱石灰的作用是____________。
(5)装置戊中冰水混合物的作用是____________;多孔球泡的作用是________________。
Ⅱ.制备苯甲酰氯(部分夹持装置省略)
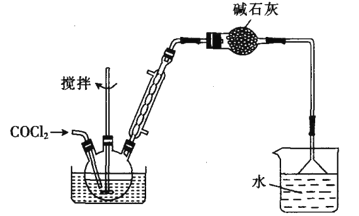
(6)碳酰氯也可以用浓氨水吸收,写出该反应的化学方程式:______________。
若向三颈烧瓶中加入610g苯甲酸,先加热至140~150℃,再通入COCl2,充分反应后,最后产品经减压蒸馏得到562g苯甲酰氯,则苯甲酸的转化率为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊噻嗪是治疗水肿及高血压的药物,其中间体G的一种合成路线如下:

回答下列问题:
(1)A的化学名称是_____________。B中含有官能团的名称为_____________。
(2)反应②的反应类型是________________。
(3)C的结构简式为_______________。
(4)G与新制Cu(OH)2反应的化学方程式为___________________。
(5)X与E互为同分异构体,X中含有六元碳环,且X能与NaOH溶液反应,则符合条件的X的结构简式为_________________。
(6)设计由1,3-丙二醇和丙二酸二乙酯制备 的合成路线(其他试剂任选)______________。
的合成路线(其他试剂任选)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)烷烃A的碳原子数是5,则符合A的结构有____________ 种,其中含有四个甲基的系统命名为________________________________ ;
(2)烷烃B在同温同压下蒸气的密度是H2的43倍,则B的分子式为____________,其中含有3个-CH3的同分异构体的结构简式为___________________________、________________________________;
(3)某气态烃在标准状况下的密度为2.59g/L,该烃的含碳量为82.8%,则分子中碳、氢原子的个数比是______________,分子式是_________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是
A | B | C | D | |
实验 | 新制氯水滴入Na2S 溶液中 | 乙醇滴入K2Cr2O7酸性溶液中 | 饱和FeCl3溶液滴入沸水中 | 草酸滴入KMnO4 酸性溶液中 |
现象 | 产生黄色浑浊 | 溶液由橙色变为绿色 | 液体变为红褐色且澄清透明 | 产生无色气体,溶液紫红色褪去 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示 π键,下列说法不正确的是( )
,其中椭圆框表示 π键,下列说法不正确的是( )
A.N2 分子与 CO 分子中都含有三键
B.CO 分子中有一个 π 键是配位键
C.N2 与 CO 互为等电子体
D.N2 与 CO 的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为 。下列关于该有机物分子结构的说法中正确的是
。下列关于该有机物分子结构的说法中正确的是
A. 最多有18个原子在同一平面内 B. 最多有4个碳原子在一条直线上
C. 最多有12个碳原子在同一平面内 D. 所有原子都可能在同一平面内
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com