
| m |
| M |
| 31g |
| (58+84x)g/mol |
| 31g |
| (58+84x)g/mol |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、实验室制乙烯:CH3CH2OH
| |||
| B、苯酚钠溶液通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |||
C、甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH-
| |||
D、工业制聚乙烯:nCH2=CH2
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| A.浮选法富集方铅矿的过程属于化学变化 |
| B.方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO |
| C.整个冶炼过程中,制取1molPb共转移2mol电子 |
| D.将1molPbS冶炼成Pb理论上至少需要6g碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
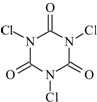 三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂.
三氯异氰尿酸(结构简式如图)是一种极强的氧化剂和氯化剂.| 滴定序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
| 1 | 25.00 | 0.06 | 24.04 |
| 2 | 25.00 | 0.02 | 24.02 |
| 3 | 25.00 | 0.12 | 24.14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入等质量的X、Y两种气体,且X、Y的气体密度相等.当隔板停止滑动时,下列说法一定正确的是( )
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在C、A处充入等质量的X、Y两种气体,且X、Y的气体密度相等.当隔板停止滑动时,下列说法一定正确的是( )| A、X、Y均为气体单质 |
| B、物质的量:n(X)<n(H2)<n(Y) |
| C、X的相对分子质量等于Y的相对分子质量 |
| D、隔板停止滑动时,A、B、C三部分体积相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com