
【题目】将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,组成甲、乙两个装置(如图)。下列说法不正确的是

A.甲为原电池,负极反应为Zn-2e-=Zn2+
B.甲为原电池,Fe电极上有气体放出
C.乙为电解池,阴极反应式为2H++2e-=H2↑
D.一段时间后,甲、乙两表面皿中溶液均有红色出现
【答案】B
【解析】
A. 根据图示可知甲为原电池,由于金属活动性Zn>Fe,所以Zn为负极,失去电子,发生氧化反应,负极反应为Zn-2e-=Zn2+,A正确;
B. 根据图示可知甲为原电池,由于电解质溶液为NaCl中性溶液,因此在Fe电极上溶解在溶液中的O2得到电子,发生还原反应,不放出氢气,B错误;
C. 乙为电解池,阴极上溶液中的阳离子得到电子,发生还原反应,由于得到电子能力H+>Na+,所以阴极的电极反应式为2H++2e-=H2↑,C正确;
D. 甲池为原电池,O2得到电子变为OH-;乙池为电解池,由于溶液中H+不断放电产生H2逸出,破坏了水的电离平衡,所以溶液中c(OH-)>c(H+),因此在一段时间后两个溶液中都是c(OH-)>c(H+),滴有酚酞后甲、乙两表面皿中溶液均有红色出现,D正确;
故合理选项是B。


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素,它们在周期表中的位置如图所示,下列说法正确的是( )

A.四种元素的原子半径由小到大的顺序为r(X)<r(Z)<r(W)<r(Y)
B.X、Y、Z既能形成离子化合物,又能形成共价化合物
C.X与其余三种元素之间形成的核外电子总数为10的微粒只有2种
D.H2Z与HW所含的化学键类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.恒温恒容密闭容器中反应:H2NCOONH4(s) ![]() 2NH3(g)+CO2(g),混合气体的压强不再改变时说明反应已达平衡
2NH3(g)+CO2(g),混合气体的压强不再改变时说明反应已达平衡
B.汽车尾气催化净化时的反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH < 0 ,平衡常数为K1;若反应在绝热容器中进行,平衡常数为K2;则K1 < K2
N2(g)+2CO2(g) ΔH < 0 ,平衡常数为K1;若反应在绝热容器中进行,平衡常数为K2;则K1 < K2
C.某恒容密闭容器中反应:nA(g)+mB(g)![]() pC(g)+qD(g) ΔH > 0已达平衡,则降温时c(B)/c(C)的值增大
pC(g)+qD(g) ΔH > 0已达平衡,则降温时c(B)/c(C)的值增大
D.2NO2(g) ![]() N2O4(g)在常温下即可进行,说明正反应是放热反应
N2O4(g)在常温下即可进行,说明正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有学生将铜与稀硝酸反应实验及NO、NO2性质实验进行改进、整合,装置如图(洗耳球:一种橡胶为材质的工具仪器)。

实验步骤如下:
(一)组装仪器:按照如图装置连接好仪器,关闭所有止水夹;
(二)加入药品:在装置A中的烧杯中加入30%的氢氧化钠溶液,连接好铜丝,在装置C的U型管中加入4.0 mol/L的硝酸,排除U型管左端管内空气;
(三)发生反应:将铜丝向下移动,在硝酸与铜丝接触时可以看到螺旋状铜丝与稀硝酸反应产生气泡,此时打开止水夹①,U型管左端有无色气体产生,硝酸左边液面下降与铜丝脱离接触,反应停止;进行适当的操作,使装置C中产生的气体进入装置B的广口瓶中,气体变为红棕色;
(四)尾气处理:气体进入烧杯中与氢氧化钠溶液反应;
(五)实验再重复进行。
回答下列问题:
(1)实验中要保证装置气密性良好,检验其气密性操作应该在____。
a.步骤(一)(二)之间 b.步骤(二)(三)之间
(2)装置A的烧杯中玻璃仪器的名称是____。
(3)加入稀硝酸,排除U型管左端管内空气的操作是________。
(4)步骤(三)中“进行适当的操作”是打开止水夹____(填写序号),并用洗耳球在U型管右端导管口挤压空气进入。
(5)在尾气处理阶段,使B中广口瓶内气体进入烧杯中的操作是____。尾气中主要含有NO2和空气,与NaOH溶液反应只生成一种盐,则离子方程式为 ___。
(6)某同学发现,本实验结束后硝酸还有很多剩余,请你改进实验,使能达到预期实验目的,反应结束后硝酸的剩余量尽可能较少,你的改进是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研人员以废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO)为原料回收镍,工艺流程如下:

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如表:

回答下列问题:
(1)浸出渣主要成分为_________(填化学式)。
(2)“除铜”时,Fe3+与H2S反应的离子方程式为__________________。
(3)“氧化”的目的是将溶液中Fe2+氧化为Fe3+,温度需控制在40~50℃之间,该步骤温度不能太高的原因是_______________________。
(4)“调pH”时,pH的控制范围为_________。
(5)在碱性条件下,电解产生2NiOOH·H2O的原理分两步,其中第一步是Cl-在阳极被氧化为ClO-,则该电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积固定的密闭容器中加入反应物N2、H2,发生反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如表所示:
2NH3(g)。反应过程中的部分数据如表所示:

下列说法正确的是
A.0~2min内,H2的反应速率为0.1 mol/(L·min)
B.2min时,NH3的物质的量浓度为0.2 mol/L
C.4min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D.4~6min内,容器内气体分子的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子核外p能级、d能级等原子轨道上电子排布为“全空”“半满”“全满”的时候一般更加稳定,称为洪特规则的特例。下列事实不能作为这个规则的证据的是( )
A.硼元素的第一电离能小于铍元素的第一电离能
B.磷元素的第一电离能大于硫元素的第一电离能
C.基态铜原子的核外电子排布式为![]() 而不是
而不是![]()
D.某种激发态碳原子的核外电子排布式为![]() 而不是
而不是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为-96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)铬(24号元素)基态原子的电子排布式为____。
(2)CH3COCH3分子中含有____个π键,含有____个σ键。
(3)固态氯化铬酰属于____晶体,丙酮中碳原子的杂化方式为____,二硫化碳属于____ (填“极性”或“非极性”)分子,分子中含有____(填“极性”或“非极性”)键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物的综合利用既有利于节约资源,又有利于保护环境。某工厂对工业污泥中Cr(III)回收与再利用工艺流程如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
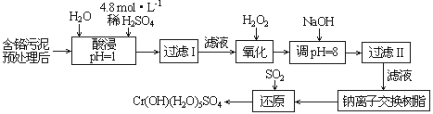
已知:常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH(开始沉淀的pH按金属阳离子浓度为1.0mol·L-1计算)和完全沉淀时溶液的pH,见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.5 | —— | —— | 4.7 | —— |
沉淀完全时的pH | 3.2 | 9.7 | 11.1 | 8 | 6.7 | 9(>9溶解) |
重铬酸根离子(Cr2O72-)在溶液中存在如下平衡:2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
(1)该工厂对工业污泥中Cr(+3价)回收与再利用工艺流程中,其中一步存在氢氧化铁的沉淀溶解平衡:Fe(OH)3(s)![]() Fe3+(aq)+3OH-(aq),其溶度积常数表达式为Ksp=__。
Fe3+(aq)+3OH-(aq),其溶度积常数表达式为Ksp=__。
(2)酸浸时,为了提高浸取率可采取的措施是__(至少答一点)。
(3)加入H2O2的作用是__。调节溶液的pH=8是为了除去__离子。
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的的杂质离子是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com