
����Ŀ��������Li2CO3��K2CO3Ϊ�����,��Ȼ���������������ṩ��Ӧ����ȼ�ϵ����ͼ������˵����ȷ����
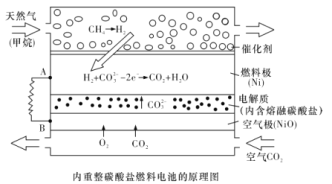
A.�Դ˵��Ϊ��Դ��ⱥ��ʳ��ˮ������0.2 mol e-ת��ʱ����������2.24 L����
B.���Լ���Ϊȼ����ʱ�����缫��Ӧʽ:CH4+5O2- - 8e - =CO32- +2H2O
C.�õ��ʹ�ù������貹��Li2CO3��K2CO3
D.�����������ĵ缫��ӦʽΪO2+4e- +2CO2 =2CO32-
���𰸡�D
��������
A. �Դ˵��Ϊ��Դ��ⱥ��ʳ��ˮ��������������������0.2 mol e-ת��ʱ������0.1mol�������DZ�״���������һ����2.24 L����A����
B. ���Լ���Ϊȼ����ʱ�����缫��Ӧʽ:CH4+4CO32- - 8e - =5CO2 +2H2O����B����
C. �ܷ�ӦΪȼ�Ϻ�������Ӧ������ʹ�ù����в��貹��Li2CO3��K2CO3����C����
D. �����������ĵ缫��ӦʽΪO2+4e- +2CO2 =2CO32-����D��ȷ��
ѡD��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T�� ʱ����һ�ݻ�Ϊ 2 L �ĺ����ܱ������м��� 2 mol A �� 3 mol B��ѹǿΪ P0�� �ڴ������ڵ������½������з�Ӧ��2A(g)+3B(g) 3C(g)��2 ���Ӵﵽƽ�⣬ƽ�������� C ���������Ϊ 37.5���� ��֪�÷�Ӧijһʱ�̵�˲ʱ���ʼ��㹫Ϊv����k����[A]2��[B]3��v��=k����[C]3������ k����k��Ϊ���ʳ�����
��1���������������� ![]() ��ֵ�� ��д����Ҫ�ļ�����̣���ͬ��_____
��ֵ�� ��д����Ҫ�ļ�����̣���ͬ��_____
��2����ij���ʵ�ƽ���ѹ���������ʵ���Ũ��Ҳ���Ա�ʾ��ѧƽ�ⳣ�������� Kp����֪ij�����ѹ(P��)��������ѹ(P��) ������������ʵ������������� T�� ʱ������Ӧ Kp ��ֵ���ú� P0 ����ֵ��ʾ����____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H��ҩ��ϳɵ����м��壬��ͨ�����·����ϳɣ�

��1��B�й���������Ϊ__��
��2��G��H�ķ�Ӧ����Ϊ__��
��3����֪C��һ��ͬ���칹��Ϊ�� ������˵����ȷ����__��
������˵����ȷ����__��
a.�ܷ���������Ӧ
b.�ܷ���������Ӧ
c.1mol��������ȫˮ��������3molNaOH
d.�÷��ӵĺ˴Ź��������з����֮��Ϊ1��2��6��2
e.�������������µ�ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ
��4�� ������̼ԭ�Ӹ���Ϊ__��
������̼ԭ�Ӹ���Ϊ__��
��5��E�ķ�����ΪC14H17O3N��E����ԭ�õ�F��д��E��F�ķ�Ӧ����ʽ��__��
��6����֪����
�ڱ���(![]() �ױ�����
�ױ�����
���Լױ���(CH3CO)2OΪԭ���Ʊ� ��д���Ʊ��ĺϳ�·������ͼ(���Լ���ѡ)��__��
��д���Ʊ��ĺϳ�·������ͼ(���Լ���ѡ)��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о��������༲������������ͻ��(���䡢����Ӳ����)����������ж��ȣ�������һ���������ͷŻ���ڲ���������ġ��ü�ӵ绯ѧ���ɶ�NO����������������ԭ����ͼ��ʾ(����Ĥ����H����H2Oͨ��)����������жϲ���ȷ���� (����)
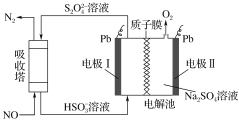
A.�缫��ӵ�Դ�������缫��ӦʽΪ2HSO3-��2H����2e��==S2O42-��2H2O
B.���Ӵӵ缫��ͨ������Ĥ��缫���������ƶ�
C.�������еķ�ӦΪ2NO��2S2O42-��2H2O==N2��4HSO3-
D.ÿ����2 mol NO��������������32 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ψһ����֬���ԵĹ��ᣬ��ҽҩ��ҵ������ͷ������Ѫ������ҩ����������������ҩ������ƥĪ�ֵȵ��м��壬Ҳ������������ʵ����������ԭ���Ʊ���

�ϳɱ������ʵ�鲽�衢װ��ʾ��ͼ������������£�
���� | ״̬ | �۵�/�� | �е�/�� | �ܽ��� |
������ | ��ɫ������ | 119 | 300 | ��������ˮ�����Ѻ������ |
���� | ��ɫ��Һ�� | -116.3 | 34.6 | ���ڵ�̼���������ȷ£�����ˮ |
����ȩ | ��ɫҺ�� | -26 | 179 | ����ˮ�������Ҵ������ѡ������ȷµȻ��� |
�ȷ� | ��ɫҺ�� | -63.5 | 61.3 | �����ڴ����ѡ�����������ˮ |
ʵ�鲽�裺

����һ������ͼ��ʾ��ʵ��װ���м���0.1mol(Լl0.1mL)����ȩ��0.2mol��Լ16mL���ȷ£��������뺬19g�������Ƶ���Һ��ά���¶���55��60�棬���貢������Ӧ1h������ӦҺ��pH�ӽ�����ʱ��ֹͣ��Ӧ��
�����������ӦҺ��200mLˮϡ�ͣ�ÿ����20mL������ȡ���Σ��ϲ��Ѳ㣬�����ա�
��������ˮ����50%�������ữ��pHΪ2��3����ÿ����40mL���ѷ�������ȡ���ϲ���ȡҺ������������ˮ�����ƣ��������ѣ��ôֲ�ƷԼ11.5g����ش��������⣺
(1)ͼ������C��������_________________��װ��B��������_____________
(2)����һ�к��ʵļ��ȷ�ʽ��_____________________��
(3)������������ѵ�Ŀ����_____________________��
(4)�������м���������ˮ�����Ƶ�Ŀ����_____________________��
(5)��ʵ��IJ���Ϊ____________��������λ��Ч���֣���
(6)�������ڸ߶˻�ѧ��Ҳ�к���Ҫ�����ã����Ա�������������Ϊԭ�ϣ��ڴ����Ĵ��¿ɺϳ����Բ�ּ�����������������д���÷�Ӧ�Ļ�ѧ����ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��ˮ�д��ڵ���ƽ��:H2OH����OH�� ��H��0������������ȷ����
A.��ˮ�м���ϡ��ˮ��ƽ�������ƶ���c(OH-)����
B.��ˮ�м������������������ƣ�c(H��)����KW����
C.��ˮ�м�����������CH3COONa��ƽ�������ƶ���c(H��)����
D.��ˮ���ȣ�KW����pH��С��������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ�����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����
A.0.1mol/L NaHS��Һ��c(H+)��c(Na+)=c(S2-)��c(HS-)��c(OH-)
B.0.1mol/L Na2CO3��Һ��c(H2CO3)��c(HCO3-)��c(CO32-)=0.2 mol/L
C.Ũ�Ⱦ�Ϊ0.1 mol/L�� �� NH4Cl ��NH4Al(SO4)2 �� NH4HCO3������Һ������c(NH4+)���ڣ��٣���
D.pH=11��NaOH��Һ��pH =3��CH3COOH��Һ�������ϣ�c(Na+)��c(CH3COO-)��c(OH-)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ԭ��ز����ĵ�ѹ������ǿ�Ⱦ��������⡢���Ҫ��Ϊ���뻯��~��Ϊ��װ���еĵ缫��š���K�պϺ�����˵����ȷ����

��Dװ���д�Cu�缫��ӦΪ:Cu2+��2e-��Cu
��������·�е��ӵ���������Ϊ:�ۡ��ڣ��١��ۣ��ߡ��ޣ��ݡ���
��װ��ԭ������һ����Ƴ�(Ag�����Cu)������Cu��������Ag������
��Aװ����C�缫��ӦΪ:O2��4e-��2H2O��4OH-
A.�٢�B.�ۢ�C.�ڢۢ�D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10L�����ܱ������г���X(g)��Y(g)��������ӦX(g)+Y(g)![]() M(g)+N(g)������ʵ���������±���
M(g)+N(g)������ʵ���������±���
ʵ���� | �¶�/�� | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | |
n(X) | n(Y) | n(M) | ||
�� | 700 | 0.40 | 0.10 | 0.090 |
�� | 800 | 0.10 | 0.40 | 0.080 |
�� | 800 | 0.20 | 0.30 | a |
�� | 900 | 0.10 | 0.15 | b |
����˵������ȷ���ǣ� ��
A.ʵ����У���5minδ���n(M)=0.050mol����0��5minʱ���ڣ���N��ʾ��ƽ����Ӧ��v(N)=1.0��10-3mol��L-1��min-1
B.ʵ����У��ﵽƽ��ʱ��Y��ת����Ϊ20%
C.ʵ����У��÷�Ӧ��ƽ�ⳣ��K=1.0
D.ʵ����У��ﵽƽ��ʱ�� b>0.060
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com