
【题目】在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法不正确的是( )
A.实验①中,若5min未测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速v(N)=1.0×10-3mol·L-1·min-1
B.实验②中,达到平衡时,Y的转化率为20%
C.实验③中,该反应的平衡常数K=1.0
D.实验④中,达到平衡时, b>0.060
【答案】D
【解析】
A. 实验①中,若5min未测得n(M)=0.050mol,则n(N)=0.050mol,则0至5min时间内,用N表示的平均反应速![]() ,故A正确;
,故A正确;
B. 实验②中,达到平衡时,n(M)=0.080mol,则Δn(M)=0.080mol,Δn(Y)=0.080mol,平衡时,则Y的转化率为![]() ,故B正确;
,故B正确;
C. 实验③与实验②温度相同,因此平衡常数相同,根据实验②求出该反应的平衡常数,因实验②中n(M)=0.080mol,n(N)=0.080mol,Δn(M)=0.080mol,则Δn(Y)= Δn(X)=0.080mol,平衡时n(X)=0.1mol0.080mol=0.02mol,n(Y)=0.3mol0.080mol=0.32mol,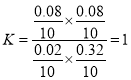 ,故C正确;
,故C正确;
D. 实验④中,当在800℃达到平衡时, ,c = 0.060mol,实验①中,在700℃达到平衡时,
,c = 0.060mol,实验①中,在700℃达到平衡时, 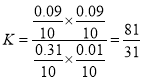 ,从700℃到800℃,升温,平衡常数减小,逆向移动,逆向是吸热反应,正向是放热反应,实验④中,在900℃达到平衡时,平衡逆向移动,因此b<0.060mol,故D错误。
,从700℃到800℃,升温,平衡常数减小,逆向移动,逆向是吸热反应,正向是放热反应,实验④中,在900℃达到平衡时,平衡逆向移动,因此b<0.060mol,故D错误。
综上所述,答案为D。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如图。下列说法正确的是
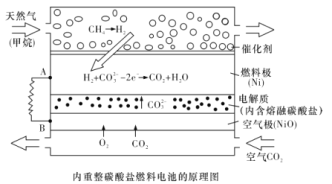
A.以此电池为电源电解饱和食盐水,当有0.2 mol e-转移时,阳极产生2.24 L气体
B.若以甲烷为燃料气时负极电极反应式:CH4+5O2- - 8e - =CO32- +2H2O
C.该电池使用过程中需补充Li2CO3和K2CO3
D.空气极发生的电极反应式为O2+4e- +2CO2 =2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)可逆反应FeO(s)+CO(g)Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表
T/K | 938 | 1100 |
K | 0.68 | 0.40 |
若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态、若降低温度,混合气体的平均相对分子质量__________________;充入氮气,混合气体的密度__________________(填“增大”“减小”或“不变”)。
(2)常温下,浓度均为0.1mol·的下列五种溶液的pH如下表
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①上述盐溶液中的阴离子,水解能力最弱的是__________________。
②根据表中数据判断,浓度均为0.01mol·L-1的下列四种物质的溶液分别稀释100倍,pH变化最小的是_______(填编号)
A. HClO B. HCN C.H2CO3 D. CH3COOH
③据上表数据,请你判断下列反应不能成立的是_______(填编号)
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B. CH3COOH+NaCN=CH3COONa+HCN
C. CO2+H2O+2NaClO=Na2CO3+2HClO
④要增大氯水中HClO的浓度,可向氯水中加入碳酸氢钠,反应的离子方程式为______________
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中的Cl-,利用Ag+与CrO42-生成砖红色沉淀指示到达滴定终点当溶液中Cl恰好完全沉淀(浓度等于1.0×10-5mol·L-1)时,溶液中c(Ag+)为_______mol·L-1,此时溶液中c(CrO42-)等于_______mol·L-1.(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于氧化还原反应的是( )
A.NH4Cl+NaOH ![]() NH3↑+NaCl+H2O
NH3↑+NaCl+H2O
B.MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.Na2O2+2H2O=2NaOH+H2O2
D.SO2+H2O=H2SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素 A、B、C、D、E 的原子序数依次增大,A 元素原子的核外电子只有一种运动状 态;基态 B 原子 s 能级的电子总数比 p 能级的多 1;基态 C 原子和基态 E 原子中成对电子数均是未成对电 子数的 3 倍;D 形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1) E 的元素名称为________。
(2)元素 A、B、C 中,电负性最大的是________(填元素符号,下同),元素 B、C、D 第一电离能由大到小的顺序为________。
(3)与同族其它元素 X 形成的 XA3相比,BA3易液化的原因是________;BA3分子中键角________109°28'(填“>”“<”或“=”),请写出与BA3互为等电子体的一个离子________。
(4)BC3 离子中 B 原子轨道的杂化类型为________,BC3 离子的立体构型为________。
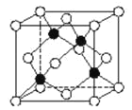
(5)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图 所示)相似。若 DB 的晶胞参数为 a pm,则晶体的密度为________g·cm3(用NA表示阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL某浓度的硫酸溶液中滴入0.1mol·L-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析不正确的是( )

A.V=20
B.b点所示溶液中:c(NH4+)>2c(SO42-)>c(H+)>c(OH-)
C.d点所溶液中:c(NH4+)+c(OH-)=2c(SO42-)+c(H+)
D.NH3·H2O的电离常数K≈2×10-5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某淡黄色固体A(仅含三种元素,式量小于160)可用于制药,为探究其组成和性质,设计并完成如下实验:
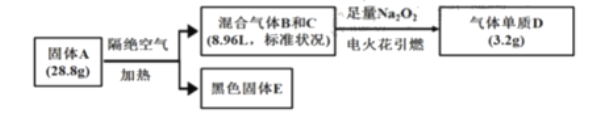
已知:①上述流程中所涉及的反应都充分进行。
②B、C、D均为常见气体。相同情况下气体B的密度大气体C。
③黑色固体![]() 溶于盐酸后滴加KSCN,无明显现象,加适量氯水后,溶液变红。
溶于盐酸后滴加KSCN,无明显现象,加适量氯水后,溶液变红。
请问答:
(1)写出气体B的电子式__,固体A的化学式是__。
(2)黑色固体E与足量浓硝酸反应的离子反应方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019 年“两会”政府工作报告指出:开展蓝天、碧水、净土保卫战。煤的综合利用 可减少直接燃烧造成的污染。下列有关煤干馏的产品说法正确的是
A.![]() 和
和![]() 互为同系物
互为同系物
B.甲烷能被氧气或酸性高锰酸钾溶液氧化
C.CH2=CH2 水化制乙醇属于取代反应
D.![]() 的一氯代物共有 3 种
的一氯代物共有 3 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在pH=5的CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述述正确的是()
CH3COO-+H+,对于该平衡,下列叙述述正确的是()
A.加入水时,平衡向右移动,CH3COOH电离常数增大
B.加入少量CH3COONa固体,平衡向右移动
C.加入少量NaOH固体,平衡向右移动,c(H+)减少
D.稍微升高溶液温度,溶液中的c(OH-)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com