
【题目】科学家发现半胱氨酸能增强艾滋病毒感染者的免疫力,对控制艾滋病毒的蔓延有奇效。已知半胱氨酸的结构简式为 ,下列关于半胱氨酸说法不正确的是
,下列关于半胱氨酸说法不正确的是
A. 能溶于水、乙醇等溶剂
B. 既能与盐酸、又能与NaOH溶液反应
C. 与 (高半胱氨酸)互为同系物
(高半胱氨酸)互为同系物
D. 官能团不变的同分异构体有2种
【答案】D
【解析】
A、分子间氢键增大了物质的溶解性;
B、半胱氨酸中含有氨基,可与盐酸反应,含有羧基,可与NaOH溶液反应;
C、结构相似,在分子组成上相差一个CH2原子团一系列物质,称同系物。
D、半胱氨酸官能团不变的同分异构体有:巯基与氨基换位,巯基和氨基同在α-碳原子上或同在β-碳原子上,由此确定同分异构体。
A、半胱氨酸中含有羧基,与水、乙醇分子间能形成氢键(或结构相似),故能溶于水、乙醇等溶剂,故A正确;
B、半胱氨酸中含有氨基,可与盐酸反应,含有羧基,可与NaOH溶液反应,故B正确;
C、高半胱氨酸与半胱氨酸结构相似,在分子组成上相差一个CH2原子团,故C正确;
D、半胱氨酸官能团不变的同分异构体有:巯基与氨基换位,巯基和氨基同在α-碳原子上或同在β-碳原子上。共有3种,故D错误。
故选D。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列各示意图与对应的表述正确的是( )
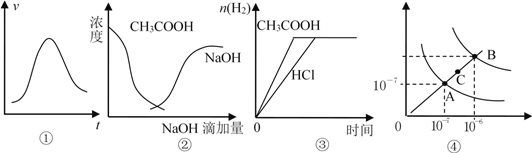
A. 图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应
B. 图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图
C. 图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化
D. 图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10.6 g Na2CO3溶解在10 mL水中,再稀释成1 L溶液,从中取出10 mL,这10 mL溶液的物质的量浓度为
A.0.1 mol·L-1B.1 mol·L-1C.0.01 mol·L-1D.10 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛被称为“21世纪金属”
(1)工业上用钛矿石(含FeTiO3,含FeO、Al2O3、SiO2等杂质)经过以下流程制得TiO2:
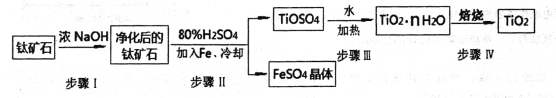
其中,步骤Ⅱ发生反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H20
①步骤I反生的化学方程式是______________________________若将所得FeSO4晶体溶于水,加热蒸干后所得的固体是_________________
②若步骤Ⅲ中是利用Ti4+在溶液中水解制得TiO2·nH2O,则该反应的离子方程式为_________________________________________________
(2)可利用TiO2通过下述两种方法制备金属钛:
方法一:将TiO2作阴极,石墨作阳极,熔融CaO为电解液,用炭块作电解槽池,电解TiO2制得钛,其阴极发生的反应:______________________________________。
方法二:通过以下反应制备金属钛
①TiO2(s)+2Cl2(g) ![]() TiCl4(g)+O2(g) △H=+151 KJ/mol
TiCl4(g)+O2(g) △H=+151 KJ/mol
②TiCl4+2Mg![]() 2MgCl2+Ti
2MgCl2+Ti
在实际生产中,需在反应①过程中加入碳才能顺利制得TiCl4,其原因是_________________________,______________________________________________。(两方面)
(3)若已知:C(s)+O2(g)=CO2(g) △H=-394 KJ/mol,则由固体TiO2、固体C与Cl2反应制取气态TiCl4的热化学方程式为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为:
![]()
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是 。
【设计、完成实验】(1)称取 g草酸晶体(H2C2O4·2H2O),配置500 mL 0.10 mol/L H2C2O4溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和 。
②下列操作会使所配溶液浓度偏低的是 (填下列选项的字母序号)。
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘 |
B.定容时俯视刻度线 |
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水 |
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容 |
(2)完成探究,记录数据
实验 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
0.10 mol/L | 等浓度 | H2O | 0.50 mol/L | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/LK2SO4溶液 | 18 |
则x = ,假设2成立
(3)由于KMnO4能氧化水中有机物等因素,为配制好稳定的KMnO4溶液,其浓度需标定。取10.00 mL 0.10 mol/L H2C2O4溶液于锥形瓶中,加入10 mL 0.50 mol/L稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00 mL,则草酸溶液与酸性KMnO4溶液反应的离子方程式为: 。上述实验中KMnO4溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于强弱电解质及非电解质的判断完全正确的是
选项 | A | B | C | D |
强电解质 | NaCl | CaCl2 | HNO3 | H2SO4 |
弱电解质 | CH3COOH | BaSO4 | AlCl3 | HF |
非电解质 | Cl2 | CO2 | SO2 | C2H5OH |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com