
����Ŀ������(H2C2O4)��Һ������KMnO4��Һ��Ӧʱ����Һ��ɫ����������죬ijѧϰС��̽����Ӧ������ʹ��ɫ�ӿ����Ҫԭ��������:
���������ϡ�KMnO4��Һ����H2C2O4�ķ�Ӧ����Ϊ��
![]()
��������衿����1:�÷�ӦΪ���ȷ�Ӧ
����2:��Ӧ���ɵ�Mn2���Ը÷�Ӧ�д�����
����3:K���Ը÷�Ӧ�д�����
��С��ͬѧδ���Ũ��ʹ��Ӧ���ʼӿ�ļ��裬ԭ���� ��
����ơ����ʵ�顿��1����ȡ g���ᾧ��(H2C2O4��2H2O)������500 mL 0.10 mol/L H2C2O4��Һ��
�������������б����õ���2�ֶ���������������ƽ�� ��
�����в�����ʹ������ҺŨ��ƫ�͵��� (������ѡ�����ĸ���)��
A����ȡ���ᾧ��ʱ�������ᾧ�����������ƽ���� |
B������ʱ���ӿ̶��� |
C�����ձ�����Һת�Ƶ�����ƿ֮ǰ������ƿ������������ˮ |
D��ҡ�Ⱥ�����ҺҺ����ڿ̶��ߣ������ý�ͷ�ιܼ�ˮ�ٶ��� |
��2�����̽������¼����
ʵ�� | �ձ��������Լ�������(mL) | �������� | ��Һ��ɫʱ��(s) | |||
0.10 mol/L | ��Ũ�� | H2O | 0.50 mol/L | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | ˮԡ�����¶�65 �� | 15 |
3 | 30 | 20 | 30 | 20 | ��������MnSO4���� | 3.6 |
4 | 30 | 20 | x | 20 | ����5 mL 0.10 mol/LK2SO4��Һ | 18 |
��x = ������2����
��3������KMnO4������ˮ���л�������أ�Ϊ���ƺ��ȶ���KMnO4��Һ����Ũ����궨��ȡ10.00 mL 0.10 mol/L H2C2O4��Һ����ƿ�У�����10 mL 0.50 mol/Lϡ���ᣬ�ã�2����KMnO4��Һ�ζ�����ƿ��ǡ�ó�dz��ɫ���Ұ���Ӳ���ɫ����¼���ݣ�ƽ������ʵ�飬ƽ������KMnO4��Һ40.00 mL���������Һ������KMnO4��Һ��Ӧ�����ӷ���ʽΪ�� ������ʵ����KMnO4��Һ�����ʵ���Ũ��Ϊ ��
���𰸡���������衿�淴Ӧ��Ũ�Ƚ��ͣ���Ӧ���ʼ���
����ơ����ʵ�顿��1��6.3 g ��500 mL����ƿ ��A��D ��2��25 mL
��3��5H2C2O4��2MnO4�� ��6H��=10CO2��2Mn2����8H2O 0.010 mol/L
�������������������������衿 ��Ϊ�淴Ӧ��Ũ�Ƚ��ͣ���Ӧ���ʼ�������ʵ���з�Ӧ�����Ǽӿ�ġ�
����ơ����ʵ�顿��1�����ᾧ�������="0.5��0.1��126=6.3" g �� ����ΪҪ����500������Һ������ѡ��500 mL����ƿ�� ��A����ΪҪ����6.3�˲��ᾧ�壬���������̣���ʵ�ʳ���������ƫ�ͣ�Ũ��ƫ�ͣ�B����������Һ�����С��Ũ��ƫ��C������ƿ����ˮ����Ӱ��Ũ�ȣ�D��ҡ�Ⱥ�Ӧ�ü�ˮ������ˮ����Ũ��ƫС������ѡA��D�� ��2����Ϊʵ����Ҫ������Һ��Ũ����ͬ�����Ի����Һ�������Ӧ��ȣ�������Ҫ����ˮ�����Ϊ25 mL����3�����ᱻ������������ɶ�����̼�����ӷ���ʽΪ��5H2C2O4��2MnO4�� ��6H��=10CO2��2Mn2����8H2O��������ص�Ũ��="5:(0.1��10)=2:(" 40��x) ��x="0.010" mol/L



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ñ�״����ij������ܶ�Ϊ1.97 g/L������������Է���������(����)
A. 16 B. 28 C. 44 D. 48
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������з�Ӧ��Fe+2Fe3+=3Fe2+ ��һ����ѧ���(�������ɵ��ߺ�һ��С���ݣ��缫���Ϻ͵��Һ��ѡ)������ʵ��װ��ͼ��ע���������Һ���ƺ����������ϣ����������������͵�������д���缫��Ӧʽ��������_____________��������__________��װ��ͼ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��L��M����Ԫ�ص�ԭ��������������X����������Y���ڲ��������ȣ�Yԭ�ӵ������������Ǵ�����������������Z��L�ǿ����к�����������Ԫ�أ�M�ǵؿ��к�����ߵĽ���Ԫ�ء��ش��������⣺
��1��X��L�γɵij��������ӵĵ���ʽΪ____________________��
��2��Z��X��Ԫ�ذ�ԭ����Ŀ��1:3��2:4���ɷ���A��B���õ���ʽ��ʾA���γɹ���______��B�Ľṹʽ_______________________��
��3����������������Ԫ�أ���Lͬһ���壬��ԭ�ӱ�Lԭ�Ӷ��������Ӳ㣬���������ڱ���λ��Ϊ_______________�������������ˮ����Ļ�ѧʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 mol HNO3��ϡ����ֱ��벻ͬ���������۷�Ӧ�����������������������ʵ����Ĺ�ϵ��ͼ��ʾ(��֪ϡ����Ļ�ԭ����ֻ��NO)���ش��������⣺
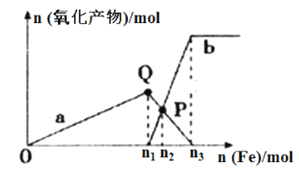
��1������a��ʾ_______________������b��ʾ_____________����дFe2+��Fe3+����
��2��P��ʱ�ܷ�Ӧ�����ӷ���ʽ�ɱ�ʾΪ_______________________��
��3��n3�Un2=________________����д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҷ��ְ��װ�������ǿ���̲�����Ⱦ�ߵ����������Կ��ư��̲�������������Ч����֪���װ���Ľṹ��ʽΪ �����й��ڰ��װ���˵������ȷ����
�����й��ڰ��װ���˵������ȷ����
A. ������ˮ���Ҵ����ܼ�
B. ���������ᡢ������NaOH��Һ��Ӧ
C. �� (�߰��װ���)��Ϊͬϵ��
(�߰��װ���)��Ϊͬϵ��
D. �����Ų����ͬ���칹����2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���Т�BaCl2���ڽ��ʯ����KOH����Na2SO4���ݸɱ�����Ƭ�������ʣ�������Ҫ��ش�
(1)�ۻ�ʱ����Ҫ�ƻ���ѧ������________(��д���ʵ���ţ���ͬ)���ۻ�ʱ��Ҫ�ƻ����ۼ�����________��
(2)�������ӻ��������______________��ֻ�����Ӽ���������________��
(3)�ٵĵ���ʽ��______________���ݵĵ���ʽ��_____________��
II��������(���ӻ�����)������18�����ӣ�
���� | A�� | B2�� | C | D | E | F |
����ص� | �������� | �����˫�˷��� | ���ʣ� ˫�˷��� | ��������˷��� | ����� �ĺ˷��� | |
��ش��������⣺
(1)A��Ԫ�ط�����____________��B2���Ľṹʾ��ͼ��________��
(2)C�ĽṹʽΪ__________����֪D�ĵ�����ˮ��Ӧ������������һ���ᣬд���÷�Ӧ�Ļ�ѧ����ʽ��________________________________________
(3)E�ĵ���ʽ��____________________��F��ˮ��Һ��������������F�Ļ�ѧʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����塣�ش��������⣺
I.CO�����ڸ�¯��������֪
Fe3O4(s)+4CO(g)====3Fe(s)+4CO2(g) ��H1 =a kJ/ mol
3Fe2O3(s)+CO(g)====2Fe3O4 (s)+CO2(g) ��H2=bkJ/mol
��ӦFe2O3(s)+3CO(g)====2Fe(s)+3CO2(g)����H3=_________kJ/mol(�ú�a��b�Ĵ���ʽ��ʾ)
��.һ�������£�CO2��CO���Ի���ת����
��1��ij�¶��£����ݻ�Ϊ2L���ܱ��������ס������ַ�ʽͶ�뷴Ӧ�����Ӧ��CO2(g)+H2(g) ![]() CO(g)+H2O(g)��
CO(g)+H2O(g)��
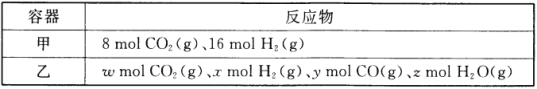
������15min��ﵽƽ�⣬��ʱCO2��ת����Ϊ75%����0~15min��ƽ����Ӧ����v(H2)= _________���������¸÷�Ӧ��ƽ�ⳣ��K=_________��
��ʹƽ������������ͬ�����������������ȣ����ء�x��y��z������Ĺ�ϵ��_________����_________ (�ú�y�ĵ�ʽ��ʾ)��
��2���о��������¶ȡ�ѹǿ�Է�Ӧ��C6H5CH2CH3(g)+CO2(g) ![]() C6H5CH=CH2(g)+CO(g)+H2O(g) ��H�����ұ���ƽ��ת����Ӱ������ͼ��ʾ��
C6H5CH=CH2(g)+CO(g)+H2O(g) ��H�����ұ���ƽ��ת����Ӱ������ͼ��ʾ��

����H_________ 0(����>����<������=��)��ѹǿp1��p 2��p3�Ӵ�С��˳����_________��
��3��CO�ɱ�NO2������CO+NO2![]() CO2+NO�����¶ȸ���225��ʱ����Ӧ����v��=k����c(CO)��c(NO2)��v��=k����c(CO2)��c(NO)��k����k���ֱ�Ϊ�����淴Ӧ���ʳ������������¶ȷ�Χ�ڣ�k����k����÷�Ӧ��ƽ�ⳣ��K֮��Ĺ�ϵΪ_________��
CO2+NO�����¶ȸ���225��ʱ����Ӧ����v��=k����c(CO)��c(NO2)��v��=k����c(CO2)��c(NO)��k����k���ֱ�Ϊ�����淴Ӧ���ʳ������������¶ȷ�Χ�ڣ�k����k����÷�Ӧ��ƽ�ⳣ��K֮��Ĺ�ϵΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4HCl(g)��O2(g)![]() 2Cl2(g)��2H2O(g)�У�4 mol HCl���������ų�115.6 kJ����������֪��
2Cl2(g)��2H2O(g)�У�4 mol HCl���������ų�115.6 kJ����������֪��![]() ���ж�����˵����ȷ����( )
���ж�����˵����ȷ����( )
A. �÷�Ӧ�Ħ�H����115.6 kJ��mol��1
B. �Ͽ�1 mol H��O ����Ͽ�1 mol H��Cl �������������ԼΪ32 kJ
C. H2O��H��O ����HCl��H��Cl����
D. �����ṩ�����ж���Ԫ�صķǽ����Ա���Ԫ��ǿ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com