
【题目】含1 mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO),回答下列问题:
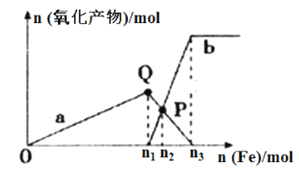
(1)曲线a表示_______________;曲线b表示_____________(填写Fe2+或Fe3+)。
(2)P点时总反应的离子方程式可表示为_______________________。
(3)n3︰n2=________________(请写出计算过程)。
【答案】Fe3+ Fe2+ 6Fe+20H++5NO3-=3Fe2++3Fe3++5NO↑+10H2O 5:4
【解析】
铁与稀硝酸反应生成硝酸铁、NO和水,铁过量时硝酸铁与铁反应生成硝酸亚铁,结合反应的图像分析解答。
(1)向稀硝酸中加入铁粉时,发生两个过程,开始先生成Fe(NO3)3,反应方程式为Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O,Fe(NO3)3与过量的铁继续反应生成Fe(NO3)2,反应方程式为2Fe(NO3)3+Fe=3Fe(NO3)2,因此曲线a表示Fe3+,曲线b表示Fe2+。
(2)P点时铁离子与亚铁离子的物质的量相等,则根据电子得失守恒、原子守恒和电荷守恒可知总反应的离子方程式可表示为6Fe+20H++5NO3-=3Fe2++3Fe3++5NO↑+10H2O。
(3)向稀硝酸中加入铁粉时,发生两个过程,开始先生成Fe(NO3)3,反应方程式为Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O,根据硝酸的物质的量为1mol利用方程式可计算出生成的Fe(NO3)3为0.25mol,所以参加反应的铁为0.25mol即n1=0.25,将0.25mol的Fe(NO3)3转化为Fe(NO3)2需要的金属铁是0.125mol,所以n3=0.25mol+0.125mol=0.375mol。根据6Fe+20H++5NO3-=3Fe2++3Fe3++5NO↑+10H2O可知n2=0.3mol,则n3:n2=5:4。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】实验室中保存下列化学药品的方法正确的是( )
A.硝酸银晶体保存在棕色试剂瓶中B.固体烧碱保存在橡胶塞细口试剂瓶中
C.白磷保存在玻璃塞广口瓶中D.浓盐酸可存放在敞口容器中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1盐酸溶液的烧杯中,该铝片与盐酸反应产生氢气的速率与反应时间的关系可用下图所示的坐标曲线来表示,

回答下列问题:
(1)曲线O→a段不产生氢气的原因,用化学方程式解释为_______________________________________________;
(2)曲线b→c段产生氢气的速率增加较快的主要原因是___________________________________________;
(3)向溶液中加入下列物质,能加快上述化学反应速率的是_________。
A.蒸馏水 B.改用铝粉 C.饱和氯化钠溶液 D.浓盐酸 E.少量硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过一步反应不能直接完成的是
①N2→NO2 ②NO2→NO ③NH3→NO ④NO→HNO3 ⑤Cu→Cu(NO3)2 ⑥HNO3→NO2
A. ①⑤B. ①C. ①④⑥D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为:
![]()
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是 。
【设计、完成实验】(1)称取 g草酸晶体(H2C2O4·2H2O),配置500 mL 0.10 mol/L H2C2O4溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和 。
②下列操作会使所配溶液浓度偏低的是 (填下列选项的字母序号)。
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘 |
B.定容时俯视刻度线 |
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水 |
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容 |
(2)完成探究,记录数据
实验 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
0.10 mol/L | 等浓度 | H2O | 0.50 mol/L | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/LK2SO4溶液 | 18 |
则x = ,假设2成立
(3)由于KMnO4能氧化水中有机物等因素,为配制好稳定的KMnO4溶液,其浓度需标定。取10.00 mL 0.10 mol/L H2C2O4溶液于锥形瓶中,加入10 mL 0.50 mol/L稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00 mL,则草酸溶液与酸性KMnO4溶液反应的离子方程式为: 。上述实验中KMnO4溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或实验操作不正确的是( )

A. 用图1所示装置制取少量的氨气
B. 用图2装置可以完成“喷泉”实验
C. 用图3所示装置收集SO2
D. 可用加热浓氨水制氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能大量共存的离子组是
A.NH4+、Mg2+、OH-、Cl- B.Ba2+、K+、SO42-、NO3-
C.Al3+、Cu2+、SO42-、Cl- D.Na+、Al3+、Cl-、AlO2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com