
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
A. 升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B. 0.l0mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C. CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D. 室温下,欲使0.1mol/L醋酸溶液的pH,电离度a都减小,可加入少量水
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是( )
A. 碳酸钙与盐酸反应: CaCO3+2H+===CO2↑+H2O+ Ca2+
B. 硫酸和氢氧化钡溶液反应: 2OH- + Ba2++2H++SO![]() ===BaSO4↓+2H2O
===BaSO4↓+2H2O
C. 铁钉放入硫酸铜溶液中: 2Fe+3Cu2+===2Fe3++3Cu
D. 钠与水反应: 2Na+2H2O ===2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增。已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,Q、R两种元素组成的原子个数比为1:1的化合物N是中学化学中常见的有机溶剂;
⑤Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同。
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)化合物M的空间构型为______________ ,其中心原子采取_________杂化;化合物N在固态时的晶体类型为_______________。
(2)R、X、Y三种元素的第一电离能由小到大的顺序为___________。
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为__________(写分子式)。
(4)由R、X、Y三种元素组成的RXY-离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物质。该反应的离子方程式为______________________________。
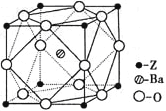
(5)Z原子基态时的外围电子排布式为_________________;Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个Z原子等距离且最近的氧原子数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
钒及其化合物在科学研究中和工业生产中具有许多用途。
(1)基态钒原子的核外价电子排布式为________。
(2)钒有+2、+3、+4、+5等几种化合价。这几种价态中,最稳定的是______。
(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。例举与VO43-空间构型相同的一种阳离子__________(填化学式)。
(4)钒(Ⅱ)的配离子有[V(CN)6]4-、[V(H2O)6]2+等。
①CN-与N2互为等电子体,CN-中σ键和Π键数目比为________。
②对H2O与V2+形成[V(H2O)6]2+过程的描述不合理的是______________。
a.氧原子的杂化类型发生了变化
b.微粒的化学性质发生了改变
c.微粒中氢氧键(H-O)的夹角发生了改变。
d.H2O与V2+之间通过范德华力相结合。
③在[V(H2O)6]2+中存在的化学键有___________。
a.金属键 b.配位键 c. σ键 d.Π键 f. 氢键
(5)已知单质钒的晶胞如图,则V原子的配位数是_______,假设晶胞的边长为d nm,密度ρ g·cm-3,则钒的相对原子质量为_______________。(设阿伏伽德罗常数为NA)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】80 ℃时,2 L 密闭容器中充入0.40 mol N2O4,发生反应N2O4![]() 2NO2 △H =+Q kJ/mol(Q>0),获得如下数据:下列判断正确的是
2NO2 △H =+Q kJ/mol(Q>0),获得如下数据:下列判断正确的是
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
A. 升高温度该反应的平衡常数K减小
B. 20~40 s 内,v(N2O4)=0.002 mol/( Ls)
C. 反应达平衡时,吸收的热量为0.30 Q kJ/mol
D. 100s 时再通入0.40 mol N2O4,达新平衡时N2O4的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】做中和热测定实验时,所用仪器的正确组合是
①容量瓶 ②量筒 ③酒精灯 ④天平 ⑤环形玻璃搅拌棒 ⑥试管 ⑦烧杯 ⑧温度计
A.②⑤⑦⑧B.②③④⑦C.①②⑤⑦⑧D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,生成的有机物只有一种的是
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2-氯丁烷(![]() )与NaOH乙醇溶液共热发生消去HCl分子的反应
)与NaOH乙醇溶液共热发生消去HCl分子的反应
C. 甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应
D. 新戊烷和氯气发生取代反应生成一氯取代物的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对羟基苯甲醛,俗称PHBA,是一种重要的有机化工原料。其结构为![]() 。有人提出,以对甲基苯酚为原料合成PHBA的途径如下:
。有人提出,以对甲基苯酚为原料合成PHBA的途径如下:
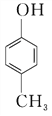
![]() CH3OCH3
CH3OCH3
![]() C
C
![]() D
D![]() E
E![]() PHBA
PHBA
已知:![]()
(1)PHBA的官能团的名称为________。
(2)下列有关PHBA的说法正确的是________。
A.PHBA的分子式为C7H6O2
B.PHBA是一种芳香烃
C.1 mol PHBA最多能与4 mol H2反应
D.PHBA能与NaHCO3溶液反应生成CO2
(3)上述反应中属于取代反应的是________。
(4)反应③的化学方程式为____________________________。
(5)该合成途径中的反应①⑤的作用为_________________。
(6)E有多种同分异构体,符合以下所有特征的同分异构体的结构简式为__________________(只写一种)。
a.苯环上存在2种不同化学环境的氢原子,且个数比为1∶2
b.遇FeCl3溶液显示特征颜色
c.能使溴的四氯化碳溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com