
【题目】某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下。
[实验目的] 测量锌和稀硫酸反应的速率。
[实验用品] 锥形瓶、双孔塞、分液漏斗、直角导管、50 mL注射器、铁架台、秒表、锌粒、1 mol·L-1的H2SO4、4 mol·L-1的H2SO4。
[实验步骤]
(1)甲同学取一套如图装置,加入40 mL 1 mol·L-1的H2SO4,测量收集10 mL H2所需的时间。

(2)乙同学取另一套同样的装置,加入40 mL 4 mol·L-1的H2SO4,测量收集10 mL H2所需的时间。
回答下列问题:
(1)Zn与稀H2SO4反应的离子方程式为________。
(2)收集10 mL H2所需时间:甲________(填“大于”“小于”或“等于”)乙。反应速率:甲________(填“大于”“小于”或“等于”)乙。
(3)下列说法正确的是________(填字母)。
A 本实验中甲、乙两同学所用锌粒的表面积要相同
B 装置气密性要好
C 40 mL的H2SO4要迅速加入
D 测量气体体积还可以用排水法
E 若用98%的浓H2SO4,则反应最快
(4)测定Zn和稀H2SO4反应的速率还可用的方法有:①___________; ②_________。
【答案】Zn+2H+=Zn2++H2↑ 大于 小于 ABCD 测定等质量的Zn完全溶解所需要的时间 单位时间内H2SO4浓度的变化
【解析】
(1)金属活动顺序表中排在氢前面的金属可从非强氧化性酸中置换出氢,金属锌可以和硫酸反应生成硫酸锌和氢气,据此书写离子方程式;
(2)浓度越大,反应速率越快,反应产生等量的气体需要的时间越短;
(3)A.研究浓度对反应速率的影响,本实验中所用锌粒的表面积要相同,根据控制变量法来回答;
B.根据测量收集10mL H2所需的时间,要求生成的氢气体积测定必须准确;
C.40mL的H2SO4要迅速加入,防止气体的体积测定误差的出现;
D.氢气的收集可以用排水法收集;
E.若用98%的浓H2SO4,金属和浓硫酸的反应产物是二氧化硫,不是氢气;
(4)可通过测定测量等质量的Zn完全溶解所需要的时间、单位时间内H2SO4浓度的变化、收集等体积H2需要的时间长短等角度判断。
(1)金属锌在金属活动顺序表中排在氢的前面,可以和硫酸反应生成硫酸锌和氢气,离子方程式为:Zn+2H+=Zn2++H2↑;
(2)1molL-1的H2SO4浓度小于4molL-1的H2SO4的,浓度越大,反应速率越快,反应产生等量的气体需要的时间越短;
(3)A.研究浓度对反应速率的影响,本实验中所用锌粒的表面积要相同,故A正确;
B.根据测量收集10mL H2所需的时间,要求生成的氢气体积测定必须准确,气密性必须好,故B正确;
C.40mL的H2SO4要迅速加入,防止气体的体积测定误差的出现,故C正确;
D.氢气不溶于水,收集可以用排水法收集,故D正确;
E.若用98%的浓H2SO4,金属和浓硫酸的反应产物是二氧化硫,不是氢气,故E错误;
故答案为:ABCD;
(4)测定Zn和稀H2SO4反应的速率,测定反应物的变化,可通过测量等质量的Zn完全溶解所需要的时间; 单位时间内H2SO4浓度的变化,测定生成物,可通过收集等体积H2需要的时间长短。


科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )

A.反应2NO(g)+O2(g)==2NO2(g)的ΔH>0
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380 ℃下,c起始(O2)=5.0×10-4 mol·L-1,NO平衡转化率为50%,则平衡常数K=2000
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol·L-1 NaOH溶液滴定20.00mL 0.1000 mol·L-1某酸(HA)溶液,溶液中HA、A-的物质的量分数δ(X)随pH的变化如图所示。[已知δ(X)=![]() ]下列说法正确的是
]下列说法正确的是
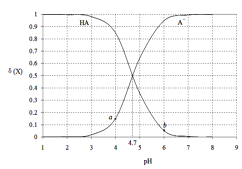
A.Ka(HA)的数量级为10-5
B.溶液中由水电离出的c(H+):a点>b点
C.当pH=4.7时,c(A-)+c(OH-)=c(HA)+c(H+)
D.当pH=7时,消耗NaOH溶液的体积为20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭烧瓶中注入NO2,在25℃时建立下列平衡:2NO2![]() N2O4(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列情况:①颜色,②平均相对分子质量,③质量,④压强,⑤密度。其中不变的是
N2O4(正反应为放热反应),若把烧瓶置于100℃的沸水中,下列情况:①颜色,②平均相对分子质量,③质量,④压强,⑤密度。其中不变的是
A. ②④ B. ③④ C. ③⑤ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度和压强下,在容积为VL的密闭容器中充入1 mol A和1 mol B,保持恒温恒压下反应:A(g)+B(g)![]() C(g) ΔH<0。达到平衡时,C的体积分数为40%。试回答有关问题:
C(g) ΔH<0。达到平衡时,C的体积分数为40%。试回答有关问题:
(1)升温时,C的反应速率________(填“加快”“减慢”或“不变”)。
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡________(填字母)。
A 一定向正反应方向移动 B 一定向逆反应方向移动
C 一定不移动 D 不一定移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) ![]() 2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
温度/体积分数/压强 | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | B |
915 | c | 75.0 | D |
1000 | E | f | 83.0 |
①b<f ②915 ℃、2.0 MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1 000 ℃)>K(810 ℃) 上述①~④中正确的 ( )
A.①②B.②③C.②③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.稀氨水中存在平衡:NH3 + H2O![]() NH4+ + OH- ,如进行下列操作,则下列物理量如何变化?试用“增大”‘减小”“不变”填写。
NH4+ + OH- ,如进行下列操作,则下列物理量如何变化?试用“增大”‘减小”“不变”填写。
(1)通适量HCl气体时,c(NH3)____________,c(OH-)__________________
(2)加入NH4Cl晶体时,c(NH4+)___________,平衡常数K_______________
Ⅱ.已知室温时,0.1 mol·L-1的某一元酸HA在水中有 0.1% 发生电离,回答下列各问题:
(1)该溶液的pH=________。
(2)HA的电离平衡常数K=________。
(3) 若在95℃时,上述溶液中水电离的H+浓度为____________(此时KW=10-12)。
Ⅲ.常温下有pH为12的NaOH溶液20 mL,加入某溶液,将其pH变为11(设溶液体积可直接相加;计算结果保留到小数点后一位)。
(1)若用pH = 10的NaOH溶液,应加入NaOH溶液_________mL;
(2)若用pH = 2的盐酸,应加入盐酸___________mL;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表格中的各种情况,可以用对应选项中的图像表示的是
选项 | 反应 | 甲 | 乙 |
A | 外形、大小相近的金属和水反应 | Na | K |
B | 4mL0.01mol·L-1 KMnO4溶液分别和不同浓度的2mLH2C2O4(草酸)溶液反应 | 0.1mol·L-1的H2C2O4溶液 | 0.2mol·L-1的H2C2O4溶液 |
C | 5mL0.1mol·L-1Na2S2O3溶液和5mL0.1mol·L-1H2SO4溶液反应 | 热水 | 冷水 |
D | 5mL4%的过氧化氢溶液分解放出O2 | 无MnO2粉末 | 加MnO2粉末 |
A.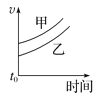 B.
B.
C. D.
D.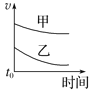
查看答案和解析>>
科目:高中化学 来源: 题型:
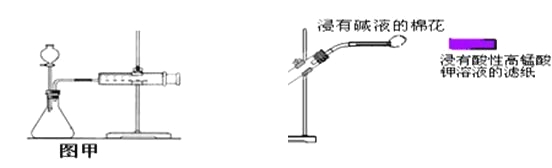
【题目】下列实验的相关描述正确的是( )
A.快速分离氢氧化铁胶状沉淀和氯化钠溶液可用抽滤法
B.常温下,苯酚与水形成的浊液静置后会分层,上层为溶有水的苯酚溶液
C.甲装置可用于某些化学反应速率的测定。该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离后松手,观察针筒是否能回到原来刻度处
D.用氢氧化钠滴定醋酸实验,酸式滴定管没有润洗就直接使用则所得待测液浓度偏高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com