
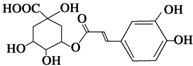
 预防和治疗甲型H1N1流感的中草药中都含有金银花.绿原酸是金银花的活性成分之一,具有广泛的抗菌及抗病毒作用.有关绿原酸的说法错误的是( )
预防和治疗甲型H1N1流感的中草药中都含有金银花.绿原酸是金银花的活性成分之一,具有广泛的抗菌及抗病毒作用.有关绿原酸的说法错误的是( )| A、绿原酸的分子式为C16H18O9 |
| B、1 mol绿原酸最多可与5 mol H2发生反应 |
| C、绿原酸中含氧官能团有羧基、羟基和酯基 |
| D、绿原酸酸性条件下水解后所得两产物碳原子数之差为2 |


科目:高中化学 来源: 题型:
| A、石油分馏时把温度计插入液面下 |
| B、向银氨溶液中加入几滴乙醛后用酒精灯加热至沸制银镜 |
| C、在试管内加入少量蔗糖溶液,再加3-5mL稀硫酸小心煮沸几分钟后冷却,加新制Cu(OH)2,煮沸,有红色沉淀生成 |
| D、用乙醇、醋酸和18mol/L的硫酸混合加热制乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
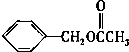 乙酸苯甲酯的结构简式如图,它有很多种同分异构体,其中含有酯基的一取代苯结构的同分异构体,除所给出的乙酸苯甲酯外,还有多少种( )
乙酸苯甲酯的结构简式如图,它有很多种同分异构体,其中含有酯基的一取代苯结构的同分异构体,除所给出的乙酸苯甲酯外,还有多少种( )| A、3 | B、4 | C、5 | D、6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com