
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”(结构式中用“*”加以标注)。凡有一个手性碳原子的物质一定具有光学活性。物质: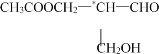 有光学活性,当它发生下列反应后生成的有机物中仍有光学活性的是( )
有光学活性,当它发生下列反应后生成的有机物中仍有光学活性的是( )
A.与乙酸发生酯化反应
B.与NaOH水溶液共热
C.在催化剂存在下与H2反应
D.与新制的Cu(OH)2悬浊液共热
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】为探究NO与铜粉的反应,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2。
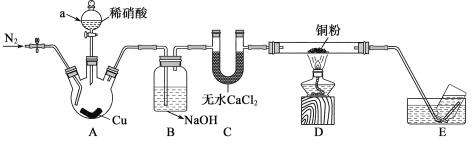
回答下列问题:
(1)通入N2的作用:_____________,仪器A的名称_____________。
(2)A中发生反应的离子方程式:_______________
(3)B中NaOH的作用__________________________。
(4)D中有__________________________现象,即可证明NO与Cu反应。
(5)NO可被Ce4+氧化,制得NH4NO3产品,流程如下(Ce为铈元素)。
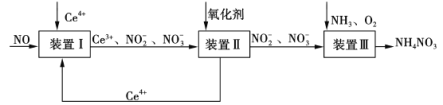
①装置Ⅰ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,写出生成等物质的量的NO3-和NO2-的离子方程式:________________。
②已知进入装置Ⅲ溶液中NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,至少需通入标况下的O2________L(用含a代数式表示,结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
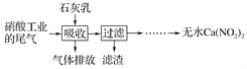
(1)一定条件下,NO与NO2可以生成一种新的氧化物,试写出该反应的化学方程式:___。
(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底部进入,石灰乳从吸收塔顶部喷淋),其目的是__;滤渣可循环使用,滤渣的主要成分是__(填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1∶1。
若n(NO)∶n(NO2)>1∶1,则会导致__;
若n(NO)∶n(NO2)<1∶1,则会导致__。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用系统命名法命名有机物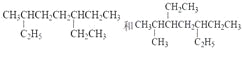 ,主链碳原子数均为7 个
,主链碳原子数均为7 个
B.![]() 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂
能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂
C.蛋白质和油脂都属于高分子化合物,一定条件下能水解
D.1mol 绿原酸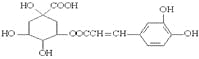 通过消去反应脱去1 molH2O时,能得到6 种不同产物(不考虑立体异构)
通过消去反应脱去1 molH2O时,能得到6 种不同产物(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )
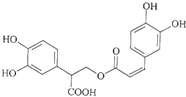
A.迷迭香酸可以发生水解反应、取代反应和酯化反应
B.1mol迷迭香酸最多能和8mol氢气发生加成反应
C.1mol迷迭香酸与NaOH的水溶液完全反应时最多消耗5molNaOH
D.迷迭香酸属于芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是化学实验室中最常见的有机物,其产量可以用来衡量一个国家的石油化工发展水平,还是一种植物生长调节剂。A和HCl反应生成B,B与烧碱溶液生成C,C氧化D,D能发生银镜反应,D氧化成E,C和E生成具有果香味的化合物F,请写出有关反应方程式,并在( )中写明反应类型
(1)A→B:___,(________);
(2)C→D:___,(________);
(3)D与新制Cu(OH)2反应:___,(_______);
(4)C+E→F:___,(________)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中,甲由C、H、O三种元素组成,元素的质量比为12:3:8,甲的沸点为78.5℃,其蒸气与H2的相对密度是23。将温度控制在400℃以下,按要求完成实验。

(1)在通入空气的条件下进行实验,加入药品后的操作依次是___。(填序号)
a.打开活塞
b.用鼓气气球不断鼓入空气
c.点燃酒精灯给铜丝加热
(2)实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,实验现象为___。
(3)现用10%的NaOH溶液和2%的CuSO4溶液,制取本实验所用试剂Cu(OH)2,请简述实验操作___。。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
①CH3—CH=CH2和CH2=CH2的最简式相同
②CH≡CH和C6H6含碳量相同
③丁二烯和丁烯为同系物
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤标准状况下,11.2 L的庚烷所含的分子数为0.5NA(NA为阿伏加德罗常数)
⑥能够快速、微量、精确地测定相对分子质量的物理方法是核磁共振谱法
A.①⑤⑥B.②③④C.③⑤⑥D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备合成气的工艺主要是水蒸气重整甲烷: CH4(g)+H2O(g)CO(g)+3H2(g) ΔH>0,在一定条件下,向体积为1L的密闭容器中充入1 molCH4(g)和1molH2O(g),测得 H2O(g)和 H2(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )
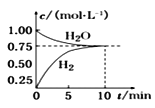
A.达到平衡时,CH4(g)的转化率为75%
B.0~10 min内,v(CO)=0.075 mol·L-1·min -1
C.该反应的化学平衡常数K=0.1875
D.当CH4(g)的消耗速率与H2(g)的消耗速率相等时,反应到达平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com