
����Ŀ������Ԫ�غ�����Ԫ���������������к���Ҫ�ĵ�λ��
��1��д������Ԫ��Ga�Ļ�̬ԭ�Ӻ�������Ų�ʽ
��2��NF3�ķ��ӹ���Ϊ �� NO3���Ŀռ乹��Ϊ �� 1mol NO3���к��еĦҼ�����ĿΪ�� ��
��3��������������ᾧ�ı��屻��Ϊ����֪����Ӳ�����ʣ�BN�ľ���ṹ����ʯ���ƣ�����Bԭ�ӵ��ӻ���ʽΪ
��4��Ԫ�ص�һ�����ܵĴ�С��As���������������=����Ga��ԭ���� ��
��5����ͬ�����£���ˮ�е��ܽ�ȣ�NH3���������������=����PH3 �� ԭ���� ��
��6����֪�����黯�ؾ����Ľṹ��ͼ��ʾ���侧���߳�Ϊc pm�����黯�صĻ�ѧʽΪ �� ������Asԭ�Ӻ��������Gaԭ��֮��ľ���Ϊpm���ú�c��ʽ�ӱ�ʾ�����黯�ص��ܶ�Ϊgcm��3����NAΪ����٤��������ֵ���ú�c��NA��ʽ�ӱ�ʾ��ԭ������Ga��70��As��75���� 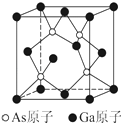
���𰸡�
��1��1s22s22p63s23p63d104s24p1
��2�������Σ�ƽ�������Σ�3NA
��3��sp3
��4������As��Gaλ��ͬһ���ڣ��ֱ�Ϊ��A���A�壬As��p������ڰ�������ȶ�״̬���ʵ�һ�����ܣ�As��Ga
��5������NH3������ˮ����֮���ܹ��γ����
��6��GaAs��![]() ��
��![]()
���������⣺��1��GaԪ��ԭ�Ӻ��������Ϊ31����������Ų�ʽΪ��1s22s22p63s23p63d104s24p1 �� ���Դ��ǣ�1s22s22p63s23p63d104s24p1����2��NF3��Nԭ�ӹµ��Ӷ���= ![]() =1���۲���Ӷ���=3+1=4��Ϊ�����Σ�NO3����Nԭ�ӹµ��Ӷ���=
=1���۲���Ӷ���=3+1=4��Ϊ�����Σ�NO3����Nԭ�ӹµ��Ӷ���= ![]() =0���۲���Ӷ���=3+0=3��Ϊƽ�������Σ�1mol NO3���к���3mol �Ҽ���������3NA���Ҽ���
=0���۲���Ӷ���=3+0=3��Ϊƽ�������Σ�1mol NO3���к���3mol �Ҽ���������3NA���Ҽ���
���Դ��ǣ������Σ�ƽ�������Σ�3NA����3��BN�ľ���ṹ����ʯ���ƣ�Bԭ����Nԭ��֮���γ�4��B��N������1��Ϊ��λ�������ӻ������ĿΪ4����Bԭ�Ӳ�ȡ�ӻ���
���Դ��ǣ�sp3����4��As��Gaλ��ͬһ���ڣ��ֱ�Ϊ��A���A�壬As��p������ڰ�������ȶ�״̬���ʵ�һ�����ܣ�As��Ga��
���Դ��ǣ�����As��Gaλ��ͬһ���ڣ��ֱ�Ϊ��A���A�壬As��p������ڰ�������ȶ�״̬���ʵ�һ�����ܣ�As��Ga����5��NH3������ˮ����֮���ܹ��γ��������ˮ�е��ܽ�ȣ�NH3��PH3 ��
���Դ��ǣ�����NH3������ˮ����֮���ܹ��γ��������6�������к���Gaԭ����Ϊ8�� ![]() +6��
+6�� ![]() =4��Asԭ����ĿΪ4���ʻ�ѧʽΪGaAs��
=4��Asԭ����ĿΪ4���ʻ�ѧʽΪGaAs��
Asԭ������Χ��4��Gaԭ���γ��������壬Asԭ���뾧������Gaԭ�����ߴ��ھ�����Խ����ϣ���Gaԭ����Asԭ��֮��ľ���Ϊ������Խ��߳��ȵ� ![]() �������Ծ�������Խ���Ϊ�����ⳤ��
�������Ծ�������Խ���Ϊ�����ⳤ�� ![]() ������Gaԭ����Asԭ��֮��ľ���Ϊ
������Gaԭ����Asԭ��֮��ľ���Ϊ ![]() pm��
pm��
��������Ϊ4�� ![]() g�����ܶ�Ϊ4��
g�����ܶ�Ϊ4�� ![]() g�£�c��10��10 cm��3=
g�£�c��10��10 cm��3= ![]() gcm��3 ��
gcm��3 ��
���Դ��ǣ�GaAs�� ![]() ��
�� ![]() ��
��


 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£���ƿ����������ԭ������һ����ȵ��ǣ� ��
A.ͬ��������ͬ�ܶȵ�C2H4��C3H6
B.ͬ��������ͬ�����CO��N2
C.ͬ�����ͬ�ܶȵ�N2O��CO2
D.ͬѹǿ��ͬ�����CO2��SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ϩ�ͱ��������У��������
A. ��ϩ��ʹ���Ը��������Һ��ɫ
B. ��ϩ����ȼ��
C. ����ʹ���Ը��������Һ��ɫ
D. ������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ӷ���ʽ��д�ɻ�ѧ����ʽ����ȷ����(����)
A. Cu2����2OH��===Cu(OH)2�� CuCO3��2NaOH===Cu(OH)2����Na2CO3
B. CO![]() ��2H��===H2O��CO2�� BaCO3��2HCl===BaCl2��H2O��CO2��
��2H��===H2O��CO2�� BaCO3��2HCl===BaCl2��H2O��CO2��
C. Ca2����CO![]() ===CaCO3�� Ca(OH)2��BaCO3===CaCO3����Ba(OH)2
===CaCO3�� Ca(OH)2��BaCO3===CaCO3����Ba(OH)2
D. H����OH��===H2O 2KOH��H2SO4===K2SO4��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʰ������������[��ѧʽΪ��NH2CH2COO��2Fe]�dz��õIJ���������ϳɷ������£� 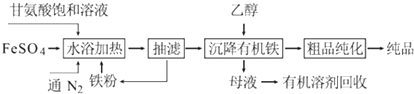
��1��ͨ��N2�������� ��
��2����֪�ʰ����������ԣ���ṹ��ʽΪNH2CH2COOH���ʰ������������������ˮ����ˮ���ѵ��룬д����ˮԡ���ȡ����������ɸʰ������������ķ�Ӧ�����ӷ���ʽ
��3�����˵ĺô��� �� �ӡ�ĸҺ���л����л��ܼ��ķ����� ��
��4������Ʒ�������IJ���Ϊ����ˮϴ�ӡ�ϴ�ӡ�������и������ʹ�õ��豸���ѡ�������ѹ�����������ո����������
��5��������ָ�������ڡ�ˮԡ���ȡ�������Ͷ��������ʯ��ʯ������ͬʱ��߲�Ʒ�IJ��ʺʹ��ȣ������ԭ�� ��
��6�����ʰ����Ͷ����Ϊ300kg��������Ʒ346.8kg�������Ϊ �� ���ʰ������Է�������Ϊ75��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����з�Ӧ�Ļ�ѧ����ʽ����д���÷�Ӧ���ں��ַ�Ӧ���ͣ�
��1����ϩʹ��ˮ��ɫ��
��2������Ũ�����Ũ����Ļ��Һ������
��3��������ϩ�ƾ�����ϩ��
��4��������Cl2�ڹ���������1��1��Ӧ��
��5��3������1����Ȳ��������Ȼ�̼��Һ�����ʵ���Ϊ1��1��Ӧ��
��6���ױ���Ũ���ᡢŨ��������TNT��
��7������ϩ������������Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��д��ȷ���ǣ���H�ľ���ֵ����ȷ���� ��
A.C��s��+ ![]() O2��g���TCO��g����H=��110.5KJmol��1��ȼ���ȣ�
O2��g���TCO��g����H=��110.5KJmol��1��ȼ���ȣ�
B.C2H5OH+3O2�T2CO2+3H2O��H=��1368.8KJmol��1����Ӧ�ȣ�
C.2NaOH��aq��+H2SO4��aq���TNa2SO4��aq��+2H2O ��l����H=��114.6KJmol��1���к��ȣ�
D.2H2O��g���T2H2��g��+O2��g����H=+483.6KJmol��1����Ӧ�ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 0.2 mol��L -1ij���������� Rn+������Һ 40mL��ǡ�ý� 20 mL 0.4 mol��L -1���������е������������ȫ�������� n ֵΪ�� ��
A. 1 B. 2 C. 3 D. 4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ��֤��SO2��Cl2��Ư���ԣ��������ͼ��ʾ��ʵ��װ����

��1��ʵ�����Ʊ�Cl2�����ӷ���ʽ��_____________________________��Ӧѡ����ͼA��Eװ���е�______������ţ���Cl2����Ӧ��Ũ���������ֳ���������_________________��
��2����Ӧ��ʼ����B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ����B��D�����Թ��е�Һ����ȣ�B�Թ��е�������___________________________________��
��3��װ��C��������____________________________________��
��4����������ͬѧ�ֱ�������ͼ��ʾװ��̽���������尴��ͬ������Ϻ��Ư���ԡ��Է�����

�����������Ʒ����Һ֮ǰ���Ƚ�SO2��Cl2ͨ��ʢ��Ũ����װ�õ�Ŀ����_____________________��
����ͬѧ��ʵ������з�����ͨ��һ��ʱ���Ʒ����Һ��������ɫ����ԭ����������Ӧ�����ӷ���ʽ������____________
����ͬѧ��ʵ������з�����ͨ��һ��ʱ���Ʒ����Һ��ɫ��ʱ�����Ʊ��Խ��Խdz��ԭ����_______________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com