
| A、上述反应中,每消耗2mol NO2,就会生成22.4L N2O |
| B、CO2是氧化产物,且为H2CO3的酸酐 |
| C、等质量的N2O和CO2含有相等的电子数 |
| D、N2O会迅速与人体血红蛋白结合,使人中毒 |


科目:高中化学 来源: 题型:
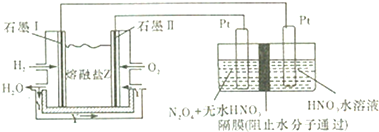
| A、石墨Ⅱ电极上发生反应的电极反应式为:O2+4e-+2CO2═2CO32- |
| B、在电解池中生成N2O5的电极反应式为:N2O4+2NO3--2e-═2N2O5 |
| C、放电时熔融盐中CO32-向石墨I电极方向移动 |
| D、每消耗11.2L氢气,理论上可以制得108g N2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置Ⅰ可用于测定中和热 |
| B、装置Ⅱ装置放置一段时间后,饱和CuSO4溶液中不出现蓝色晶体 |
| C、装置Ⅲ中的石英坩埚可用于熔化氢氧化钠 |
| D、装置Ⅳ可用于吸收易溶于水的尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、1mol M最多可以与2mol Br2发生反应 |
| B、M在一定条件下可以发生消去反应、取代反应和加成反应 |
| C、一个M分子中最多有8个碳原子在同一平面上 |
| D、1mol M与足量的NaOH溶液反应,最多可以消耗3mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、溶液中c(H+)=
| ||
B、物质的量浓度c(HA)=
| ||
C、t℃时,HA的溶解度S=
| ||
D、HA的质量分数w(HA)=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有②④ | B、只有④ |
| C、只有②③④ | D、只有①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、84g NaHCO3晶体中含有NA个CO32- |
| B、0.1mol?L-1K2CO3溶液中,阴离子总数大于0.1NA |
| C、1.8g石墨和C60的混合物中,碳原子数目为0.15NA |
| D、标准状况下,22.4L CCl4中含有的共用电子对数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向稀盐酸中加入少量钠粒:2Na+2H2O═2Na++2OH-+H2↑ |
| B、向氯化铁溶液中滴加偏铝酸钠溶液:Fe3++3AlO2-+6H2O═Fe(OH)3↓+3Al(OH)3↓ |
| C、用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| D、向含氯化铝的氯化镁溶液中加入氧化镁:Al3++MgO+H2O═Al(OH)3↓+Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定温度下,4L密闭容器内M、N两种物质随时间变化的曲线如图所示:
在一定温度下,4L密闭容器内M、N两种物质随时间变化的曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com