
下列说法或表示方法正确的是
A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由“C(石墨)=C(金刚石)ΔH = +1.9kJ/mol”可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH = - 57.3kJ/mol,若将含1molCH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3kJ
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表为:2H2(g)+O2(g)=2H2O(l)ΔH = —285.8kJ/mol
科目:高中化学 来源:2014-2015学年湖南益阳市高一上学期10月月考化学试卷(解析版) 题型:填空题
(14分)下图是我校实验室化学试剂浓硫酸试剂标签上的部分内容。
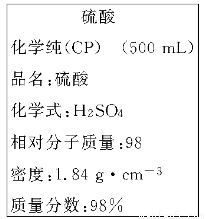
现用该浓硫酸配制480 mL 1 mol·L-1的稀硫酸。可供选用的仪器有:
①胶头滴管;②玻璃棒;③烧杯;④量筒。
请回答下列问题:
(1)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的________;
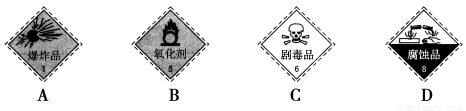
(2)配制稀硫酸时,还缺少的仪器有_________________(写仪器名称)。
(3)经计算,所需浓硫酸的体积约为________mL;若将该硫酸与等体积的水混合,所得溶液中溶质的质量分数____49%(填“>” 、“<” 或“=”)。
(4)配制过程中需先在烧杯中将浓硫酸进行稀释。稀释的操作方法是
_____________________________________________________ ;
若在稀释过程中,少量浓硫酸不慎沾在手上,处理方法为____________。
(5)对所配制的稀硫酸进行测定,发现其浓度大于1 mol·L-1,配制过程中下列各项操作可能引起该误差的原因________。
①用量筒量取浓硫酸时,仰视刻度线
②容量瓶用蒸馏水洗涤后未经干燥
③将稀释后的稀硫酸立即转入容量瓶后,立即进行后面的实验操作
④转移溶液时,不慎有少量溶液洒出
⑤定容时,俯视容量瓶刻度线
⑥定容后,把容量瓶倒置摇匀,正放后发现液面低于刻度线,又补充几滴水至刻度处
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北鄂州市高二上第一次月考化学试卷(解析版) 题型:填空题
(1)中和热的测定是高中化学的定量实验之一.50 mL0.50 mol/L 盐酸与50 mL 0.55 mol/L NaOH 溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。从实验装置上看,图中尚缺少的一种仪器是 。大烧杯上如不盖硬纸板,求得的中和热数值将会 (填“偏大”、“偏小”或“无影响”)。

(2)氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照下表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是________。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分 解。为了达到实验目的,你对原实验方案的改进方法是 ________(填一种即可)。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系下图所示。分析该图能够得出的实验结论是________。
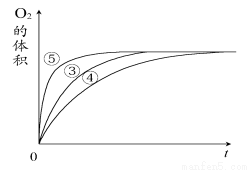
Ⅱ.资料显示,某些金属离子对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如图所示的实验装置进行实验。
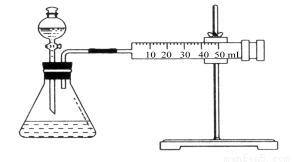
(1)
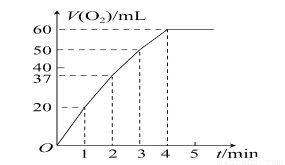
 某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量 ____ 或 _____来比较; (2)0.1g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。解释反应速率变化的原因:________,计算H2O2的初始物质的量浓度为________。(保留两位有效数字,在标准状况下测定)
某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量 ____ 或 _____来比较; (2)0.1g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。解释反应速率变化的原因:________,计算H2O2的初始物质的量浓度为________。(保留两位有效数字,在标准状况下测定)
Ⅲ.(1)为了加深对影响反应速率因素的认识,老师让甲同学完成下列实验:在Ⅱ中的实验装置的锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分液漏斗加入40 mL 2.5 mol/L的硫酸,10s时收集产生的H2体积为50 mL(若折合成标准状况下的H2体积为44.8mL),用锌粒来表示10s内该反应的速率为____g/s;
(2)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是________(填序号)。
A.化学反应速率理论可以指导怎样在一定时间内快出产品
B.勒夏特列原理可以指导怎样使有限原料多出产品
C.催化剂的使用是提高原料转化率的有效办法
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北鄂州市高二上第一次月考化学试卷(解析版) 题型:选择题
在一定条件下,可逆反应X(g) + 3Y(g) 2Z(g)达到平衡时,测得Y的转化率为37.5%,X的转化率为25%,则反应开始时,充入容器中的X、Y的物质的量之比是:
2Z(g)达到平衡时,测得Y的转化率为37.5%,X的转化率为25%,则反应开始时,充入容器中的X、Y的物质的量之比是:
A.1:3 B.3:1 C.3:2 D.1:2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北鄂州市高二上第一次月考化学试卷(解析版) 题型:选择题
某有机物的结构为下图所示,这种有机物不可能具有的性质是( )

①可以燃烧; ②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应; ④能发生酯化反应;
⑤能发生加聚反应; ⑥能发生水解反应
A.①④ B.只有⑥ C.只有⑤ D.④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中考试试化学试卷(解析版) 题型:填空题
硫酸工业中接触氧化是最重要的一个反应:2SO2(g) + O2(g)  2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
时间/min | 10 | 20 | 30 | 40 | 50 |
N(SO3)/mol | 0.4 |
0.6 | 1.2 | 1.6 | 1.6 |
(1)反应前10 min,用O2表示该反应的反应速率v(O2)= 。
(2)该温度下,该反应的平衡常数为 。
(3)在反应进行至50min时,再向容器中充入2molSO2和1molO2,达到新平衡后,SO2的转化率将 。(填“增大”、“减小”或“不变”)
(4)保持温度不变,若在该容器中只投入2mol SO3,达到平衡时,反应吸收的热量为 kJ。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中考试试化学试卷(解析版) 题型:选择题
下列关于化学反应进行的方向说法正确的是
A.放热反应都能自发进行,吸热反应都不能自发进行
B.自发反应的熵一定增大,非自发反应的熵一定减小
C.能自发进行的反应一定能实际发生
D.常温下,反应C(s)+CO2(g) === 2CO(g)不能自发进行,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中考试化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
保护环境,就是关爱自己。下列说法中你认为不正确的是( )
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com