
| A�� | ij��������ʱ����ɫ��ӦΪ��ɫ��������һ�����ƵĻ����� | |
| B�� | ��10mL0.05mol/LKAl��SO4��2��Һ�еμ�10mL0.1mol/LBa��OH��2��Һ����Ӧ����Ԫ�ص���Ҫ������ʽ��Al3+��Al��OH��3 | |
| C�� | AlCl3��NaOH��HCl��NaAlO2��Na2CO3��HCl�����Բ��������Լ��ܼ������ | |
| D�� | �����ĸ��仯�Т٢ܿ���ͨ��һ��ʵ��ֱ����ɢ�AlO2-��Al3+��Al2O3��Al��OH��3��Al3+��AlO2-��AlCl3��Al��OH��3 |
���� A����ɫ��ӦΪԪ�ص����ʣ�
B.10mL0.05mol/LKAl��SO4��2��Һ�к���0.0005mol�����ӣ�����0.001mol��������ӣ�10mL0.1mol/LBa��OH��2��Һ����0.001mol�����ӣ�0.002mol���������ӣ�
C���μ�˳���Լ����������ͬ����Ӧ������ͬ��
D��Al2O3����ֱ������Al��OH��3��
��� �⣺A����ɫ��ӦΪԪ�ص����ʣ���һ��Ϊ�����Ҳ����Ϊ���ʣ���A����
B.10mL0.05mol/LKAl��SO4��2��Һ�к���0.0005mol�����ӣ�����0.001mol��������ӣ�10mL0.1mol/LBa��OH��2��Һ����0.001mol�����ӣ�0.002mol���������ӣ�ǡ�÷�Ӧ����ƫ��������ӣ���B����
C��NaOH��Һ��AlCl3��Һ�μ�˳��ͬ������ͬ����NaOH��Һ�μӵ�AlCl3 ��Һ�У������ɳ�������NaOH����ʱ�������ܽ⣬HCl��NaAlO2��Һ�μ�˳��ͬ������ͬ����NaAlO2�μӵ�HCl��Һ����û�г������ɣ����μӵ�һ���̶�ʱ�г������ɣ�����HCl�μӵ�NaAlO2��Һ�У���ʼ���г������ɣ�����ȫ��Ӧ���ٵμ���Һ���������ܽ⣬Na2CO3 ��HCl��Һ�μ�˳��ͬ������ͬ����Na2CO3 �μӵ�HCl��Һ���������������������HCl�μӵ�Na2CO3 ��Һ�У���û���������ɣ����μӵ�һ���̶�ʱ�������������ɣ���C��ȷ��
D��Al2O3��ˮ����Ӧ������ֱ������Al��OH��3����D����
��ѡC��
���� �����ۺϿ���Ԫ�ػ�����֪ʶ��Ϊ�߿��������ͺ�Ƶ���㣬������ѧ���ķ���������ʵ�������Ŀ��飬ע��������ʵ������Լ���Ӧ������жϣ��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
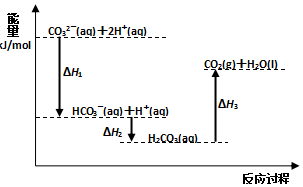
| A�� | ��ӦHCO3-��aq��+H+��aq��=CO2��g��+H2O��l�� Ϊ���ȷ�Ӧ | |
| B�� | CO32-��aq��+2H+��aq��=CO2��g��+H2O��l����H=����H1+��H2+��H3�� | |
| C�� | ��H1����H2��H2����H3 | |
| D�� | H2CO3��aq��=CO2��g��+H2O��l������ʹ�ô��������H3��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
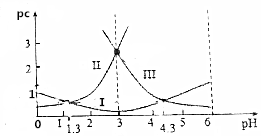 ���ᣨH2C2O4��ˮ��Һ��pc��H2C2O4����pc��HC2O4-����pc��C2O42-��������ҺpH�ı仯������ͼ��ʾ������˵���в���ȷ���ǣ�������
���ᣨH2C2O4��ˮ��Һ��pc��H2C2O4����pc��HC2O4-����pc��C2O42-��������ҺpH�ı仯������ͼ��ʾ������˵���в���ȷ���ǣ�������| A�� | pH=4ʱ��c��HC2O4-����c��C2O42-�� | |
| B�� | c��H2C2O4��+c��HC2O4-��+c��C2O42-��һ������ | |
| C�� | ����ĵ��볣��Ka1=10-1.3 | |
| D�� | $\frac{c��{C}_{2}{{O}_{4}}^{2-}��•c��{H}_{2}{C}_{2}{O}_{4}��}{{c}^{2}��H{C}_{2}{{O}_{4}}^{-}��}$=10-3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڻ�����CaCl2�У�������Ca2+��Cl-֮������Ӽ��⣬��������Cl-֮��Ĺ��ۼ� | |
| B�� | ����������ʱ���ۼ����ƻ� | |
| C�� | �ۻ�״̬���ܵ���Ļ�������һ���������Ӽ� | |
| D�� | ���ӻ������п��ܺ��й��ۼ������ۻ������п��ܺ������Ӽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��NH4+����c��SO42-����c��H+����c��OH-�� | B�� | c��NH4+��=2c��SO42-�� | ||
| C�� | c��NH4+��+c��NH3•H2O��=2c��SO42-�� | D�� | c��NH4+��+c��H+��=c��OH-��+2c��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
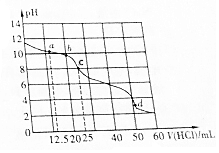 �����£���VmL0.01mol•L-1��BOH��Һ�еμ�0.01mol•L-1���ᣬ��ҺpH���������֮��Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������
�����£���VmL0.01mol•L-1��BOH��Һ�еμ�0.01mol•L-1���ᣬ��ҺpH���������֮��Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������| A�� | BOH���뷽��ʽΪBOH�TB++OH- | |
| B�� | ��������Һ��pH=2 | |
| C�� | ��c��ʾ����Һ��c��OH-��=1.0��10-6mol•L-1 | |
| D�� | BOH��aq��+HCl��aq���TBCl��aq��+H2O��l����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Na+2H2O=2NaOH+H2�� | B�� | CaO+H2O�TCa��OH��2 | ||
| C�� | SO3+H2O�TH2SO4 | D�� | 2F2+2H2O�T4HF+O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ۢ� | C�� | �ڢܢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com