
 xC(g)+2D(g) ΔH<0经5min后达到平衡,平衡时测得D的浓度为0.5mol/L,C(A):C(B)=1:2,C的平均反应速率为0.05mol/(L·min)
xC(g)+2D(g) ΔH<0经5min后达到平衡,平衡时测得D的浓度为0.5mol/L,C(A):C(B)=1:2,C的平均反应速率为0.05mol/(L·min)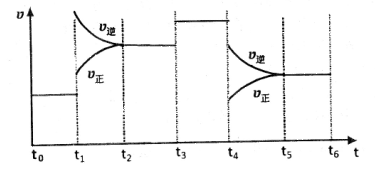
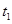 、
、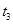 、
、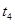 时刻体系中分别是什么条件发生了变化?
时刻体系中分别是什么条件发生了变化?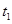 ___________、
___________、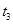 _____________ 、
_____________ 、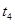 _____________(填A-E)
_____________(填A-E)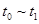 B.
B.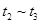 C.
C.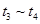 D.
D.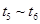


科目:高中化学 来源:不详 题型:单选题
| A.向FeCl3和KSCN混合溶液中加入少量KCl固体,溶液血红色变浅 |
| B.向5mL 0.1mol/L K2Cr2O7溶液中加入少量NaOH固体,溶液由橙色变为黄色 |
| C.等体积等浓度Na2S2O3和H2SO4混合,温度升高出现浑浊和生成气体速度加快 |
| D.酸性KMnO4溶液中滴加H2C2O4,H2C2O4浓度越大褪色和生成气体速度越快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①②③④ | B.①③④ | C.①② | D.①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B.0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度30℃ |
| D.0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应是吸热反应,且可逆,加热使平衡向正向移动 |
| B.加热促使SO2逸出,使平衡向正向移动 |
| C.加热促进S2O32-与H+的碰撞,使反应加速 |
| D.加热促进Na+与Cl-的碰撞,使反应加速 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是
CH3CH2OH(g)△H <0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是| A.充入氦气 | B.分离除乙醇 | C.增大压强 | D.升高温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
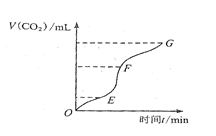
| A.蒸馏水 | B.NaCl固体 | C.NaCl溶液 | D.浓盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.②④⑥ | C.②⑤⑥ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3合成氨反应中,在下列情况下,不能使反应速率加快的是
2NH3合成氨反应中,在下列情况下,不能使反应速率加快的是 | A.充入氮气 | B.减小压强,扩大容器体积 |
| C.加入催化剂 | D.适当升高温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com