
【题目】氢气是一种十分熟悉的物质.在许多反应中既可以作为反应物,也可以作物生成物.
(1)电解饱和食盐水制取氢气,反应的化学方程式
(2)在氢气还原氧化铜的反应中,标出电子转移的方向及数目. H2+CuO ![]() Cu+H2O.
Cu+H2O.
(3)在铜锌原电池中,如图,在铜极附近看到的现象是;电子流向从 .
(4)氢气作为燃料,有1g氢气燃烧生成液态水放出142.8kJ热量,表示该反应的热化学方程式;
(5)实验室用锌与稀硫酸反应制取氢气.某学校实验员为了提高制取氢的速度,在此溶液中加入少量硫酸铜溶液,你认为合理吗?为什么? . 
【答案】
(1)2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(2)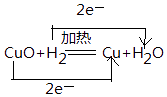
(3)Cu电极上产生气泡;电子从Zn电极沿导线流向Cu电极
(4)H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8kJ/mol
O2(g)=H2O(l)△H=﹣285.8kJ/mol
(5)因为Zn置换出硫酸铜溶液中的Cu,Zn、Cu和稀硫酸构成原电池,原电池能加快化学反应速率,所以该操作能提高制取氢气的速率
【解析】解:(1)用惰性电极电解饱和食盐水时,阳极上氯离子失电子生成氯气,阴极上水得电子生成氢气同时生成氢氧根离子,则电池反应式为2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,
2NaOH+H2↑+Cl2↑,
所以答案是:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑;(2)该反应中H元素化合价由0价变为+1价、Cu元素化合价由+2价变为0价,转移电子数为2,电子转移方向和数目为
2NaOH+H2↑+Cl2↑;(2)该反应中H元素化合价由0价变为+1价、Cu元素化合价由+2价变为0价,转移电子数为2,电子转移方向和数目为 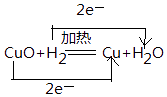 ,
,
所以答案是: 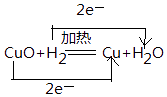 ;(3)该铜锌原电池中,Zn易失电子生成锌离子而作负极,Cu作正极,Cu电极上氢离子得电子生成氢气,则Cu电极上看到的现象是:有气泡产生,在外电路中电子从负极沿导线流向正极,所以电子从Zn电极沿导线流向Cu电极,
;(3)该铜锌原电池中,Zn易失电子生成锌离子而作负极,Cu作正极,Cu电极上氢离子得电子生成氢气,则Cu电极上看到的现象是:有气泡产生,在外电路中电子从负极沿导线流向正极,所以电子从Zn电极沿导线流向Cu电极,
所以答案是:Cu电极上产生气泡;电子从Zn电极沿导线流向Cu电极;(4)n(H2)= ![]() =0.5mol,0.5mol氢气完全燃烧生成液态水放出142.8kJ热量,则1mol氢气完全燃烧生成液态水放出285.6kJ热量,其热化学方程式为H2(g)+
=0.5mol,0.5mol氢气完全燃烧生成液态水放出142.8kJ热量,则1mol氢气完全燃烧生成液态水放出285.6kJ热量,其热化学方程式为H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8kJ/mol,
O2(g)=H2O(l)△H=﹣285.8kJ/mol,
所以答案是:H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8kJ/mol;(5)Zn置换出硫酸铜溶液中的Cu,Zn、Cu和稀硫酸构成原电池,原电池能加快化学反应速率,所以在此溶液中加入少量硫酸铜溶液能提高制取氢气的速度,
O2(g)=H2O(l)△H=﹣285.8kJ/mol;(5)Zn置换出硫酸铜溶液中的Cu,Zn、Cu和稀硫酸构成原电池,原电池能加快化学反应速率,所以在此溶液中加入少量硫酸铜溶液能提高制取氢气的速度,
所以答案是:合理;因为Zn置换出硫酸铜溶液中的Cu,Zn、Cu和稀硫酸构成原电池,原电池能加快化学反应速率,所以该操作能提高制取氢气的速率.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是( )
A.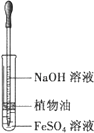 观察Fe(OH)2的生成
观察Fe(OH)2的生成
B.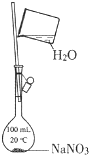 配制一定物质的量浓度的NaNO3溶液
配制一定物质的量浓度的NaNO3溶液
C. 实验室制取氨
实验室制取氨
D.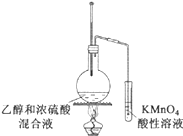 验证乙烯的生成
验证乙烯的生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强热绿矾晶体,除结晶水蒸发外,还发生如下化学反应:2FeSO4 ![]() Fe2O3+SO2↑+SO3↑.如果将生成的气体通入浓BaCl2溶液中,产生的现象是( )
Fe2O3+SO2↑+SO3↑.如果将生成的气体通入浓BaCl2溶液中,产生的现象是( )
A.生成确BaSO4和BaSO3混合沉淀
B.生成BaSO4沉淀,有SO2气体逸出
C.生成BaSO4沉淀,有SO3气体逸出
D.有SO2和SO3两种气体同时逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是含氧酸,第二种是混合物,第三种是碱的是( )
A. 爆鸣气、硫酸铜、硫酸 B. 水、空气、纯碱
C. 硝酸、石灰石、烧碱 D. 氧化铁、胆矾、熟石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是( )
A. 元素周期表共有七个周期B. 元素周期表共有18个族
C. 所含元素种数最多的族是Ⅷ族D. 原子核外最外层电子数为2的元素都是第ⅡA元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.原电池外电路中电子由负极流向正极
B.原电池中发生还原反应的电极是正极
C.电解池中发生还原反应的电极是阳极
D.电解池中质量增加的电极是阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(夹持装置省略),按要求回答问题:
(1)写出浓盐酸与二氧化锰反应制取Cl2的离子方程式 ,
实验中若用0.2mol浓盐酸与足量的MnO2反应制得Cl2的体积(标况下)总是小于1.12L的原因是 ,
(2)①装置B的作用是;
②装置C和D出现的不同现象说明的问题是;
③装置E的作用是;
(3)乙同学认为甲同学的实验有缺陷,不能确定最终通入AgNO3溶液中的气体只有一种.为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置与之间(填装置字母序号)增加一个装置,增加装置里面的试剂可为 .
A.湿润的淀粉KI试纸 B.氢氧化钠溶液
C.湿润的红色布条 D.饱和的食盐水.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com