
【题目】一种利用失活的含镍催化剂(含NiB、MgO及SiO2等)为原料制备超细镍粉,其工艺流程如下:
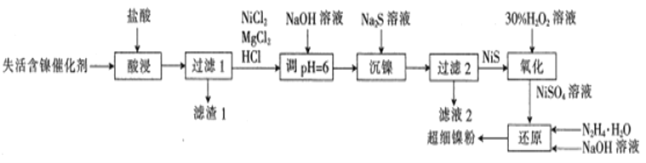
已知:pH=6时,Mg2+、Ni2+都不生成沉淀。
回答下列问题:
(1)非晶态NiB可由KBH4和Ni(NO3)2溶液反应制备。KBH4的电子式为_________
(2)“酸浸”时,为提高镍的浸取率可采取的措施是___________ (列举一点);滤值1中除了含有B单质外,还含有___________ (填化学式)。
(3)若流程中没有“NaOH溶液调pH=6”,则导致的后果是________
(4)“氧化”时发生反应的化学方程式为_______________;氧化时温度不宜超过50℃,其原因是_________________
(5)“还原”时产生无污染的气体,“还原”时发生反应的离子方程式为___________
【答案】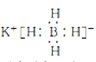 碎失活的含镍催化剂,增大反应物的接触面积或增大盐酸的浓度(或用量)或适当延长浸取时间或搅拌(或振荡)等 SiO2 会产生大量硫化氢气体,污染环境 NiS+4H2O2=NiSO4+4H2O 减少过氧化氢分解损失 2Ni2++N2H4·H2O+4OH—=2Ni↓+N2↑+4H2O
碎失活的含镍催化剂,增大反应物的接触面积或增大盐酸的浓度(或用量)或适当延长浸取时间或搅拌(或振荡)等 SiO2 会产生大量硫化氢气体,污染环境 NiS+4H2O2=NiSO4+4H2O 减少过氧化氢分解损失 2Ni2++N2H4·H2O+4OH—=2Ni↓+N2↑+4H2O
【解析】
向失活的含镍催化剂中加入盐酸,NiB溶于盐酸生成Ni2+和B,MgO溶于盐酸生成Mg2+,SiO2与盐酸不反应,过滤,得到含有Ni2+和Mg2+的溶液和含有B单质和SiO2的滤渣;向滤液中加入NaOH溶液pH为6,再加入Na2S溶液,Na2S溶液与Ni2+反应生成NiS沉淀,过滤得到NiS沉淀;向NiS沉淀中加入30%过氧化氢溶液,NiS沉淀与过氧化氢溶液反应生成硫酸镍和水;向溶液中继续加入N2H4·H2O和氢氧化钠溶液,硫酸镍和N2H4·H2O碱性条件下发生氧化还原反应生成超细镍粉。
(1)KBH4是由K+和BH4—组成的离子化合物,电子式为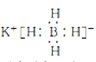 ,故答案为:
,故答案为: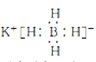 ;
;
(2)“酸浸”时,为提高镍的浸取率,可粉碎失活的含镍催化剂,增大反应物的接触面积或增大盐酸的浓度(或用量)或适当延长浸取时间或搅拌(或振荡)等;向失活的含镍催化剂中加入盐酸,NiB溶于盐酸生成Ni2+和B,MgO溶于盐酸生成Mg2+,SiO2与盐酸不反应,过滤得到的滤渣1中除了含有B单质外,还含有SiO2,故答案为:碎失活的含镍催化剂,增大反应物的接触面积或增大盐酸的浓度(或用量)或适当延长浸取时间或搅拌(或振荡)等;SiO2;
(3)若流程中没有“NaOH溶液调pH=6”,加入Na2S溶液时,Na2S溶液会与氢离子反应生成有毒的硫化氢气体,污染空气,故答案为:会产生大量硫化氢气体,污染环境;
(4)“氧化”时,,NiS沉淀与过氧化氢溶液反应生成硫酸镍和水,反应的化学方程式为NiS+4H2O2=NiSO4+4H2O,故答案为:NiS+4H2O2=NiSO4+4H2O;因过氧化氢受热易分解生成氧气和水,则氧化时温度不宜超过50℃,故答案为:NiS+4H2O2=NiSO4+4H2O;减少过氧化氢分解损失;
(5)“还原”时,硫酸镍和N2H4·H2O碱性条件下发生氧化还原反应生成超细镍粉,反应的离子方程式为2Ni2++N2H4·H2O+4OH—=2Ni↓+N2↑+4H2O,故答案为:2Ni2++N2H4·H2O+4OH—=2Ni↓+N2↑+4H2O。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:
【题目】感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料,其结构简式为 。
。
试回答下列问题:
(1)该物质的单体是______。
(2)在一定条件下,该高聚物可发生的反应有__________(填序号)。
①加成反应 ②氧化反应 ③取代反应 ④酯化反应
(3)该高聚物在催化剂的作用下,水解后得到相对分子质量较小的产物为A,则:
①A的分子式是_____。
②A在一定条件下与乙醇反应的化学方程式是________。
③A的同分异构体有多种,其中含有苯环、![]() 和
和![]() ,且苯环上有两个对位取代基的结构简式是_______、______。
,且苯环上有两个对位取代基的结构简式是_______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在家中进行化学实验,按照图1连接好线路后发现灯泡不亮,按照图2连接好线路后发现灯泡亮,由此得出的结论正确的是
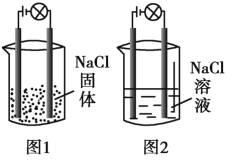
A. NaCl固体中没有离子
B. 图2中NaCl在电流的作用下电离出大量的离子
C. NaCl溶液中水电离出大量的离子
D. 图2工作时发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述不正确的是( )
A.试剂X可以是氢氧化钠溶液
B.反应①过滤后所得沉淀为氧化铁
C.图中所示转化反应包含氧化还原反应
D.反应②的化学方程式为2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某校化学实验兴趣小组为了验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),请按要求回答下列问题。
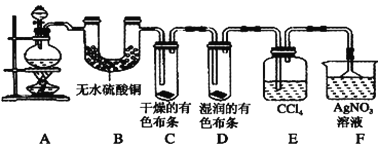
(1) 实验室制备Cl2所用的化学药品是________。
写出该反应的离子方程式,并用单线桥表示电子转移情况_____________________ ,此反应中每转移0.8mol电子,消耗Hcl____mol
(2)①装置B的作用是_______
②装置C和D出现的不同现象说明的问题是___
③装置E的作用是_______
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置___与___之间(填装置字母序号)增加一个装置,所增加装置里面的试剂可以为___(填字母序号)。
A.湿润的碘化钾淀粉试纸 B.浓硫酸 C.湿润的红色布条 D.饱和食盐水
Ⅱ.洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为:_____________。
②漂白粉的有效成分是________________________。
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某同学采用萃取—分液的方法从碘水中提取碘,主要操作步骤如下图:

①该同学所采用的萃取剂可能是______________(填序号)。
A 酒精 B 苯 C 四氯化碳 D 汽油
②甲、乙、丙3步实验操作中,不正确的是_______________(填“甲”、“乙”或“丙”)。
(2)实验室制取、净化并收集氯气涉及以下几个主要阶段:

现有以下2种试剂:A 饱和食盐水 B NaOH溶液
请在以上实际中选择填空(填“A”或“B”):
①X溶液应选用________________。
②尾气处理过程中,多余的氯气可用________________吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 在煤中添加石灰石作脱硫剂
B. 将废弃塑料热裂解处理,可获得乙烯、丙烯等化工原料
C. 用催化法处理汽车尾气中的CO和NO:CO+NO![]() C+NO2
C+NO2
D. 利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1mol/L①CH3COOH、②NaOH、③CH3COONa,下列叙述正确的是( )
A.①中[CH3COOH]>[CH3COO-]>[H+]>[OH-]
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则(Na+)>(CH3COO-)>(H+)
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物的结构简式如图所示: ![]() (a)、
(a)、![]() (b)、
(b)、![]() (c)。下列说法正确的是
(c)。下列说法正确的是
A. 三种物质中只有a、b互为同分异构体
B. a、b、c分别有3种、4种、5种不同化学环境的氢原子
C. a、b、c均能发生氧化反应、取代反应、加成反应
D. c分子内至少有6个碳原子共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com