
【题目】实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:

(1)该实验制取溴乙烷的化学方程式为:__.
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为__,同时生成的无色气体分子式为__.
(3)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是__.
(4)U型管内可观察到的现象是__.
(5)反应结束后,∪形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的__(填序号).
(a)NaOH溶液 (b)H2O (c)Na2SO3溶液 (d)CCl4
所需的主要玻璃仪器是__(填仪器名称).要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行__(填操作名称).
(6)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__(填代号).
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却.
【答案】NaBr+H2SO4+C2H5OH![]() NaHSO4+C2H5Br+H2O Br2 SO2和H2O 水浴加热 有油状液体生成 c 分液漏斗 蒸馏 ④①⑤③②
NaHSO4+C2H5Br+H2O Br2 SO2和H2O 水浴加热 有油状液体生成 c 分液漏斗 蒸馏 ④①⑤③②
【解析】
(1)乙醇、浓硫酸和溴化钠加热反应生成溴乙烷、硫酸氢钠和水;
(2)浓硫酸具有强氧化性,温度过高会把溴离子氧化成红棕色的溴,同时浓硫酸被还原成二氧化硫;
(3)为了更好的控制温度,最好用水浴加热的方法;
(4)U型管得到了溴乙烷;
(5)溴乙烷中混有溴,除杂时注意溴和溴乙烷的性质角度考虑;分液用到分液漏斗;将溴乙烷与水分离采用蒸馏操作;
(6)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成;有溴乙烷参加的主要反应是溴乙烷和碱溶液中的水解。
(1)溴化钠、浓硫酸和乙醇制取溴乙烷的化学方程式为:NaBr+H2SO4+C2H5OH![]() NaHSO4+C2H5Br+H2O,故答案为:NaBr+H2SO4+C2H5OH
NaHSO4+C2H5Br+H2O,故答案为:NaBr+H2SO4+C2H5OH![]() NaHSO4+C2H5Br+H2O;
NaHSO4+C2H5Br+H2O;
(2)由于浓硫酸具有强氧化性,会有溴生成,化学式为Br2,同时浓硫酸被还原成SO2,因此无色气体为SO2和H2O,故答案为:Br2;SO2和H2O;
(3)为了更好的控制温度,最好用水浴加热的方法,故答案为:水浴加热;
(4)U型管得到了溴乙烷,因此可观察到有油状液体生成,故答案为:有油状液体生成;
(5)粗制的C2H5Br呈棕黄色,说明含有单质溴杂质,则,
a.溴乙烷能够与氢氧化钠反应,故A错误;
b.溴在溴乙烷中的溶解度比在水中大,加水难以除去溴乙烷中的溴,故B错误;
c.Na2SO3与溴发生氧化还原反应,Na2SO3可除去溴,故C正确;
d.溴和溴乙烷都能溶于四氯化碳,不能将二者分离,故D错误;
分液使用的主要仪器是分液漏斗,要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,利用沸点不同再进行蒸馏分离,故答案为:c;分液漏斗;蒸馏;
(6)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,所以操作顺序为④①⑤③②,故答案为:④①⑤③②。


科目:高中化学 来源: 题型:
【题目】已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.H2O(g)= H2(g)+![]() O2(g) ΔH=242 kJ·mol-1
O2(g) ΔH=242 kJ·mol-1
B.2H2(g)+O2(g)= 2H2O(l) ΔH=-484 kJ·mol-1
C.H2(g)+![]() O2(g)= H2O(g) ΔH=242 kJ·mol-1
O2(g)= H2O(g) ΔH=242 kJ·mol-1
D.2H2(g)+O2(g)= 2H2O(g) ΔH=484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下AgCl(s)的溶度积常数Ksp=1×10-10。在该温度下,向50mL 0.018mol/L的AgNO3溶液中加入50mL 0.02mol/L的盐酸,生成沉淀(混合后溶液的体积变化忽略不计)。下列说法正确的是()
A.AgCl的溶解性为难溶,则该物质不溶于水
B.沉淀生成后,溶液中Ag+的浓度1×10-5mol/L
C.沉淀生成后,溶液中NO3-的浓度1.8×10-2mol/L
D.沉淀生成后,溶液的pH为2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的恒容密闭容器中,发生反应如下:X(g) + 2Y(g)![]() W(g) + Z(g),下列物理量不能用于表明反应是否已达到平衡状态的是
W(g) + Z(g),下列物理量不能用于表明反应是否已达到平衡状态的是
A.Y的物质的量浓度
B.混合气体的密度
C.混合气体的压强
D.混合气体的平均相对分子量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是五种主族元素的结构特点及其元素、单质、化合物的性质.
元素 | 结构特点及元素、单质、化合物的性质 |
X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
W | 最外层电子排布(n+1)sn(n+1)pn﹣1 |
T | 单质升华可以产生紫色的烟 |
(1)写出X元素的原子核外电子排布__;其单质的化学性质__(填“稳定”或“活泼”),该元素的非金属性__(填“强”或“弱”),证明其强弱的理由是__.
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式__;已知w的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为__.
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:__,__.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为__.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一包铝热剂(铝粉和氧化铁的混合物),进行如下实验,①向一份铝热剂中加入800ml 2mol/L的氢氧化钠溶液,使其充分反应后,收集到的气体体积为20.16L(S.T.P.)②另一份等质量的铝热剂在高温下充分反应后,向反应后固体中加入2L 2.5mol/L的盐酸溶液,使固体完全溶解,反应后溶液PH=0(假设过程中溶液体积不变),取少量反应后溶液,滴加硫氰化钾,没有出现血红色.完成下列计算:
(1)计算该铝热剂中铝与氧化铁物质的量之比?_______________
(2)实验②产生的气体的体积是多少?(S.T.P.)______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄是一种常见水果,可以生食或制作葡萄干,除此之外,葡萄还可用于酿酒。
(1)检验葡萄汁含有葡萄糖的方法是:向其中加碱调至碱性,再加入新制的Cu(OH)2并加热,其现象是________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)![]() 2_________+ 2 C2H5OH
2_________+ 2 C2H5OH
(3)葡萄酒密封储存过程中会生成有香味的酯类,酯类也可以通过化学实验来制备,实验室可用如图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是__________。
②试管b中盛放的试剂是饱和____________溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是________。
④若要分离出试管b中的乙酸乙酯,需要用到的仪器是_______(填字母)。
A.普通漏斗 B.分液漏斗 C.长颈漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯氏制碱法原理是:NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl析出碳酸氢钠,下列实验装置及原理设计说法不合理的是:
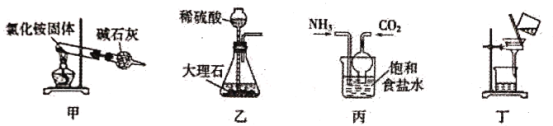
A.用装置甲制取氨气时得到氨气很少,主要原因是分解得到NH3、HCl的遇冷会重新化合
B.用装置乙生成的CO2速率很慢,原因是反应生成微溶于水的硫酸钙,覆盖着大理石的表面
C.用装置丙模拟侯氏制碱法,可以同时通入NH3、CO2,也可以先通氨气再通CO2
D.用装置丁分离得到产品NaHCO3,为得到干燥产品,也可采用减压过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应2HI(g) ![]() H2(g) + I2(g) - 11 kJ,正确的是
H2(g) + I2(g) - 11 kJ,正确的是
A.反应物的总键能低于生成物的总键能
B.1mol I2(g)中通入1mol H2(g),反应放热11kJ
C.等物质的量时,I2(g)具有的能量低于I2(l)
D.平衡时分离出HI(g),正反应速率先减小后增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com