
【题目】下表是五种主族元素的结构特点及其元素、单质、化合物的性质.
元素 | 结构特点及元素、单质、化合物的性质 |
X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
W | 最外层电子排布(n+1)sn(n+1)pn﹣1 |
T | 单质升华可以产生紫色的烟 |
(1)写出X元素的原子核外电子排布__;其单质的化学性质__(填“稳定”或“活泼”),该元素的非金属性__(填“强”或“弱”),证明其强弱的理由是__.
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式__;已知w的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为__.
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:__,__.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为__.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
【答案】1s22s22p3 稳定 强 硝酸是强酸 ![]() 分子晶体 Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH﹣=AlO2﹣+2H2O AB
分子晶体 Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH﹣=AlO2﹣+2H2O AB
【解析】
五种主族元素中,X气态氢化物与最高价氧化物对应水化物可以化合成盐,则X为N元素;Y原子中s电子数与p电子数相同,且p电子的能量最高,核外电子排布为1s22s22p4,则Y为O元素;Z单质在空气中燃烧产生黄色火焰,生成黄色粉末,则Z为Na;W元素原子最外层电子排布(n+1)sn(n+1)pn﹣1,由于s能级只能容纳2个电子,且p能级已填充电子,故n=2,则W为Al;T单质升华可以产生紫色的烟,则T为I元素,据此解答。
(1)X为N元素,电子排布式为1s22s22p3;其单质中存在氮氮三键,化学性质稳定,该元素的非金属性强,证明其强弱的理由是:硝酸是强酸等,故答案为:1s22s22p3;稳定;强;硝酸是强酸;
(2)Z单质在空气中燃烧生成黄色粉末为Na2O2,其电子式为![]() ;已知W的氯化物在177.8°C时会发生升华现象,熔沸点很低,由此可以判断它的晶体类型为:分子晶体,故答案为:
;已知W的氯化物在177.8°C时会发生升华现象,熔沸点很低,由此可以判断它的晶体类型为:分子晶体,故答案为:![]() ;分子晶体;
;分子晶体;
(3)W的最高价氧化物对应的水化物为氢氧化铝,X、Z的最高价氧化物对应的水化物分别为硝酸、NaOH,氢氧化铝与硝酸、氢氧化钠反应的离子方程式:Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH﹣=AlO2﹣+2H2O;故答案为:Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH﹣=AlO2﹣+2H2O;
(4)O、I可形成多种化合物,其中I元素的化合价为+3、+5时,可以看作I2O3、I2O5 混合物,二者1:1混合时为I2O4,二者1:3混合时为I4O9,由O、I原子数目之比可知不可能为I6O10,由于I元素化合价可知,不能为I2O3,故选:AB。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】骨胶黏剂是一种极具应用前景的医用高分子材料。某骨胶黏剂的制备原料为聚酯三元醇,其合成原理如下:
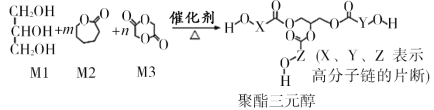
已知:R1COOR2+R318OH![]() R1CO18OR3+R2OH
R1CO18OR3+R2OH
下列说法正确的是
A.单体Ml可用于配制化妆品,且分子中含有3个手性碳原子
B.改变Ml在三种单体中的比例,可调控聚酯三元醇的相对分子质量
C.该合成反应为缩聚反应
D.X、Y、Z中包含的结构片段可能有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
(提出猜想)小组提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2 乙:MgO、NO2、O2
丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)查阅资料得知,NO2可被NaOH溶液吸收,反应的化学方程式为:____________.
(2)实验前,小组成员经讨论认定猜想丁不成立,理由是____________.
(实验操作)
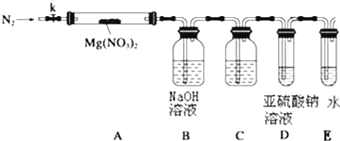
(3)设计如图装置,用氮气排尽装置中空气,其目的是___________;加热Mg(NO3)2固体,AB装置实验现象是:____________,说明有Mg(NO3)2固体分解了,有NO2生成.
(4)有同学提出可用亚硫酸钠溶液检验是否有氧气产生,但通入之前,还需在BD装置间增加滴有酚酞的氢氧化钠溶液,其作用是:____________
(5)小组讨论后认为即便通过C后有氧气,仅仅用亚硫酸钠溶液仍然难以检验,因为:____________,改进的措施是可在亚硫酸钠溶液中加入____________.
(6)上述系列改进后,如果分解产物中有O2存在,排除装置与操作的原因,未检测到的原因是____________.(用化学方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)100°C时,KW=1.0×10-12,在该温度下,测得0.1mol/L Na2A溶液pH=6。
①H2A在水溶液中的电离方程式为_____;
②体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,H2A溶液产生的H2_____(填“多”、“少”或“一样多”)。
(2)将0.4mol/L HA溶液与0.2mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-):
①混合溶液中c(A)_____c(HA)(填“>”、“<”或“=”,下同);
②混合溶液中c(HA)+c(A)_____0.2mol/L。
(3)已知在常温下测得浓度均为0.1mol/L的下列5种溶液的pH,如表所示:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①少量二氧化碳通入NaClO溶液中的离子方程式_____;
②浓度均为0.01mol/L的下列4种物质的溶液分别加水稀释100倍,pH变化最小的是_____(填编号);
a.CH3COOH b.HCN c.HClO d.H2CO3
③常温下浓度相同的醋酸和醋酸钠混合液pH=6,则c(CH3COO-)-c(CH3COOH)=_____mol/L(填准确数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A(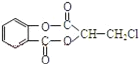 )在一定条件下可以发生如图所示的转化(其他产物和水已略去)。
)在一定条件下可以发生如图所示的转化(其他产物和水已略去)。
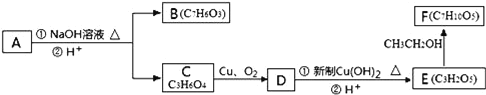
请回答下列问题:
(1)请写出A中包含的官能团的名称:__。
(2)有机物C可以由乳酸经过几步有机反应制得,其中最佳的次序是__。
A.消去、加成、水解、酸化 B.氧化、加成、水解、酸化
C.取代、水解、氧化、酸化 D.消去、加成、水解、氧化
(3)写出由E制得F的化学方程式:__。
(4)1molA在氢氧化钠溶液中加热,充分反应消耗氢氧化钠__mol,写出该反应的化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:

(1)该实验制取溴乙烷的化学方程式为:__.
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为__,同时生成的无色气体分子式为__.
(3)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是__.
(4)U型管内可观察到的现象是__.
(5)反应结束后,∪形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的__(填序号).
(a)NaOH溶液 (b)H2O (c)Na2SO3溶液 (d)CCl4
所需的主要玻璃仪器是__(填仪器名称).要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行__(填操作名称).
(6)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__(填代号).
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①在稀碱溶液中,溴苯难发生水解
②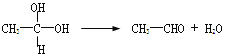
③苯酚与浓溴水反应,只有邻、对位上的氢被取代
现有分子式为C10H10O2Br2的芳香族化合物X,其苯环上有四个取代基且苯环上的一溴代物只有一种,其在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。
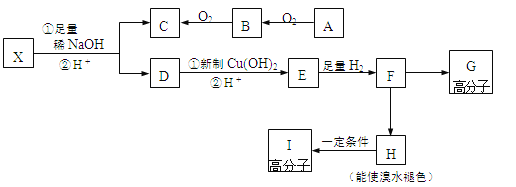
请完成下列填空:
47、写出B的电子式________;F→H的反应类型是________反应。
48、写出A→B的化学方程式_________________________。
49、X的结构简式为__________。
50、下列关于E的描述正确的是___(选填序号)
a.能发生酯化反应 b.含有4种不同化学环境的氢原子
c.与C互为同系物 d.1mol E最多能与2mol NaHCO3作用
51、写出F→G的化学方程式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B ![]() 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=2 mol·L-1·s-1B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1D.v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 甲苯分子中所有原子在同一平面上
B. 苯、乙酸、乙醇均能发生取代反应
C. 分子式为C3H6Cl2的同分异构体共有4种(不考虑立体异构)
D. 可用溴的四氯化碳溶液区别![]() 和
和![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com