
【题目】几种有机物的转化关系如下图所示(部分条件已省略)
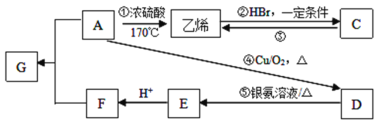
(1)反应①的化学方程式为____________________,反应类型为_________。
(2)③的试剂及反应条件是____________。
(3)写出反应④的化学方程式___________________。
(4)写出反应⑤的化学方程式__________________。
(5)写出A+F反应生成G的化学方程式____________________。
【答案】C2H5OH![]() CH2=CH2↑+H2O 消去反应 NaOH的醇溶液、加热 2CH3CH2OH
CH2=CH2↑+H2O 消去反应 NaOH的醇溶液、加热 2CH3CH2OH![]() 2CH3CHO+2H2O CH3CHO +2Ag(NH3)2OH
2CH3CHO+2H2O CH3CHO +2Ag(NH3)2OH![]() CH3COONH4+2Ag
CH3COONH4+2Ag![]() +3NH3+ H2O CH3COOH+C2H5OH
+3NH3+ H2O CH3COOH+C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
【解析】
A在浓硫酸加热170℃的条件下生成乙烯,可以得出A是乙醇,乙烯与溴化氢反应生成溴乙烷(C),乙醇在铜作催化剂与氧气反应生成乙醛(D),乙醛与银氨溶液反应产物之一是乙酸铵(E),乙酸铵加入酸生成乙酸(F),乙醇(A)与乙酸(F)反应生成乙酸乙酯(G)和水,据此回答问题。
(1)有以上分析可知,反应①的化学方程式为C2H5OH![]() CH2=CH2↑+H2O,反应类型是消去反应;
CH2=CH2↑+H2O,反应类型是消去反应;
(2)反应③是溴乙烷生成乙烯,反应需要的试剂是NaOH的醇溶液,反应条件需要加热;
(3)反应④是乙醇催化氧化生成乙醛,化学方程式是2CH3CH2OH![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(4)反应⑤是乙醛与银氨溶液反应生成乙酸铵、银、氨气和水,化学方程式是CH3CHO +2Ag(NH3)2OH![]() CH3COONH4+2Ag
CH3COONH4+2Ag![]() +3NH3+ H2O;
+3NH3+ H2O;
(5)A(乙醇)+F(乙酸)反应生成G(乙酸乙酯)的化学方程式是CH3COOH+C2H5OH CH3COOC2H5+H2O。
CH3COOC2H5+H2O。


科目:高中化学 来源: 题型:
【题目】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓硝酸、浓硫酸反应生成SeO2以回收Se。在回收过程中涉及如下化学反应:①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O;③Se+4HNO3(浓)=SeO2+4NO2↑+2H2O;
下列有关叙述正确的是( )
A.氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2
B.反应①中Se是氧化产物,I2是还原产物
C.反应①中生成0.6molI2,转移的电子数目为2.4NA
D.反应②③中等量的Se消耗浓硫酸和浓硝酸中溶质的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学展开对漂白剂亚氯酸钠![]() 的研究.
的研究.
实验I:制取![]() 晶体
晶体
己知:![]() 饱和溶液在温度低于
饱和溶液在温度低于![]() 时析出晶体是
时析出晶体是![]() ,高于
,高于![]() 时析出晶体是
时析出晶体是![]() ,高于
,高于![]() 时
时![]() 分解成
分解成![]() 和
和![]() 。利用如图所示装置进行实验.
。利用如图所示装置进行实验.
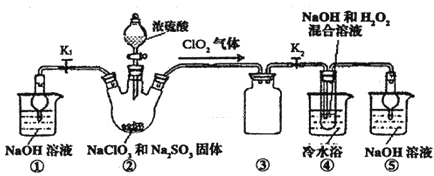
![]() 装置
装置![]() 的作用是 ______ ;装置
的作用是 ______ ;装置![]() 的作用是 ______ .
的作用是 ______ .
![]() 装置
装置![]() 中产生
中产生![]() 的还原剂是 ______ ;装置
的还原剂是 ______ ;装置![]() 中制备NaClO2的化学方程式为 ______ .
中制备NaClO2的化学方程式为 ______ .
![]() 从装置
从装置![]() 反应后的溶液获得
反应后的溶液获得![]() 晶体的操作步骤为:
晶体的操作步骤为:
![]() 减压,
减压,![]() 蒸发结晶;
蒸发结晶;
![]() 趁热过滤;
趁热过滤;
![]() ______ ;
______ ;
![]() 低于
低于![]() 干燥,得到成品.
干燥,得到成品.
实验Ⅱ:测定某亚氯酸钠样品的纯度.
设计如下实验方案,并进行实验:
![]() 准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应
准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应![]() 已知:
已知:![]() 将所得混合液配成250mL待测溶液.
将所得混合液配成250mL待测溶液.
![]() 移取
移取![]() 待测溶液于锥形瓶中,加几滴淀粉溶液,用c
待测溶液于锥形瓶中,加几滴淀粉溶液,用c ![]()
![]() 标准液滴定,至滴定终点。重复2次,测得平均值为V
标准液滴定,至滴定终点。重复2次,测得平均值为V ![]() 已知:
已知:![]()
![]() 达到滴定终点时的现象为 ______ .
达到滴定终点时的现象为 ______ .
![]() 该样品中
该样品中![]() 的质量分数为 ______
的质量分数为 ______ ![]() 用含m、c、V的代数式表示
用含m、c、V的代数式表示![]() .
.
![]() 在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为 ______ .
在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素( )能防治坏血病。
)能防治坏血病。
(1)维生素C属于___(填“无机化合物”或“有机化合物”)。
(2)维生素C中含氧官能团有酯基和___(填名称)。
(3)向维生素C溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有___性。
(4)维生素C具有还原性。向维生素C溶液中滴入几滴酸性KMnO4稀溶液,实验现象为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物X中可能含有FeO、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、KI、
、KI、![]() 中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图所示:
中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图所示:
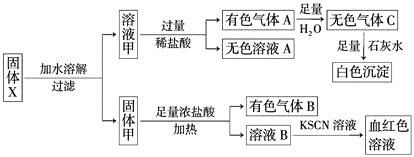
已知:![]()
![]() 在酸性环境下具有较强的氧化性
在酸性环境下具有较强的氧化性
![]() 无色,不溶于水且不与碱溶液反应
无色,不溶于水且不与碱溶液反应![]()
根据上述实验,下列说法中不正确的是 ![]()
![]()
A.X中一定含有![]() 、
、![]() 和
和![]()
B.X中一定没有![]() 和KI,可能含有
和KI,可能含有![]() 和
和![]()
C.X中至少有FeO、![]() 中的一种
中的一种
D.气体A一定含有![]() 、
、![]() 和
和![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
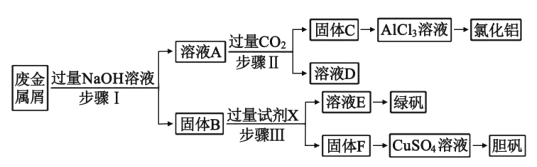
请回答:
(1)步骤Ⅰ中,发生的氧化还原反应的离子方程式为___,涉及到的分离操作是___。
(2)试剂X是___;溶液D是___。
(3)溶液E在空气中易被氧化,请设计一个简单的实验方案检验溶液E是否被氧化___。
(4)在步骤Ⅱ时,若用大理石与浓盐酸制取CO2并直接通入溶液A中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是___。
(5)工业上常用溶液E制取净水剂Na2FeO4,流程如图:
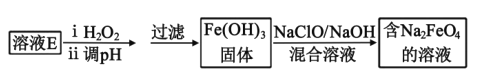
写出由Fe(OH)3制取Na2FeO4的离子方程式___。(已知NaClO还原为NaCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是人类提出的一个新理念,主要内容之一是从技术、经济上设计一种可行的化学反应,尽可能减少对环境的负面作用。
(1)下列化学反应符合绿色化学理念的有________(填序号)。
A 制![]() :
: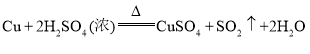
B 制![]() :
: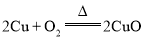 ,
,![]()
C 制![]() :
:![]()
D 制![]() :
: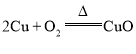 ,
,![]()
(2)对垃圾的分类处理,属于绿色化学的范畴。请你根据日常生活中所见到的垃圾设计几种处理的方法:________________,________________,________________,________________。
(3)废旧电池的处理尤为重要,如果随意丢弃,主要会造成________(填序号)
A 水体污染 B 大气污染 C 资源污染 D 土壤污染
废旧电池的处理方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3—二异丙烯基苯![]() 是重要的化工原料。下列有关1,3一二异丙烯基苯的说法正确的是
是重要的化工原料。下列有关1,3一二异丙烯基苯的说法正确的是
A.可以发生加成聚合反应B.不能使稀高锰酸钾溶液褪色
C.分子中所有原子共平面D.其苯环上的二氯代物有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化学中的反应类型较多,现有如下反应:
①乙醛发生银镜反应 ②由乙炔制氯乙烯 ③乙醇与浓氢溴酸混合共热④甲苯使酸性高锰酸钾溶液褪色⑤溴乙烷和氢氧化钠的乙醇溶液共热 ⑥苯酚与浓溴水的反应
(1)其中属于取代反应的是_____________,(填序号,下同)属于氧化反应的是__________________,属于加成反应的是__________________,属于消去反应的是_______________________.
(2)写出反应①的方程式_________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com