
【题目】如图所示,铁片、铜片和硫酸铜溶液可以构成原电池或电解池,下列说法不正确的是( )

A.构成原电池时,Cu极反应为![]()
B.构成电解池时,Fe电极质量一定减少
C.构成电解池时,Cu极质量可能增加也可能减少
D.构成的原电池或电解池在工作时的反应原理可能相同
【答案】B
【解析】
构成原电池时,较活泼的金属铁作负极,负极上金属失电子发生氧化反应,较不活泼的金属铜作正极,正极上得电子发生还原反应;构成电解池时,阳极上金属电极失电子发生氧化反应,阴极上铜离子得电子发生还原反应,据此解答。
A、构成原电池时,较不活泼的金属铜作正极,正极上溶液中铜离子得电子生成铜单质而析出,电极反应式为Cu2++2e=Cu,故A正确;
B、构成电解池时,连接电源正极的电极为阳极,阳极上金属电极失电子发生氧化反应,若a连接电源负极,则质量增加,故B错误;
C、构成电解池时,连接电源正极的电极为阳极,阳极上金属电极失电子发生氧化反应,连接电源负极的电极为阴极,阴极上铜离子得电子发生还原反应;如果b为阳极,电解池工作时,铜失电子生成铜离子进入溶液导致电极质量减少,如果b为阴极,溶液中铜离子得电子生成铜单质而析出附着在b电极上,导致电极质量增加,故C正确;
D、构成原电池时,负极上铁失去电子,正极上铜离子得电子而析出,构成电解池时,当铁电极为阳极时,铁失去电子,阴极上铜离子得电子而析出,其原理相同,故D正确。


科目:高中化学 来源: 题型:
【题目】F可用作丙烯酸酯橡胶的基材。以煤为原料制取F的一种合成路线如下:

(1)所用催化剂Fe在周期表的位置为:__________基态Mn原子价电子电子排布式为:__________ 。
(2)①的加工手段称为煤 __________(填“气化”“液化”或“干馏”)。
(3)②、④反应类型依次是________、________。
(4)E中所含官能团名称是________和________。
(5)C与A互为同系物,C的化学名称是________;F的结构简式为 ________。
(6)反应④的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸。发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云。根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等。运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等。
回答下列问题:
(1)在组成NH4NO3、NaCN两种物质的元素中第一电离能最大的是__________(填元素符号),解释原因_____________________________________________
(2)二甲基二硫和甲酸中,在水中溶解度较大的是 (填名称),原因是_______;烧碱所属的晶体类型为______;硫化碱(Na2S)的S2-的基态电子排布式是____________。
(3)硝酸铵中,NO3-的立体构型为 ,中心原子的杂化轨道类型为__________
(4)1mol化合物NaCN中CN-所含的π键数为______,与CN-互为等电子体的分子有 。(CN)2又称为拟卤素,实验室可以用氰化钠、二氧化锰和浓硫酸在加热条件下制得,写成该制备的化学方程式___________。
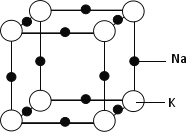
(5)钠钾合金属于金属晶体,其某种合金的晶胞结构如图所示。合金的化学式为____________;晶胞中K 原子的配位数为 ;已知金属原子半径r(Na)=186pm、r(K)=227pm,计算晶体的空间利用率 ________(列出计算式,不需要计算出结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析正确的是
A. CuS的溶解度大于PbS的溶解度
B. 原生铜的硫化物具有还原性,而铜蓝没有还原性
C. CuSO4与ZnS反应的离子方程式是![]()
![]() CuS↓
CuS↓
D. 整个过程涉及的反应类型有氧化还原反应和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新物质的发现、制备改变着我们的生活。下列物质或材料属于有机物的是( )
|
|
|
|
A.双氢青蒿素 | B.硅碳复合材料 | C.层状复合金属氧化物光催化材料 | D.砷化铌纳米带 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容密闭容器中发生可逆反应![]() ,X、Y、Z的初始浓度分别为2.0 mol·L-1和1.0 mol·L-1,2.0 mol·L-1,达平衡后,下列数据肯定不正确的是( )
,X、Y、Z的初始浓度分别为2.0 mol·L-1和1.0 mol·L-1,2.0 mol·L-1,达平衡后,下列数据肯定不正确的是( )
A.c(X)=0.5 mol·L-1B.c(Y)=0.5 mol·L-1
C.c(Z)=0.5 mol·L-1D.c(Z)=3.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到目的的是


A. 装置①用于测定生成氢气的速率
B. 装置②依据褪色快慢比较浓度对反应速率的影响
C. 装置③依据U管两边液面的高低判断Na和水反应的热效应
D. 装置④依据出现浑浊的快慢比较温度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时,Ksp[Zn(OH)2]=1.0×10-18,Ka(HCOOH)=1.0×10-4。该温度下,下列说法错误的是
A. Zn(OH)2溶于水形成的饱和溶液中c(Zn2+)>1.0×10-6 mol·L-l
B. HCOO-的水解常数为1.0×10-10
C. 向Zn(OH)2悬浊液中加入HCOOH,溶液中c(Zn2+)增大
D. Zn(OH)2+2HCOOH![]() =Zn2++2HCOO-+2H2O的平衡常数K=100
=Zn2++2HCOO-+2H2O的平衡常数K=100
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com