
��13�֣���ѧ�ڻ�������������ʮ����Ҫ�����á������������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
��1�������������У�H2�ܽ�NO ��ԭΪN2��25��ʱ����Ӧ����10 min����Һ��pH��7��Ϊ12�������£���
��ԭΪN2��25��ʱ����Ӧ����10 min����Һ��pH��7��Ϊ12�������£���
�� ��֪��pH=-lgc(H+),�����£�ˮ��Һ��c(H+)��c(OH-)=10-14 ��
��N2�ĽṹʽΪ________��
���벹�����ӷ���ʽ����������ƽ��������Ӧ���ӷ���ʽΪ(��ƽΪ1��ʡ��)
�� ��NO ���� ��H2���� �� ��N2���� ��H2O���� ��__________��
���� ��H2���� �� ��N2���� ��H2O���� ��__________��
��ƽ����Ӧ����v(NO )= mol��L��1��min��1��
)= mol��L��1��min��1��
��2���绯ѧ����NO ��ԭ����ͼ��ʾ��
��ԭ����ͼ��ʾ��
�ٵ�Դ����Ϊ________(�A����B��)��
������ӦʽΪ ��
������������ת����2 mol���ӣ���Ĥ������Һ�������仯��(��m������m��)Ϊ________g��
��1����N��N ��2�֣�
��2NO3?+5H2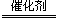 N2+2OH?+4H2O ��3�֣���ƽȫ�Ե�2�֣�OH?�Ե�1�֣� 0.001 ��2�֣�
N2+2OH?+4H2O ��3�֣���ƽȫ�Ե�2�֣�OH?�Ե�1�֣� 0.001 ��2�֣�
��2���� A ��2�֣�2NO3?+6H2O+10e?=N2��+12OH? ��3�֣�
��14.4 ��3�֣�
���������������1����N2������Nԭ�Ӽ��γ��˵������������ԽṹʽΪ��N��N��
�ڸ���ԭ���غ�͵���غ㣬�����ﻹ��OH?�����ݻ��ϼ۱仯��NԪ����+5�۽���Ϊ0�ۣ���N2Ϊ�о���������10�ۣ�H2��HԪ����0��������+1�ۣ�������2�ۣ����ݻ��ϼ����ߺͽ��͵ļ�����ȣ���ƽ�ɵ����ӷ���ʽ��2NO3?+5H2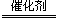 N2+2OH?+4H2O������pH=-lgc(H+)��pH��7��Ϊ12������Һ��H+Ũ����10-7��Ϊ10-12������ˮ��Һ��c(H+)��c(OH-)=10-14 ���ɵ�?c��OH?��=0.01mol?L?1����v(NO)=0.01mol?L?1��10min=0.001 mol��L��1��min��1��
N2+2OH?+4H2O������pH=-lgc(H+)��pH��7��Ϊ12������Һ��H+Ũ����10-7��Ϊ10-12������ˮ��Һ��c(H+)��c(OH-)=10-14 ���ɵ�?c��OH?��=0.01mol?L?1����v(NO)=0.01mol?L?1��10min=0.001 mol��L��1��min��1��
��2���ٵ��ص��Ҳ�NO3?ת��ΪN2��NԪ�صõ��ӷ�����ԭ��Ӧ����Ag��PtΪ���ص�������BΪ��Դ�ĸ��������Ե�Դ����ΪA����������NO3?�õ�������N2�����ݻ��ϼۺ͵���ת�ơ�ԭ���غ㡢����غ�ɵõ缫��ӦʽΪ��2NO3?+6H2O+10e?=N2��+12OH?
�ڵ��ص�������Ӧ:2H2O��4e?=4H++O2��������������ת����2 mol���ӣ��ų�0.5mol O2��2mol H+ͨ�����ӽ���Ĥ�����Ҳ࣬���������Һ�������٣�0.5mol��32g/mol+2mol��1g/mol=18g�����ص��Ҳ����Ӧ��2NO3?+6H2O+10e?=N2��+12OH?������������ת����2 mol���ӣ��ų�0.2mol N2����������2g H+�������Ҳ�������Һ�������٣�0.2mol��28g/mol��2g=3.6g����Ĥ������Һ�������仯��(��m������m��)Ϊ��18g��3.6g=14.4g��
���㣺���⿼�����ʵĽṹ�����ʡ�����ʽ����д�����ԭ������ؼ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����������ʵıȽϣ���ȷ����
| A�����ȶ��ԣ�Na2CO3>NaHCO3>H2CO3 |
| B���۵㣺K>Na>Li |
| C��ͬ�����£�ͬŨ����Һ��pHֵ��NaHCO3>Na2CO3 |
| D����ԭ�ԣ�S2->Br->I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������NO�ķ�Ӧԭ��Ϊ��2CO��2NO=N2��2CO2�йظ÷�Ӧ��˵������ȷ���� ( )
| A����Ӧ��COΪ������ |
| B����Ӧ��NO����ԭ |
| C���ڷ�Ӧ����1 mol N2ʱ��ת�Ƶĵ���Ϊ4 mol |
| D��CO��NO������ɫ�ж����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��10�֣�Ϊ�˲ⶨ���ᾧ�壨H2C2O4��xH2O���е�xֵ����������ʵ��
��1����ȡWg���ᾧ�壬���100.00mL��Һ
��2��ȡ25.00mL������Һ����ƿ�ڣ���������ϡH2SO4����Ũ��Ϊamol/L��KMnO4��Һ�ζ���KMnO4������ɫΪֹ���������ķ�ӦΪ�� 2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2��+2MnSO4+8H2O��
�Իش�
��ʵ���У���Ҫ�������У�����ţ� ����ȱ�ٵ������У������ƣ�
A������ƽ�������롢���ӣ� B�ζ��� C 100mL����Ͳ D��100mL������ƿ
E���ձ� F��©�� G����ƿ H�������� I��ҩ�� J����ƿ
��ʵ���У���KMnO4��ҺӦװ�� ʽ�ζ����У���Ϊ
�����ڽӽ��ζ��յ�ʱ������������ˮ����ƿ�ڱڳ�ϴһ�£��ټ��������յ㣬������õ�x��ֵ�� ����ƫ��ƫС����Ӱ�죩��
���ڵζ�����������ȥamol/L��KMnO4��ҺVmL���������ƵIJ�����Һ�����ʵ���Ũ��Ϊ mol/L���ɴˣ�x= ��
�����ζ��յ����ʱ���ӿ̶ȣ�������xֵ�� ����ƫ��ƫС����Ӱ�죩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(10��)Ϊ�˷�ֹǹ֧���⣬����ǹ֧�ĸ����������NaNO2��NaOH�Ļ��Һ�н��л�ѧ����ʹ���������������Fe3O4�����ܵı����㡪����������������̿������л�ѧ����ʽ��ʾ�� �� 3Fe��NaNO2��5NaOH��3Na2FeO2��H2O��NH3��
�� ��Na2FeO2����NaNO2����H2O ������Na2Fe2O4����NH3������NaOH
�� Na2FeO2��Na2Fe2O4��2H2O Fe3O4��4NaOH
Fe3O4��4NaOH
��1����ƽ��ѧ����ʽ�ڡ�
��2��������Ӧ���л�ԭ��Ϊ ������1mol Na2FeO2���ɣ���Ӧ�������� mol����ת�ơ�
��3�������γɡ��������Ĺ��̣�����˵����ȷ���� ��
| A�����������̲��������Ⱦ | B����Ӧ�����ɵ��������������п���ʴ���� |
| C����Ӧ�٢ڢ۾���������ԭ��Ӧ | D����Ӧ�٢��е���������ΪNaNO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������16�֣���ˮAlCl3�������л��ϳɵĴ�����ʳƷ���ɼ��ȡ���ҵ�Ʊ���ˮAlCl3���������£�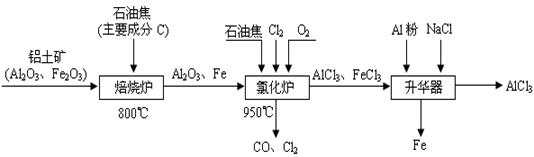
��1���Ȼ�¯��ͨ��O2��Ŀ���� _________��
��2���Ȼ�¯��Al2O3��C12��C��Ӧ�Ļ�ѧ����ʽ��____________________________��
��3���Ȼ�¯�е��������壬ͨ��������������Һ�����գ���д����Na2SO3��Һ����β��ʱ������Ӧ�����ӷ���ʽ___________________________________________________��
��4�����������м������۵�Ŀ����_________________________________________��
��5�����Ȼ������壨AlCl3��6H2O����HCl���м���Ҳ�ܽ�����ˮ�Ȼ������Ʊ�������ʵ���������Ʋ��������յõ��������Ǽ�ʽ�Ȼ���[��ѧʽΪAl2(OH)nCl(6-n)]����������ԭ�Ȼ������壨AlCl3��6H2O����40%���������n��ֵΪ ��
��6�����������У�������Ϊ�����������ε��Һ����Ԫ����Ҫ��AlCl4����ʽ���ڣ��������ĵ缫��ӦʽΪ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
þ�Ǻ�ˮ�к����϶�Ľ�����þ��þ�Ͻ���þ�Ļ������ڿ�ѧ�о���ҵ��������;�dz��㷺��
��1��Mg2Ni��һ�ִ���Ͻ���֪��
Mg(s) + H2(g)=MgH2(s) ��H1=��74.5kJ��mol��1
Mg2Ni(s) + 2H2(g)=Mg2NiH4(s) ��H2=��64.4kJ��mol��1
Mg2Ni(s)+2MgH2(s) = 2Mg(s)+Mg2NiH4(s) ��H3
���H3 = kJ��mol��1��
��2����ҵ�Ͽ��õ�����ڵ���ˮ�Ȼ�þ���þ�������Ȼ�þ��ˮ�ǹؼ�����֮һ��һ������������Ȼ�þ������ˮ�ķ����ǣ��Ƚ�MgCl2��6H2Oת��ΪMgCl2��NH4Cl��nNH3���þ���Σ�,Ȼ����700���Ѱ��õ���ˮ�Ȼ�þ���Ѱ���Ӧ�Ļ�ѧ����ʽΪ ����������Ȼ�þ�������ĵ缫��ӦʽΪ ��
��3���������Mg(AlH4)2��110-200��C�ķ�ӦΪ��Mg(AlH4)2=MgH2 +2A1+3H2��ÿ����27gAlת�Ƶ��ӵ����ʵ���Ϊ ��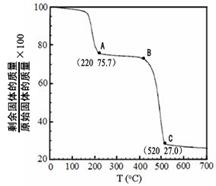
��4����ҵ����MgC2O4��2H2O�ȷֽ��Ƴ�ϸMgO�����ȷֽ�������ͼ��
ͼ�и�������������B��C������Ӧ�Ļ�ѧ����ʽΪ ��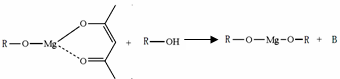
��5��һ���л�þ����������������ѧԪ����Ϳ��Һ����ѧʽ�ɱ�ʾΪ��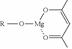 �����ɷ������·�Ӧ��
�����ɷ������·�Ӧ��
ROH��B�ĺ˴Ź�����������ͼ: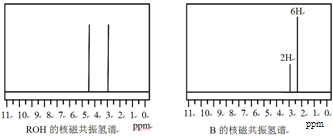
ROH��C��H��O��F����Ԫ����ɵĺ����л��������ֻ��1����ԭ�ӣ����з�ԭ�ӻ�ѧ������ͬ����Է�������Ϊ168����ROH�Ľṹ��ʽΪ �� B�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��50 mL a mol��L��1��������Һ�У�����6��4 g Cu������ȫ���ܽ⣬�һ�ԭ����ֻ��NO2��NO������Ӧ����Һ������ˮϡ����100 mL�����c(NO3-)��4 mol��L��1��
��1��ϡ�ͺ����Һ��c(H+)�� mol��L��1
��2����a��10�������ɵ�������NO2�����ʵ���Ϊ________mol
��3����������������Ⱦ�ķ���֮һ����NaOH��Һ�������գ���Ӧԭ�����£�
NO2��NO��2NaOH=2NaNO2��H2O 2NO2��2NaOH=NaNO2��NaNO3��H2O
������������屻1 mol��L��1��NaOH��Һǡ�����գ���NaOH��Һ�����Ϊ________mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
Ϊ֤��Fe3+���н�ǿ�������ԣ���ͬѧ��������ʵ�飺��CuƬ����0.5mol/L Fe(NO3)3��Һ�У��۲쵽CuƬ���ܽ⣬��Һ�ɻ�ɫ��Ϊ����ɫ���ɴ˼�ͬѧ�õ�Fe3+���н�ǿ�����ԵĽ��ۡ�
��ͬѧ����˲�ͬ�Ŀ�������Fe(NO3)3��Һ�������ԣ��ڴ�����������NO3-Ҳ������Cu���������ʵ�����̽������֪��
| ˮ�ⷴӦ | ƽ�ⳣ����K�� |
Fe3+ + 3H2O  Fe(OH)3 + 3H+ Fe(OH)3 + 3H+ | 7.9 �� 10-4 |
Fe2+ + 2H2O  Fe(OH)2 + 2H+ Fe(OH)2 + 2H+ | 3.2 �� 10-10 |
Cu2+ + 2H2O  Cu(OH)2 + 2H+ Cu(OH)2 + 2H+ | 3.2 �� 10-7 |
| ʵ������ | ʵ������ |
| ��ͬѧ��ʵ�鷽�� | ��Һ�������ɫ�� pH�������� |
| ��ͬѧ��ʵ�鷽�� | ����������pHû�����Ա仯�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com