
【题目】某学习小组用下图装置研究SO2的性质。
| 序号 | X | 实验现象 |
Ⅰ | 紫色石蕊溶液 | 现象a | |
Ⅱ | 品红溶液 | 溶液由红色变为无色,加热后又恢复原来的颜色 | |
Ⅲ | 酸性KMnO4溶液 | 溶液由紫色变为无色 |
请回答:
(1)实验Ⅰ中,现象a是______。
(2)根据实验Ⅱ,推断SO2的化学性质是______。
(3)根据实验Ⅲ,推断无色溶液中所含的离子是K+、Mn2+、H+和______。
(4)结合离子方程式说明实验中NaOH溶液的作用是______。
【答案】溶液由紫色变为红色 漂白性 SO42- SO2+2OH- =SO32-+H2O,吸收SO2防止环境污染
【解析】
(1) 二氧化硫为酸性氧化物,溶于水生成压力算,溶液显酸性;
(2) 二氧化硫具有漂白性,能够使品红溶液褪色;
(3) 根据氧化还原反应中化合价变化分析;
(4)二氧化氮有毒,需要用碱液吸收。
(1) 二氧化硫为酸性氧化物,溶于水生成亚硫酸,溶液显酸性,能使紫色石蕊变为红色;
(2) SO2能够使品红溶液褪色,说明SO2具有漂白性;
(3) 高锰酸钾具有强氧化性,能将SO2氧化,S元素从+4价升高到+6价,且氧化产物为SO42-;
(4) 二氧化硫有毒,需要用碱液吸收,避免污染环境,离子方程式为:SO2+2OH- =SO32-+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硼酸和硫酸镁是重要的化工原料。以硼铁混精矿[主要成分为MgBO2(OH)、UO2和Fe3O4,还有少量的Fe2O3、FeO、SiO2]为原料制备硼酸和硫酸镁的工艺流程如下:
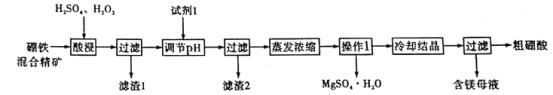
已知:①UO22+在pH为4-5的溶液中生成UO2(OH)2沉淀;②Fe2+和Fe3+沉淀完全的pH分别为9.7、3.7。
(1)酸浸过程中MgBO2(OH)与硫酸反应的离子方程式为_____。
(2)酸浸过程中加入H2O2的目的是______(写出两条),滤渣1的主要成分是___(填化学式)。
(3)试剂1最好选择_____(填化学式)。若调节溶液pH前,溶液中c(Mg2+)=0.2 mol/L,当溶液pH调至5时,UO2+沉淀完全,此时是否有Mg(OH)2沉淀生成____。{通过计算说明,Ksp[Mg(OH)2]=5.6×10-12}
(4)操作1的名称是_____。
(5)MgSO4·H2O加热脱水可以得无水MgSO4,那么MgCl2·6H2O晶体直接加热___(填“能”或“不能”)得到无水MgCl2,理由是_______。
(6)已知:H2CO3的Ka1=4.4×10-7,Ka2=4.7×10-11;H3BO3的Ka=5.8×10-10。向碳酸钠溶液里逐滴加入硼酸溶液____(填“有”或“无”)气泡产生,理由是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学方程式书写正确的是( )
A. CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B. H2C=CH2+Br2→CH3CHBr2
C. 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D. CH3CH2OH+CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯(C7H8)和二甲苯(C8H10)是重要的化工原料。利用苯(C6H6)和甲醇(CH3OH)在催化剂作用下反应得到C7H8、C8H10和副产物三甲苯(C9H12),发生的主要反应如下:
Ⅰ.C6H6(g)+CH3OH(g)C7H8(g)+H2O(g)
Ⅱ.C7H8(g)+CH3OH(g)C8H10(g)+H2O(g)
Ⅲ.C8H10(g)+CH3OH(g)C9H12(g)+H2O(g)
(1)500℃、0.18Mpa条件下,反应达到平衡时,结果如图所示。
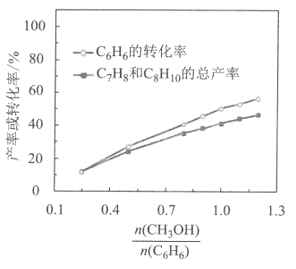
①由图分析,随着投料比![]() 增加,CH3OH的平衡转化率___,平衡时
增加,CH3OH的平衡转化率___,平衡时![]() 的值___。(填“增大”、“减小”或“不变”)
的值___。(填“增大”、“减小”或“不变”)
②投料比![]() 为1.0时,C6H6的平衡转化率为50%,产物中C7H8、C8H10和C9H12物质的量之比为6︰3︰1。CH3OH的平衡转化率为___,反应I的平衡常数K=___。
为1.0时,C6H6的平衡转化率为50%,产物中C7H8、C8H10和C9H12物质的量之比为6︰3︰1。CH3OH的平衡转化率为___,反应I的平衡常数K=___。
(2)我国学者结合实验与计算机模拟结果,研究了反应I在固体酸(HB)催化剂表面进行的反应历程如图所示。其中吸附在固体酸(HB)表面的物种用*标注。
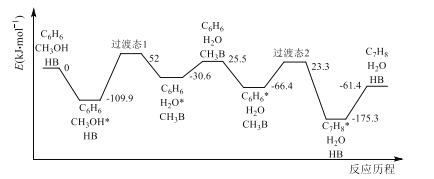
①反应I的H=___kJ·mol-1。
②吸附CH3OH的焓变___吸附C6H6的焓变(填“>”或“<”)。
③C6H6*在催化剂表面转化为C7H8*的反应方程式为___。
④在固体酸(HB)催化作用下,测得反应I的速率方程为v=kp(C6H6)(k为速率常数)。在刚性容器中发生反应I,关于反应I的平衡常数(K)和反应速率(v)的叙述正确的是__(填标号)。
A.升高温度,K和v均增大
B.增大p(C6H6),K不变,v增大
C.降低温度,K和v均减小
D.增大p(CH3OH),K不变,v增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以V2O5为原料制备氧钒(Ⅳ)碱式碳酸铵晶体{(NH4)5[(VO)6(CO3)4(OH)9]·10H2O},其流程如下:
V2O5![]() VOCl2溶液
VOCl2溶液![]() 氧钒(Ⅳ)碱式碳酸铵晶体
氧钒(Ⅳ)碱式碳酸铵晶体
(1)“还原”过程中的还原剂是____________(填化学式)。
(2)已知VO2+能被O2氧化,“转化”可在如图装置中进行。
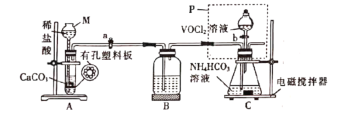
①仪器M的名称是___________,实验开始前的操作是_________。
②装置B的作用是__________________。
③加完VOCl2溶液后继续搅拌一段时间,使反应完全,再进行下列操作,顺序为_______(填字母)。
a.锥形瓶口塞上橡胶塞
b.取下P
c.将锥形瓶置于干燥器中,静置过夜
④得到紫红色晶体,抽滤,并用饱和NH4HCO3溶液洗涤3次,用无水乙醇洗涤2次,再用乙醚洗涤2次,抽干称重。用饱和NH4HCO3溶液洗涤除去的阴离子主要是_______(填离子符号),用无水乙醇洗涤的目的是_______________。
⑤称量![]() 产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol/L KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用c mol/L (NH4)2Fe(SO4)2标准溶液滴定至终点(已知滴定反应为
产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol/L KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用c mol/L (NH4)2Fe(SO4)2标准溶液滴定至终点(已知滴定反应为![]() +Fe2++2H+=VO2++Fe3++H2O),消耗标准溶液的体积为V mL。若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果______________(填“偏高”“偏低”或“无影响”),产品中钒的质量分数为_________(以VO2+的量进行计算,列出计算式)。
+Fe2++2H+=VO2++Fe3++H2O),消耗标准溶液的体积为V mL。若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果______________(填“偏高”“偏低”或“无影响”),产品中钒的质量分数为_________(以VO2+的量进行计算,列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多巴胺是一种重要的中枢神经传导物质,用来帮助细胞传送脉冲的化学物质,能影
响人对事物的欢愉感受。多巴胺可用香兰素与硝基甲烷等为原料按下列路线合成:
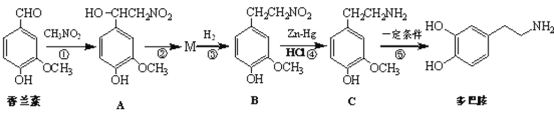
(1)香兰素保存不当往往会导致颜色、气味发生明显变化,其原因是___。
(2)多巴胺中的官能团的名称是___、___,反应①、⑤的反应类型分别为___、___。
(3)写出由A→M的化学方程式___。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①具有天然氨基酸的共同结构
②能与FeCl3溶液发生显色反应
③有6种不同化学环境的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是极其重要的化工原料,在工业、农业、医药、军事等领域应用广泛。工业上通常用接触法制硫酸,主要原料是硫铁矿和空气。接触法制硫酸的生产过程大致可分为三个阶段:二氧化硫的制取和净化;二氧化硫转化为三氧化硫;三氧化硫的吸收和硫酸的生成。为了防止环境污染并对尾气进行综合利用,硫酸厂常用氨水吸收尾气的SO2、SO3等气体,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。为了测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液50.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
实验 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L(标准状况) |
1 | 7.24 | 50.00 | 1.792 |
2 | 14.48 | 50.00 | 3.584 |
3 | 21.72 | 50.00 | 4.032 |
4 | 36.20 | 50.00 | 2.240 |
(1)由1组数据直接推测:1.81g样品进行同样实验时,生成氨气的体积(标准状况)为___L。
(2)试计算该混合物中(NH4)2SO4和 NH4HSO4的物质的量之比为___。
(3)求所用NaOH溶液的物质的量浓度___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二次电池装置如图所示,锂、充有催化剂的碳纳米管为电极,电解质能传导Li+。放电时生成的Li2CO3和C附着在电极上,充电时可使Li2CO3转化为Li、CO2和O2。下列说法不正确的是( )
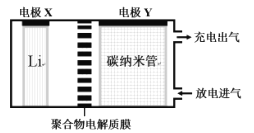
A.放电时,电流从电极Y经外电路流向电极X
B.充电时,电极X接外电源的正极发生氧化反应
C.充电时,电极Y的电极反应式为2Li2CO3-4e-=2CO2↑+O2↑+4Li+
D.应用该电池电镀铜,若析出64gCu,理论上消耗标况下33.6LCO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①②③
实验编号 | HA物质的量浓度/mol L-1 | NaOH物质的量浓度/moL- 1 | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请同答:
(1)根据①组实验情况,分析混合溶液的pH=9的原因是(用反应的离子方程式表示)___________________________
(2)在①组游液中下列关系式不正确的是(填序号字母)_______
A.c(Na+)+(H+)=c(OH-) +c(A-)
B.c(Na+ )=c(HA) +c(A-)
C.c(HA)+c(H+)=c(OH-)+c(Na+)
D. c(Na+)+(H+)=c(OH-) +c(A-)+c(HА)
(3)②组情况表明.c __________0.2 mol L-1(选填“> "、"<"或"="),混合溶液中离子浓度c(A-)________________c(Na+ )(选填“>"、"<"或=")
(4)从③组实验结果分析,说明HA的电离程度__________NaA的水解程度(选填“>"、“<"或“="),离子浓度由大到小的顺序是_____________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com