
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
A. ①④⑥B. ①②④C. ②③⑤D. ③⑤⑥
科目:高中化学 来源: 题型:
【题目】治理大气和水体污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)CO泄漏会导致人体中毒,用于检测CO的传感器的工作原理如图所示:写出电极I上发生的反应式:__。

工作一段时间后溶液中H2SO4的浓度__(填“变大”、“变小”或“不变”)
(2)用O2氧化HCl制取Cl2,可提高效益,减少污染。反应为:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g) H,通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:
2Cl2(g)+2H2O(g) H,通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:
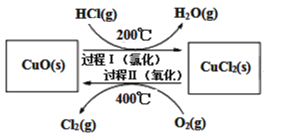
过程I的反应为:2HCl(g)+CuO(s)![]() CuCl2(s)+H2O(g) H1
CuCl2(s)+H2O(g) H1
过程II反应的热化学方程式(H2用含有H和H1的代数式表示)__。
(3)在温度T0℃,容积为1L的绝热容器中,充入0.2molNO2,发生反应:2NO2(g)![]() N2O4(g) H<0,容器中NO2的相关量随时间变化如图所示。
N2O4(g) H<0,容器中NO2的相关量随时间变化如图所示。
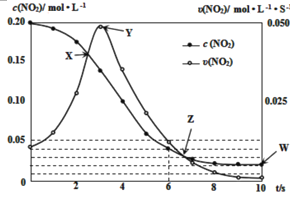
①反应到6s时,NO2的转化率是__。
②根据图示,以下各点表示反应达到平衡状态的是__。
a.X b.Y c.Z d.W
③0~3s内容器中NO2的反应速率增大,而3s后容器中NO2的反应速率减小了,原因是__。
④此容器中反应达平衡时,温度若为T1℃,此温度下的平衡常数K═__。
(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1molL-1的Na2SO3溶液吸收SO2,当溶液pH═7时,溶液中各离子浓度的大小关系为:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)═c(OH-)。(已知25℃时:H2SO3的电离常数Ka1═1.3×10-2,Ka2═6.2×10-8)请结合所学理论通过计算说明c(HSO3-)>c(SO32-)的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,还含有少量SiO2。现以卤块为原料按如图所示流程进行生产,用于制备金属镁。

请回答下列问题:
(1)步骤①中,为了加快酸溶速率,除了适当增加稀盐酸的浓度外,还可以采取的措施是____________(任写一条)。
(2)步骤②得到的X是___(填化学式),能够分离得到沉淀的方法是_____
(3)写出步骤④的化学方程式:_______
(4)步骤①中溶解卤块的盐酸如果过量太多造成的影响是____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制95mL 1 mol·L-1的稀硫酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的_______。

(2)配制稀硫酸时,除玻璃棒外还缺少的仪器是________________(写仪器名称);
(3)经计算,配制95mL1 mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为______mL,量取硫酸时应选用_________mL规格的量筒(填序号);
A.10 mL B.50 mL C.100 mL D.200mL
(4)取25 mL1 mol·L-1的硫酸,向其中加入一定量的氧化铜,充分反应后制得硫酸铜溶液。用该溶液制取CuSO4·5H2O,所需要的主要玻璃仪器除酒精灯、玻璃棒外,还缺少的仪器是___________;
(5)对所配制的稀硫酸进行测定,发现其浓度大于1 mol·L-1,配制过程中下列各项操作可能引起该误差的原因__________(填序号)。
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.定容时,俯视容量瓶刻度线进行定容
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
(1)汽车尾气中常含有碳烟、CO、NO等有害物质,尾气中含有碳烟的主要原因为___。
(2)已知在298K和101kPa条件下,有如下反应:
反应①:C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
反应②:N2(g)+O2(g)=2NO(g) ΔH2=+180.5kJ·mol-1
若反应![]() CO2(g)+
CO2(g)+![]() N2(g)
N2(g)![]() C(s)+NO(g)的活化能为akJ·mol-1,则反应C(s)+2NO(g)CO2(g)+N2(g)的活化能为___kJ·mol-1。
C(s)+NO(g)的活化能为akJ·mol-1,则反应C(s)+2NO(g)CO2(g)+N2(g)的活化能为___kJ·mol-1。
(3)在常压下,已知反应2CO(g)+2NO(g)N2(g)+2CO2(g) ΔH(298K)=-113.0kJ·mol-1,ΔS(298K)=-145.3J/(mol·K),据此可判断该反应在常温下___(填“能”或“不能”)自发进行。
(4)向容积为2L的真空密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)N2(g)+CO2(g),NO和N2的物质的量变化如表所示,在T1℃、T2℃分别到达平衡时容器的总压强分别为p1kPa、p2kPa。
物质的量/mol | T1℃ | T2℃ | |||||
0 | 5min | 10min | 15min | 20min | 25min | 30min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~10mi内,以NO表示的该反应速率v(NO)=___kPa·min-1。
②第15min后,温度调整到T2,数据变化如表所示,则p1___p2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2mol,再次达平衡时NO的体积百分含量为___。
(5)为探究温度及不同催化剂对反应2NO(g)+2CO(g)+N2(g)+2CO2(g)的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得NO转化率与温度的关系如图所示:

①在催化剂乙作用下,图中M点对应的速率(对应温度400℃)v正___v逆(填“>”、“<”或“=”),其理由为___。
②温度高于400℃,NO转化率降低的原因可能是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示的反应判断下列说法中错误的是

A. CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量
B. 该反应的焓变大于零
C. 该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量
D. 由该反应可推出凡是需要加热才发生的反应均为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。如图是废旧钻酸锂(LiCoO2)(含少量铁、铝、铜等元素的化合物)回收工艺流程:
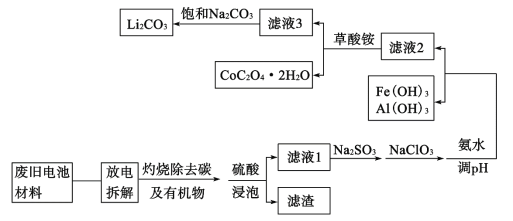
(1)“拆解”前需进入“放电”处理的目的是__;用食盐水浸泡是放电的常用方法,浸泡放电过程中产生的气体主要有__。
(2)上述流程中将CoO2-转化为Co3+的离子方程式为__。
(3)滤液1中加入Na2SO3的主要目的是__;加入NaClO3的主要目的是__。
(4)“沉钴”过程中,(NH4)2C2O4的加入量(图a)、沉淀反应的温度(图b)与钴的沉淀率关系如图所示:

根据图沉钴时应控制n(C2O42-):n(Co2+)比为__,温度控制在__℃左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量Fe、FeO、Fe2O3的混合物中,加入50mL1mol·L-1硫酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量为
A. 11.2g B. 2.8g C. 5.62g D. 无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com