
����Ŀ����������������ɴ�����Ⱦ����Ҫ���ʡ��о���������ķ�Ӧ��������������������Ⱦ����Ҫ���塣�ش�����������
��1����֪2NO(g) +O2(g)![]() -2NO2(g) ��H�ķ�Ӧ���̷�������
-2NO2(g) ��H�ķ�Ӧ���̷�������
��2NO( g )![]() N2O2 (g)( �� ) ��H1<0��v1��=k1��c2(NO)��v1��=k1��c2(N2O2)
N2O2 (g)( �� ) ��H1<0��v1��=k1��c2(NO)��v1��=k1��c2(N2O2)
��N2O2 (g)+ O2 (g) ![]() 2NO2(g)(��) ��H2<0��v2��=k2��c2(N2O2)c(O2)��v2��=k2��c2(NO2)
2NO2(g)(��) ��H2<0��v2��=k2��c2(N2O2)c(O2)��v2��=k2��c2(NO2)
�ȽϷ�Ӧ���Ļ��E1�뷴Ӧ���Ļ��E2�Ĵ�С: E1__ E2 (����>������<������=��) ���ж�������__________��2NO(g) +O2(g)![]() 2NO2(g) ��ƽ�ⳣ��K��������Ӧ���ʳ���k1����k1����k2���� k2���Ĺ�ϵʽΪ_______����֪��Ӧ���ʳ���k���¶����߶������������¶Ⱥ�k2���� k2���ֱ�����a����b������a____b (����>������<������=��)��һ�������£�2NO (g)+O2(g)
2NO2(g) ��ƽ�ⳣ��K��������Ӧ���ʳ���k1����k1����k2���� k2���Ĺ�ϵʽΪ_______����֪��Ӧ���ʳ���k���¶����߶������������¶Ⱥ�k2���� k2���ֱ�����a����b������a____b (����>������<������=��)��һ�������£�2NO (g)+O2(g) ![]() 2NO2 (g)��ƽ������ߵ�ij�¶ȣ��ٴ�ƽ���v2����ԭƽ���С�������������ʷ��̷����������Ľ�����_________________��
2NO2 (g)��ƽ������ߵ�ij�¶ȣ��ٴ�ƽ���v2����ԭƽ���С�������������ʷ��̷����������Ľ�����_________________��
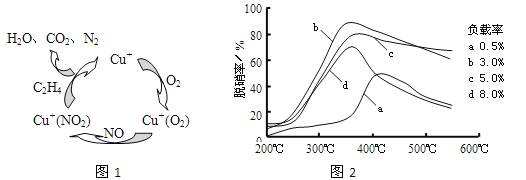
��2��������ϩ(C2H4)��Ϊ��ԭ������(NO)������������������ͼ��ʾ������Ӧ��n(NO): n(O2) =2 ��1�����ܷ�Ӧ�Ļ�ѧ����ʽΪ_______________�����������¶ȡ�������(����ɸ�д�������������) �Ĺ�ϵ������ͼ��Ϊ�ﵽ�������Ч����Ӧ���õ�������________________��
����NO��ֱ�Ӵ�NO�ֽ�����N2��O2�����䷴Ӧ������������(Vo��������Ѩ)��
2Ni2++2Vo+2NO��2Ni3++2O-+N2 2O-��O2-+1/2O2+Vo ______________
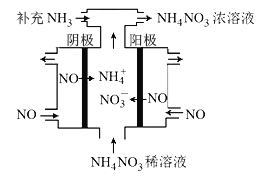
��3�����NO���Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ�������ĵ缫��ӦʽΪ______________��
���𰸡� �� ���Խ��һ����ӳ�Ϊ�����Խ�ѣ���Ӧ����Խ�� ![]() �� �¶����ߣ���Ӧ�����ڵ�ƽ������������ڷ�Ӧ�ٵ����ʴ���c(N2O2)��С����̶ȴ���k2����c(O2)����ij̶���ʹ���ߵij˻���v2����С 6NO+3O2+2C2H4
�� �¶����ߣ���Ӧ�����ڵ�ƽ������������ڷ�Ӧ�ٵ����ʴ���c(N2O2)��С����̶ȴ���k2����c(O2)����ij̶���ʹ���ߵij˻���v2����С 6NO+3O2+2C2H4![]() 3N2+4CO2+4H2O 350����������3.0% 2Ni3+ + O2-��2Ni2+ +VO+
3N2+4CO2+4H2O 350����������3.0% 2Ni3+ + O2-��2Ni2+ +VO+![]() O2 NO + 6H+ +5e- = NH4+ + H2O
O2 NO + 6H+ +5e- = NH4+ + H2O
����������1����2NO(g)![]() N2O2(g)(��)����N2O2(g)+ O2(g)
N2O2(g)(��)����N2O2(g)+ O2(g) ![]() 2NO2(g)(��) �����Խ��һ����ӳ�Ϊ�����Խ�ѣ���Ӧ����Խ������Ӧ�ٵĻ��E1����Ӧ�ڵĻ��E2����2NO(g)
2NO2(g)(��) �����Խ��һ����ӳ�Ϊ�����Խ�ѣ���Ӧ����Խ������Ӧ�ٵĻ��E1����Ӧ�ڵĻ��E2����2NO(g)![]() N2O2(g)(��) ��H1<0��v1��=k1��c2(NO)��v1��=k1��c2(N2O2)����N2O2(g)+ O2(g)
N2O2(g)(��) ��H1<0��v1��=k1��c2(NO)��v1��=k1��c2(N2O2)����N2O2(g)+ O2(g) ![]() 2NO2(g)(��) ��H2<0��v2��=k2��c2(N2O2)c(O2)��v2��=k2��c2(NO2)����Ŀ�귴Ӧ2NO��g��+O2��g��2NO2��g������H=��+��=��H1+��H2���ɷ�Ӧ��ƽ��״̬������v1��=v1����v2��=v2��������v1����v2��=v1����v2������k1��c2��NO����k2��c��N2O2��c��O2��=k1��c��N2O2����k2��c2��NO2������K=
2NO2(g)(��) ��H2<0��v2��=k2��c2(N2O2)c(O2)��v2��=k2��c2(NO2)����Ŀ�귴Ӧ2NO��g��+O2��g��2NO2��g������H=��+��=��H1+��H2���ɷ�Ӧ��ƽ��״̬������v1��=v1����v2��=v2��������v1����v2��=v1����v2������k1��c2��NO����k2��c��N2O2��c��O2��=k1��c��N2O2����k2��c2��NO2������K= =
=![]() ���÷�ӦΪ���ȷ�Ӧ���¶����ߣ���Ӧ�ڵ�ƽ�����ƣ�k2����k2������a��b��2NO(g)+O2(g)
���÷�ӦΪ���ȷ�Ӧ���¶����ߣ���Ӧ�ڵ�ƽ�����ƣ�k2����k2������a��b��2NO(g)+O2(g) ![]() 2NO2(g)Ϊ���ȷ�Ӧ���¶����ߣ���Ӧ�����ڵ�ƽ������ƣ����ڷ�Ӧ�ٵ����ʴ���c(N2O2)��С����̶ȴ���k2����c(O2)����ij̶ȣ�ʹ���ߵij˻���vspan>2����С���ʴ�Ϊ���������Խ��һ����ӳ�Ϊ�����Խ�ѣ���Ӧ����Խ����
2NO2(g)Ϊ���ȷ�Ӧ���¶����ߣ���Ӧ�����ڵ�ƽ������ƣ����ڷ�Ӧ�ٵ����ʴ���c(N2O2)��С����̶ȴ���k2����c(O2)����ij̶ȣ�ʹ���ߵij˻���vspan>2����С���ʴ�Ϊ���������Խ��һ����ӳ�Ϊ�����Խ�ѣ���Ӧ����Խ���� ![]() �������¶����ߣ���Ӧ�����ڵ�ƽ������ƣ����ڷ�Ӧ�ٵ����ʴ���c(N2O2)��С����̶ȴ���k2����c(O2)����ij̶ȣ�ʹ���ߵij˻���v2����С��
�������¶����ߣ���Ӧ�����ڵ�ƽ������ƣ����ڷ�Ӧ�ٵ����ʴ���c(N2O2)��С����̶ȴ���k2����c(O2)����ij̶ȣ�ʹ���ߵij˻���v2����С��
��2���ٸ���ͼʾ��֪���ڴ����������£�C2H4��NO��O2��Ӧ��������N2��CO2��H2O����Ӧ��n(NO):n(O2) =2��1����Ӧ�ܷ���ʽΪ6NO+3O2+2C2H4![]() 3N2+4CO2+4H2O����ͼ��֪��b���ߵ���ߵ㴦�������ʸߣ������ʵͣ����˵��¶ȣ��ʺ�����Ϊ350�桢������3%���ʴ�Ϊ��6NO+3O2+2C2H4
3N2+4CO2+4H2O����ͼ��֪��b���ߵ���ߵ㴦�������ʸߣ������ʵͣ����˵��¶ȣ��ʺ�����Ϊ350�桢������3%���ʴ�Ϊ��6NO+3O2+2C2H4![]() 3N2+4CO2+4H2O��350�桢������3.0%��
3N2+4CO2+4H2O��350�桢������3.0%��
����NO��ֱ�Ӵ�NO�ֽ�����N2��O2����Ӧ���ܷ�ӦΪ2NO![]() O2+N2�����ݷ�Ӧԭ����Ni2+Ϊ���������ܷ�Ӧ-��2Ni2++2Vo+2NO��2Ni3++2O-+N2��-��2O-��+O2-+1/2O2+Vo)�ã�2Ni3+ + O2-��2Ni2+ +VO+
O2+N2�����ݷ�Ӧԭ����Ni2+Ϊ���������ܷ�Ӧ-��2Ni2++2Vo+2NO��2Ni3++2O-+N2��-��2O-��+O2-+1/2O2+Vo)�ã�2Ni3+ + O2-��2Ni2+ +VO+![]() O2���ʴ�Ϊ��2Ni3+ + O2-��2Ni2+ +VO+
O2���ʴ�Ϊ��2Ni3+ + O2-��2Ni2+ +VO+![]() O2��
O2��
��3�����NO�Ʊ�NH4NO3��������ӦΪNO-3e-+2H2O=NO3-+4H+��������ӦΪ��NO+5e-+6H+=NH4++H2O���ʴ�Ϊ��NO + 6H+ +5e- = NH4+ + H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������װ���Ʊ�������������,��̽����ز������ʡ�
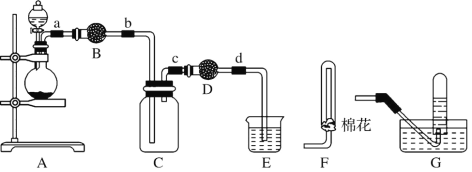
(1) װ��A�еķ�Һ©��ʢװ��Һ����____,��ƿ��Ԥ�ȼ������ͭм,���ļ۸��ͭ�ļ۸��,�˴���ͭ��������ԭ����______________��
(2) �����B��D��ʢװ�ĸ����������____(�Ũ���ᡱ������ˮ�Ȼ��ơ��������������ס���ʯ�ҡ�),�����D�и������������______________��
(3) װ��E������������β��,���չ����з�����Ӧ�Ļ�ѧ����ʽ����,�뽫�䲹��������
NaOH+ NO2![]() ������+ NaNO2+ H2O ______
������+ NaNO2+ H2O ______
(4) ij��ѧ��ȤС����Ϊͭ������Ũ���ᷴӦ�����������к�NO,ѡ�����б�Ҫ��װ��(N2��O2�����������ɿ���)�����֤ʵ�顣
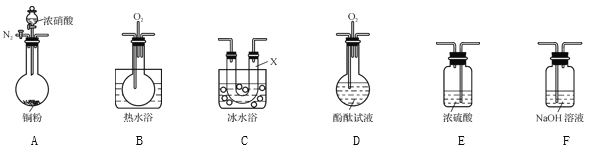
��֪:
i. NO+NO2+2OH-![]() 2NO2-+H2O
2NO2-+H2O
ii����Һ���¶�����:
���� | NO2 | NO |
Һ���¶� | 21 �� | -152 �� |
������������˳��(�������������,���������ĸ)Ϊ________��
��ʵ��ʱ�ȼ��װ�������Ժ�,�ټ����Լ�,�ڷ�Ӧǰ�IJ�����_______��
��ȷ�������к�NO��������__________;װ��C��������____��
��NH3����ԭ��������(SCR)������ĿǰӦ����㷺�������е��������ѳ�������������NO��NO2�Ļ����6 L,����ͬ��ͬѹ��7 L NH3ǡ��ʹ����ȫת��ΪN2,��ԭ���������NO��NO2�����ʵ���֮��Ϊ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��µĶ����ܱ������У����������������ٱ仯ʱ���ɱ�����Ӧ��A(g)��B(g)![]() C(g)��D(g) �Ѵﻯѧƽ��״̬���ǣ� ��
C(g)��D(g) �Ѵﻯѧƽ��״̬���ǣ� ��
A. ��������ѹǿ B. B�����ʵ���Ũ�� C. ���������ܶ� D. v(A)�� = v(D)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Һ���������Һ���ַ�ɢϵ�����ɢ�ʵĸ���������
A.�Ƿ���������ЧӦB.��ɢ����ֱ���Ĵ�С
C.�Ƿ��һ���ȶ�����D.�Ƿ�������ֽ����Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ĺ��ɽ���Ԫ�أ�ͨ�������Ͻ���ֵ����Ӽ�������ǿ�Ͻ��ǿ�ȡ�Ӳ�ȡ��ɺ��Եȡ������ƾ���(Na2MoO4��2H2O)����Ϊ��������ȴˮϵͳ�Ľ�����ʴ���Ƽ�����ͼ15�ǻ����������Ի����(��Ҫ�ɷ�Ϊ����MoS2)Ϊԭ�����Ʊ������⡢�����ƾ������Ҫ����ͼ��
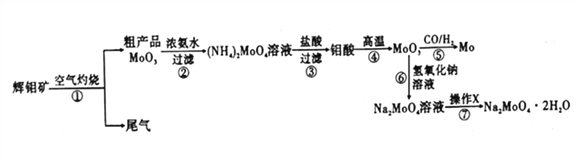
�ش���������:
��1����֪��Ӧ��Ϊ���ֽⷴӦ����������Կ�Ļ��ϼ�Ϊ___________��
��2����Ӧ�������ӷ���ʽΪ___________��
��3�����������ʱ�Ļ�ѧ����ʽΪ____________��
��4������XΪ_________����֪��������һ���¶ȷ�Χ�ڵ��������ʼ���Ӧ���ʵ��ܽ�����±���ʾ�����ڲ���X��Ӧ�����¶ȵ���ѷ�ΧΪ_______(�����)��
�¶�(��) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
�������� | Na2MoO4��10H2O | Na2MoO4��2H2O | Na2MoO4 | ||||||
�ܽ�� | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45.57 | |
A.0�桫10�� B.10�桫100�� C.15.5�桫50�� D.100������
��5���Ʊ������ƾ��廹����ͨ�����ƵĻ������ֱ�Ӽ������������Һ�����ķ����������������У��������������ɣ����������뻹ԭ�������ʵ���֮��Ϊ_________��
��6��Li��MoS2�ɳ���صĹ���ԭ��ΪxLi+nMoS2![]() Lix(MoS2)n[Lix(MoS2)n�����ڵ缫��]�����س��ʱ�����ĵ缫��ӦʽΪ___________________��
Lix(MoS2)n[Lix(MoS2)n�����ڵ缫��]�����س��ʱ�����ĵ缫��ӦʽΪ___________________��
��7�����û�ԭ������(CO��H2)��ԭMoO3���⣬ҵ���Ʊ���ԭ������CO��H2�ķ�Ӧԭ��֮һΪCO2+CH4![]() 2CO+2H2���������������Ϊ90%��7L(��״��)��Ȼ��������������̼�ڸ����·�Ӧ������ת����Ϊ80%,�ò�����CO��H2��ԭMoO3���⣬�������������������Ϊ_________��
2CO+2H2���������������Ϊ90%��7L(��״��)��Ȼ��������������̼�ڸ����·�Ӧ������ת����Ϊ80%,�ò�����CO��H2��ԭMoO3���⣬�������������������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�����þ��CO2�ķ�Ӧ���ʵ��̽��þ��NO2�ķ�Ӧ��
��ͬѧ�Ʋ������MgO��N2��
��ͬѧ�Ʋ�������MgO��N2�⣬�����л����ܺ���Y��
��С��ͬѧ���������װ��̽��þ��NO2��Ӧ�Ĺ��������ⶨ����ɡ�

��1��ʵ�鿪ʼʱ���ȹر�ֹˮ�к���ɼУ��ٴ�Һ©����������Ӳ�ʲ����ܳ�������ɫ�����ֹˮ�У��رյ��ɼУ�����ȼ�ƾ��ơ���������Ŀ����___________________________________________________________
��2��װ��B�е��Լ�����ѡ��________
A��Ũ���� B����ˮ�Ȼ��� C������������ D����ʯ��
��3��װ��C��ʢװ����������Һ�������ǣ�___________________________________
��4��Ϊ��֤�������������ȷ�ԣ���ȡ��Ͳ�̶�ʱӦע��������Ǣ�����ָ��������ٶ�������_______________________________����______________________________��
��5��ʵ���������ͬѧ�ǽ��������ȡ����ˮ��Ӧ�������д̼�����ζ�������������������ʹʪ���ʯ����ֽ������˵������ͬѧ�Ʋ���ȷ����д��Y��ˮ��Ӧ�Ļ�ѧ����ʽ__________________________________
��6������ʼ����þ������Ϊ3.6 g����������NO2�г�ַ�Ӧ�� ���ռ���N2���Ϊ448mL (��״��)���������MgO��������_________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɱ��顢��ϩ����Ȳ��ɵĻ�����壬��ȫȼ�պ�����CO2��H2O�����ʵ�����ͬ��ԭ���������������������Ȳ�������(����)
A. 1��2��1 B. 3��2��3 C. 2��5��2 D. 1��2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������մ���Һ���������Ժͽ�ǿ�Ļ�ԭ�ԣ�����֯��Ư������ȼ������������еĻ�ԭ������������ƣ�Na2S2O3�������������ƺ����ͨ�����Ϸ�Ӧ�Ƶã�װ����ͼI��ʾ��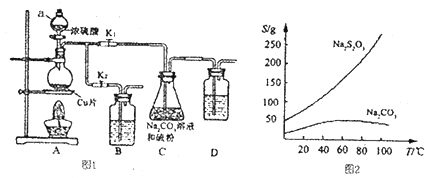
��֪��Na2S2O3��������Һ�в����ȶ����ڣ��й����ʵ��ܽ��������ͼ2��ʾ��
��1��Na2S2O35H2O���Ʊ���
����1����ͼ���Ӻ�װ�ú�δװҩƷ�������A��Cװ�������ԵIJ�����_ ��
����2������ҩƷ����K1���ر�K2�����ȣ�װ��B��D�е�ҩƷ��ѡ�����������е������ţ���
A��NaOH��Һ B��ŨH2S04C������KMnO4��Һ D������NaHCO3��Һ
����3��C�л��Һ��������������Ӧһ��ʱ�����۵������٣�
����4������C�еĻ��Һ������Һ��������Ũ�������ȹ��ˣ��ٽ���Һ���ˡ�ϴ�ӡ���ɣ��õ���Ʒ��
��2��Na2S2O3���ʵļ��飺��������������ˮ�еμ�����Na2S2O3��Һ����ˮ��ɫ��dz����鷴Ӧ����Һ�к����������д���÷�Ӧ�Ļ�ѧ����ʽ ��
��3������Na2S2O3��Һ�ⶨ��ˮ��Ba2+Ũ�ȣ��������£�ȡ��ˮ25.00mL�������ʵ�����ȼ�������K2Cr2O7��Һ����BaCrO4���������ˡ�ϴ�Ӻ�������ϡ�����ܽ⣮��ʱCr42��ȫ��ת��ΪCr2O72�����ټӹ���KI��Һ����ַ�Ӧ���������Һ��ָʾ������0.010molL��1��Na2S2O3��Һ���еζ�����Ӧ��ȫʱ������Na2S2O3��Һ18.00mL�����ַ�Ӧ�����ӷ���ʽΪ��Cr2O72��+6I��+14H+�T2Cr3++3I2+7H2O��I2+2S2O32���TS4O62��+2I�� �� ��÷�ˮ��Ba2+�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������е�һ����Ҫ��Ӧ��SO2��400��500���µĴ�������2SO2+O2![]() 2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������
2SO3������һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н��У������й�˵���д������
A. �����������£�SO2������100%��ת��ΪSO3
B. ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч��
C. Ϊ�����SO2��ת���ʣ�Ӧ�ʵ����O2��Ũ��
D. �ﵽƽ��ʱ��SO2��Ũ����SO3��Ũ��һ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com